Klīniskā gadījuma demonstrācijas mērķis — aktualizēt retu autoimūnu skrimšļaudu patoloģiju, slimības radītās komplikācijas un raksturot empīriskās terapijas pamatprincipus, kas izriet no atsevišķiem publicētiem klīniskiem gadījumiem.
Klīniskais gadījums
Pacients, 18 gadus vecs, 2014. gada 1. oktobrī stacionēts P. Stradiņa KUS LOR nodaļā ar sūdzībām par balss aizsmakumu un sēcošu, apgrūtinātu elpošanu naktī, reiboni, pārvests no Bērnu klīniskās universitātes slimnīcas.
Slimības anamnēze
Pirmās sūdzības parādījušās 2013. gada septembrī (17 gadu vecumā): reibonis, galvassāpes, troksnis labajā ausī. Stacionēts Bērnu KUS, kur izmeklēts un izrak-stīts ar diagnozi "akūts labās puses sekretors otīts. Perifērs vestibulārs sindroms".
2014. gada augustā atkārtoti stacionēts Bērnu KUS ar sūdzībām par vienu mēnesi ilgu balss aizsmakumu, apgrūtinātu elpošanu, stridoru. Izrakstīts ar diagnozi "alerģisks laringīts".
2014. gada 6. septembrī pacients ieradies uz LOR ambulatoro kontroli ar sūdzībām par pieaugošu balss aizsmakumu, subfebrilu temperatūru un sāpēm mutē. Stacionēts Bērnu KUS, kur konstatē subakūtu laringītu, mutes dobuma kandidozi.
Analīžu rezultāti 6. septembrī: Leu 19,59 tk., Neu leu 74,4%, Ly 14,4%, Mo 9,7%, Er 5,6 milj., Hgb 143 g/l, Tr 310 000; CRO 29,95 mg/l.
Terapijā ordinētie līdzekļi: Sol. Ceftriaxoni 10 dienas, T. Azytromicini 2 dienas, Mundgel mutes dobuma kopšanai 8 dienas, T. Medroli 32 mg 23.-29.09. Izrak-stoties saglabājas sūdzības par galvas reiboni, pie dziļas ieelpas dzirdama stridoroza elpošana. Balss vēl izmainīta, taču dinamika pozitīva.
Objektīvā izmeklēšana un terapija
2014. gada 1. oktobrī PSKUS objektīvi: balsenes tūska izteiktāka neīsto balssaišu rajonā, īstās balssaites ap-sārtušas, fonācijā slēdzas, bet ieelpā atveras nepilnīgi. Mutes dobuma kandidoze.
Audiogramma - 1. pakāpes sensoneirāla vājdzirdība labajā pusē.
Terapijā ordinē S. Dexamethasoni 20 mg i/v samazinošā devā. Dinamikā balsenes tūska mazinās, pašsajūta uzlabojas. Trīs dienas pēc deksametazona atcelšanas - temperatūra 39 °C, CRO 170 mg/l, terapijā pievieno T. Amoxiclavi 1 g × 2, atsāk S. Dexamethasoni 20 mg i/v samazinošā devā.
13. oktobrī - pacients praktiski nedzird teikto, bet ar katru nākamo reizi dzirde atgriežas, taču nesasniedz normas robežu. GK terapijas fonā - CRO 39 mg/l.
Imunoloģija: HLA B27 - neg., ANA, ENA, Av dsDNS - neg., C3, C4 - norma, pANCA, cANCA - neg., Av pret fosfolipīdiem, kardiolipīniem - neg., anti HIV1/2 - neg., TPHA - neg.
Ārstu konsilijs par tālāko taktiku. Izvērtējot slimības gaitu, terapiju, objektīvos datus (sedlveida deguns, balsenes tūska, sensoneirāla vājdzirdība, DT un MRI datus), pozitīvo dinamiku uz GK ievadi un negatīvo dinamiku, šos preparātus atceļot, tiek pieņemts lēmums par pagaidām neprecizētu sistēmisku slimību. Nolemts sagaidīt visus histoloģiskos rezultātus un atkārtoti pieaicināt reimatologu.
Terapijā sākt S. Solumedroli 500 mg × 1 i/v 3 dienas.
MRI galvai un kaklam (14.10.2014.; skat. 1. attēlu). Slēdziens: iekšējās auss struktūrās, balsenes skrimšļu daļēja destrukcija un iekaisums, pārsvarā vairogskrimšļa labā lapiņa, cartilago cricoidea riņķa mugurējā daļā, articulatio arythenoidea, dažādās pakāpēs, kreisais vairāk izteikti - ar fragmentāciju, dislokāciju un izteiktu tūsku. Izteikta balsenes tūska.
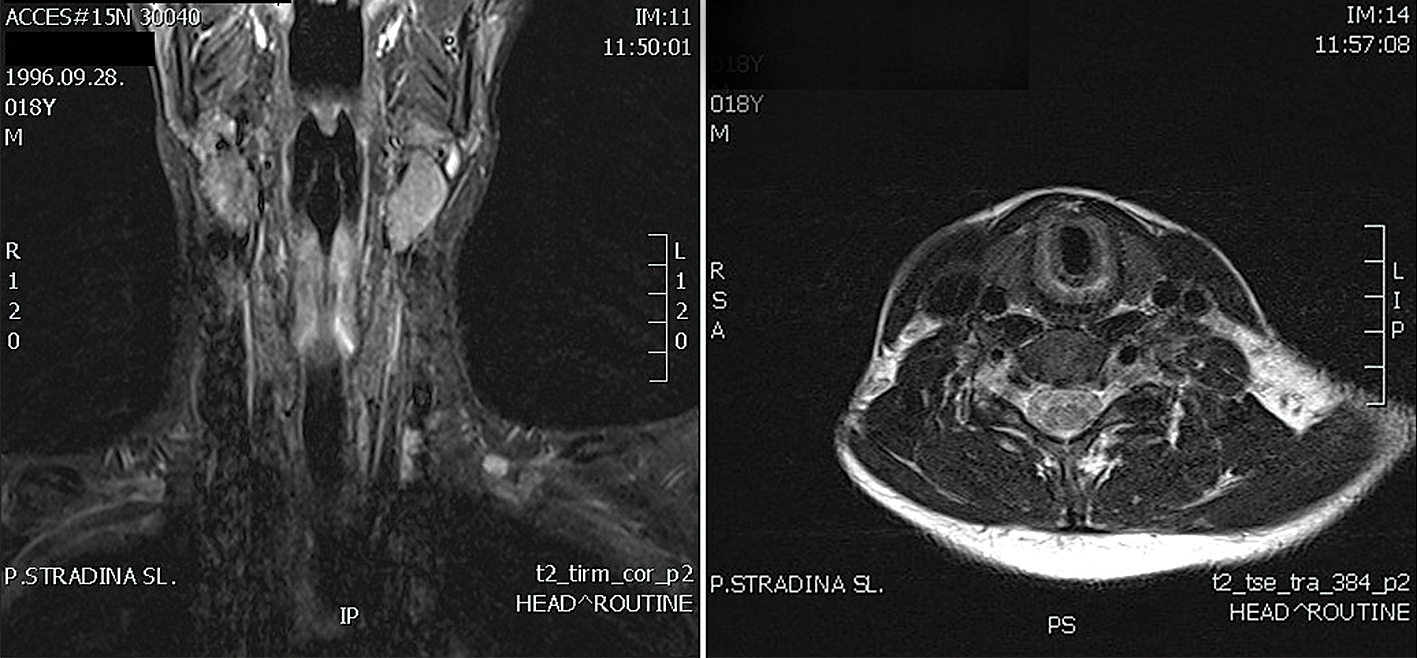

1. attēls
MRI galvai un kaklam
Difūzijas ADC kartē visi izmainītie skrimšļi ar augstu ADC koeficientu, kas atbilst iekaisumam.
Audiogramma 21.10.2014. dinamikā: visās frekvencēs vērojama dzirdes sliekšņa pazemināšanās par 10-20 dB. Akūta abpusēja sensoneirāla vājdzirdība.
Deguna starpsienas, neīsto balssaišu, trahejas, bronhu biopsijā - nav datu par granulomatozu iekaisumu vai sistēmisku slimību.
21.10.2014. pacients tiek izrakstīts no LOR nodaļas ar rekomendācijām turpināt šādu medikamentu lietošanu: T. Medroli 32 mg × 1 no rīta, 16 mg × 1 vakarā 3 nedēļas, tad medrola devu ik 2 nedēļas mazināt par 4 mg. Sākt lietot T. Azathioprini 50 mg × 1 dienā, pēc 10 dienām analīžu kontrole. Ja panesība apmierinoša, tad T. Azathioprini 50 mg × 2.
Atkārtota stacionēšana
30.10.2014. pacients stacionēts ar sūdzībām par dzirdes zudumu no 29.10. Sūdzas par balss aizsmakumu, sēcošu elpošanu, kas izteiktāka naktī.
LOR 30.10.2014. Balss sprauga elpošanai pietiekama. Balssaites kustīgas, tūskainas. Deguna ejas tīras. Aizdegune un rīkle brīva. Slēdziens: sensoneirāla vājdzirdība. Tūska balsenē saistīta ar sistēmas slimību.
Analīžu rezultāti: Leu 17,7 tk., Er 5,4 milj., Hgb 148 g/l, Tr 235 000.
Bioķīmija: AlAT 92 v/l, AsAT 19 v/l, kreatinīns 41 μmol/l, CRO 0,2 mg/l.
Slimības aktivitātes dēļ palielina imūnsupresīvo medikamentu devas: S. Solumedroli 750 mg i/v 6 dienas → 500 mg i/v 3 dienas, sāk pirmo S. Cyclophosfamidi 400 mg i/v infūziju.
Ambulatori rekomendē T. Medroli 64 mg × 1 no rīta, 16 mg × 1 vakarā, kombinējot ar Caps. Omeprasoli 20 mg × 1 kuņģa gļotādas aizsardzībai, kā arī turpināt S. Cyclophosfamidi 400 mg i/v ik 2 nedēļas.
13.11.2014. sūdzas par dzirdes pasliktināšanos, pievienojies troksnis kreisajā ausī. Kreisā auss "aizkritusi". Saziņa ar pacientu notiek rakstveidā. Sūdzības par sēcošu, skaļu elpošanu naktī. Stacionēts otrajai ciklofosfamīda infūzijai.
Par izteikto stridoru naktī pacientu ambulatori konsultē miega speciālisti. Naktī sāk neinvazīvu ventilāciju ar CPAP, kas ir bez efekta, vēlāk pāriet uz BiPAP.
04.12.2014. Ārstu konsilijs par tālāko ārstēšanas taktiku. Izvērtē MRI galvai dinamikā: iekšējā ausī izmainīts signāls, kas liecina par procesa aktivitāti. Dzirdes zudums skaidrojams ar izmaiņām iekšējās matiņšūnās. Nolemj sākt S. Solumedroli 500 mg × 1 i/v 3 dienas.
DT balsenei 04.12.2014.: salīdzinot ar izmeklējumu 12. oktobrī, mazinājusies balsenes tūska un muskuļu tūska pie vairogskrimšļa plātnītes. Stenoze īsto balssaišu līmenī. Labās balssaites parēze. Iekšējas laringocēles. Skrimšļi nav atjaunojušies. Kausiņskrimslis nepareizā lokalizācijā. Gredzenskrimslis ar fragmentāciju. Trahejas skrimšļi bez patoloģiskām izmaiņām.
Naktī no 5. uz 6. decembri plkst. 3.15 - dežūrreanimatologa konsultācija samaņas traucējumu, krampju lēkmes, cianotiskas sejas krāsas dēļ. Pacients bezsamaņā, kontakta nav. Acu zīlītes vidēji platas, diverģē. Cīpslu refleksi simetriski, abpusēji ↑. Āda sausa, perifēri vēsa. Seja cianotiska. Elpo 8 ×/min. Stridorozas elpošanas skaņas. SpO2 65%. TA 110/60 mmHg.
Slēdziens: balsenes tūska, progresējoša elpošanas mazspēja. Stāvoklis pēc ģeneralizētas krampju lēkmes (hipoksiskas?). Autoimūns recidivējošs polihondrīts.
Elpceļu nodrošināšanai indicēta endotraheāla intubācija. Tālākai terapijai pārved uz reanimācijas nodaļu. RAN turpina MPV, vispārējais stāvoklis stabilizējas.
8. decembrī ārstu konsilijs par tālāko taktiku. Nav ievērojamas uzlabošanās no līdzšinējās terapijas, progresē balsenes tūska, sākta MPV.
Pacientam indicēta traheostomija.
Turpināma imūnsupresīvā terapija ar S. Solumedroli 500 mg × 1 i/v.
Par tālāko terapijas taktiku, bioloģisko medikamentu lietošanas sākšanu lemj 9. decembrī prof. D. Andersones vizītes laikā 26. nodaļā.
Pacientam RAN tiek veikta traheostomija, elpo spontāni caur traheostomijas kanili, pie samaņas, adekvāti komunicē, sazināšanās rakstiski. Tālākai terapijai pārved uz pulmonoloģijas nodaļu. Pulmonoloģijas nodaļā sākta pacienta aktivācija, pacients atsācis staigāt.
Reimatologu konsilijs 9. decembrī: tā kā glikokortikoīdiem lielās devās un terapijai ar ciklofosfamīdu nav pozitīva efekta, nolemts sākt bioloģisko medikamentu TNFα blokatoru S. Etanecept 25 mg s.c. ievadi × 2 nedēļā.
LOR konsultācija 17. decembrī: elpošana caur traheostomu. Balsene - balss sprauga ievērojami platāka, tūsku nevēro. Balssaites pelēcīgas. Pie ieejas barības vadā tūsku nevēro. Turpina pamatslimības ārstēšanu.
Lietojot dzirdes aparātu, spēj sazināties ar apkārtējiem, dzirde uzlabojusies.
Terapijā: S. Solumedroli 250 mg i/v → T. Medroli 32 mg × 1 p.o. → izraksta tālākai terapijai ambulatori ar T. Medroli 28 mg × 1 dienā. Caps. Omeprazoli 20 mg × 1.
S. Etanercept 25 mg s.c. × 2 nedēļā.
Galīgā klīniskā diagnoze
- Recidivējošs polihondrīts.
- Balsenes tūska, dekompensēta. MPV 6.-9.12.2014., traheostoma no 8.12.2014.
- Daļēja c. cricoidea, c. arythenoidea, c. thyroidea destrukcija.
- Abpusēja sensoneirāla vājdzirdība.
- Sedlveida deguns.
- Perifērs reibonis.
Rekomendācijas
Izrakstot no pulmonoloģijas nodaļas 30. decembrī, pacientam rekomendē turpināt imūnsupresīvo terapiju: T. Medroli 28 mg × 1 dienā no rīta vēl 2 nedēļas, tad devu pakāpeniski ik 2 nedēļas par 4 mg mazināt līdz T. Medroli 20 mg × 1 dienā. Devas tālākā mazināšana atkarīga no reimatologa rekomendācijām.
S. Etanercept 25 mg s.c. × 2 nedēļā. Kontrole pie reimatologa 2015. gada janvāra beigās, kad dinamikā plāno DT balsenei dienas stacionārā.
Recidivējošs polihondrīts
Recidivējošs polihondrīts (RP) ir multisistēmiska nezināmas etioloģijas autoimūna slimība, kas parasti skar skrimšļaudu struktūras ausīs, degunā, hialoīdo skrimsli perifērajās locītavās, kā arī trahejas un bronhu skrimšļus. Iekaisums var skart arī citas proteoglikānus saturošas struktūras, piemēram, acis, kardiovaskulāro sistēmu, nieres.
Reta slimība, sastopamība - trīs uz miljonu iedzīvotāju.
Parasti izpaužas 40-60 gadu vecumā, bet var parādīties arī bērnībā.
Autoimūnā iekaisuma pamatā ar lielu varbūtību ir imunoloģiska reakcija pret dažiem skrimšļa antigēniem, kas nav precīzi identificēti.
Viens no iespējamajiem patoģenētiskajiem mehānismiem - ģenētiski predisponētiem indivīdiem autoreaktīvi T limfocīti aktivē autoimūnu reakciju pret kolagēna II tipu, matrillīnu 1 un skrimšļa oligomērisko matrices proteīnu (COMP), izraisot citokīnu izdali no iekaisuma šūnām, hondrocītu apoptozi, skrimšļa matrices un elastīgo šķiedru destrukciju, ko veic matrices metaloproteināzes (MMP).
Klīniskās izpausmes
Slimība var skart praktiski jebkuru orgānu. Izmaiņas parasti izraisa vaskulīts. Klīniski ap 80% gadījumu izpaužas ar ausu hondrītu un poliartrītu. Auss hondrīts - sāpēs, apsārtums, pietūkums ārējās auss struktūrās. Epizode var ilgt no dažām dienām līdz vairākām nedēļām (skat. 2. attēlu).
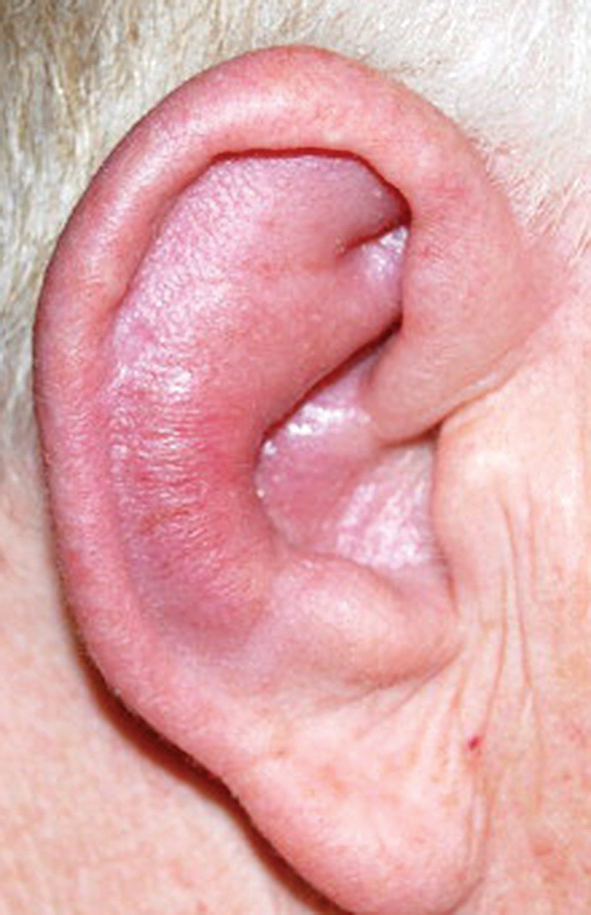

2. attēls
Auss hondrīts
Dzirdes traucējumus var radīt ārējās auss ejas slēgšanās, serozs otitis media. Iekaisums/vaskulīts vidusausī un iekšējās auss struktūrās var radīt sensoneirālu dzirdes zudumu, līdzsvara traucējumus, reiboni.
Elpceļu iesaiste ir saistīta ar visnopietnākajām slimības radītām komplikācijām. Bojājums parasti skar balseni un traheju. Iekaisums balsenes, trahejas vai bronhu skrimšļos rada balss aizsmakumu, neproduktīvu klepu, elpas trūkumu, sēkšanu, inspiratoru stridoru. Letālas respiratoras komplikācijas - infekcijas pievienošanās, trahejas kolapss - raksturīgas 10-50% gadījumu.
Nazāls hondrīts konstatēts vidēji pusei pacientu ar polihondrītu. Atkārtotas hondrīta epizodes var radīt sedlveida deguna deformāciju (skat. 3. attēlu).
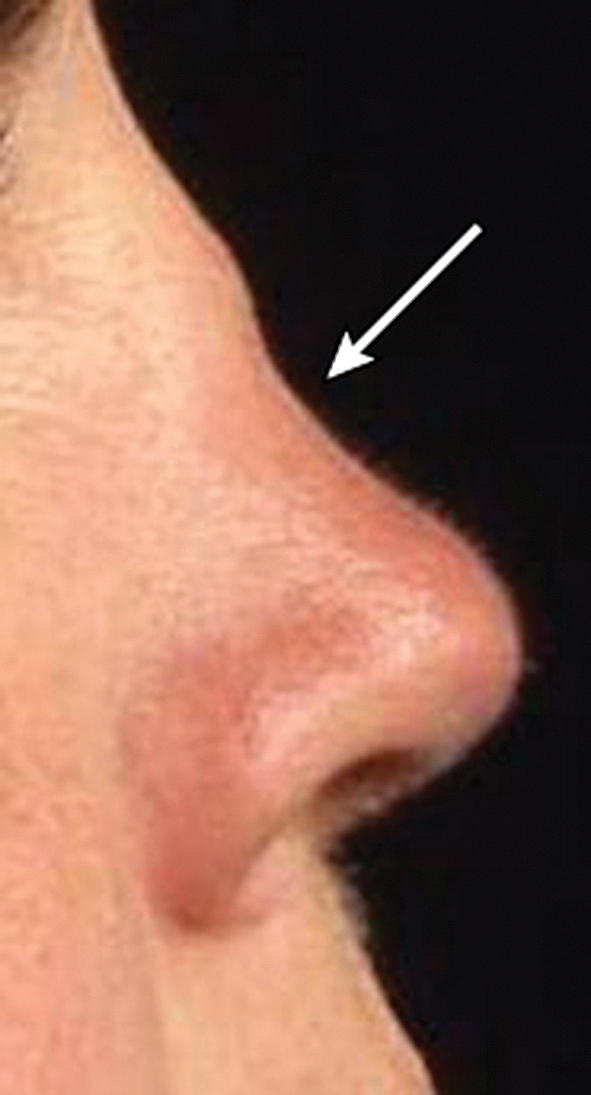

3. attēls
Sedlveida deguna deformācija
Acu bojājums (ap 60%) - episklerīts, sklerīts, retinopātija, optisks neirīts. Vaskulīts var skart arī ekstraokulāros muskuļus.
Retāk bojājums skar kardiovaskulāro sistēmu, nieres, nervu sistēmu.
Var būt dažādu asinsvadu (sīko, vidējo, lielo) vaskulīts.
Diagnostika
McAdam diagnostiskos kritērijus skat. 1. tabulā. Diagnozi apstiprina, ja ir vismaz trīs no sešiem diagnostiskajiem kritērijiem. Histoloģisks diagnozes apstiprinājums nepieciešams gadījumā, ja klīniskā aina nav nepārprotami skaidra. Klīniskā aina var būt ļoti mainīga, tāpēc diagnozes noteikšanai nepieciešami:
- vismaz trīs McAdam diagnostiskie kritēriji;
- viens vai divi klīniskie kritēriji un pozitīvs histoloģiskais slēdziens (biopsija no auss, deguna vai elpceļu skrimšļa);
- hondrīts, kas skar vismaz divas lokalizācijas, ar pozitīvu efektu, ja terapijā lieto glikokortikoīdus.


1. tabula
McAdam diagnostiskie kritēriji
Nav specifisku laboratorisko testu, kas apstiprinātu diagnozi:
- var būt paaugstināti iekaisuma rādītāji - EGĀ, CRO;
- normohroma normocitāra anēmija, leikocitoze, trombocitoze;
- antivielu pret II tipa kolagēnu noteikšana slimības akūtajā fāzē nav specifiska, antivielu titrs var korelēt ar slimības smagumu.
Agrīnu izmaiņu diagnostikai laringotraheālajā un bronhiālo skrimšļu zonā kā izvēles diagnostikas metode izmantojama DT. Magnētiskās rezonanses attēlveidošanas (MRA) izmeklējums ir nozīmīgākais recidivējošā polihondrīta diagnostikā, jo vizualizē agrīnas iekaisuma radītās izmaiņas perihondrijā un hondroepifiziāli. Pat gadījumā, kad slimība norit subklīniski, MRA fibrozi atšķir no iekaisuma (pretstatā DT) un iekaisumu no tūskas.
Terapijas pamatprincipi
Slimības retuma dēļ nav veikti klīniskie pētījumi par terapijas drošumu un efektivitāti. Ārstēšana pārsvarā empīriska vai pēc ziņām no dažiem aprakstītajiem klīniskajiem gadījumiem, kā arī atkarīga no slimības aktivitātes un smaguma.
Sistēmiska RP gadījumā kombinē pirmās un otrās izvēles medikamentus.
Sākotnēji glikokortikoīdu pulsterapija ar S. Solumedroli 500 mg × 1 i/v 3 dienas, tad per-orāla GK lietošana - prednizolons 1 mg/kg, devu pakāpeniski mazinot.
Slimības paasinājuma riska pakāpe ir augsta arī GK terapijas fonā, tāpēc uzturošajā terapijā jāpievieno bāzes medikaments; biežāk lietotie: ciklofosfamīds, azatiorīns, ciklosporīns.
Ciklofosfamīds (1-2 mg/kg) ir izvēles preparāts arī citu autoimūnu slimību (un arī nekrotizējošu vaskulītu) gadījumā. Parasti indukcijas terapija ilgst sešus mēnešus; pēc stāvokļa stabilizēšanās rekomendē pāriet uz azatioprīnu vai metotreksātu.
Kā alternatīva ciklofosfamīdam rekomendēts azatioprīns 2 mg/kg.
Bioloģiskie medikamenti RP terapijā
Par bioloģisko medikamentu izmantojumu RP terapijā publicēti vien atsevišķi klīniskie gadījumi. Ir dati par 62 pacientiem, kam ievadīti bioloģiskie medikamenti; skat. 2. tabulu.
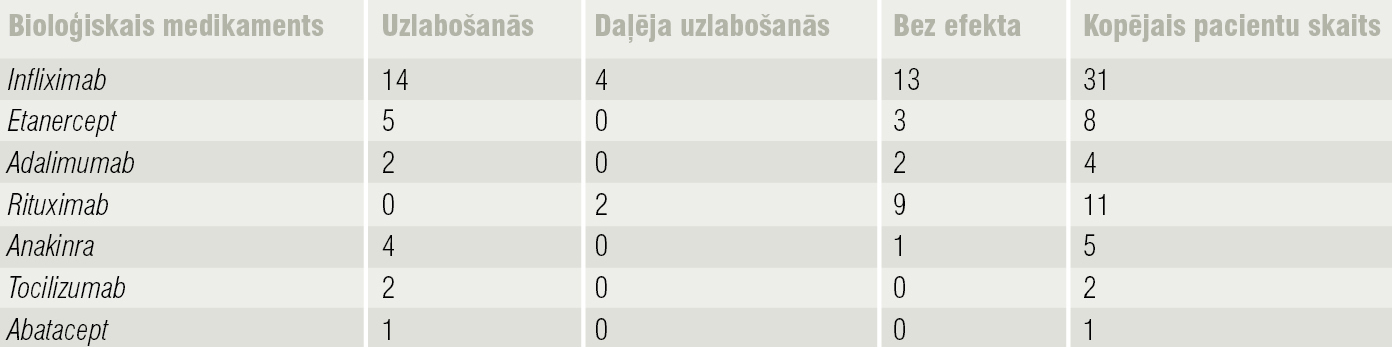

2. tabula
Bioloģiskie medikamenti
Nav vienotu uzskatu par bioloģisko medikamentu efektivitāti RP terapijā. Bioloģisko medikamentu darbības dažādie mehānismi dod cerību terapeitiskai efektivitātei potenciāli dzīvību apdraudošas slimības, kāda ir RP, ārstēšanā, ja līdzšinējā standarta terapija bijusi nesekmīga.
Papildu terapija
Laringotraheāls hondrīts var izraisīt izteiktu elpceļu sašaurināšanos, kas rada dinamisku elpceļu kolapsu forsētas ieelpas (balsenē) un izelpas laikā (trahejā). Augšējo elpceļu bojājuma gadījumā var būt nepieciešama traheostomija.
Apakšējo elpceļu segmentāla kolapsa gadījumā apsverama ķirurģiska rezekcija vai stenta implantācija.
Papildus apsverama arī neinvazīvās ventilācijas (BiPAP un CPAP) izmantošana, sevišķi naktī.
Vārstuļa protezēšana vai valvuloplastija - ja ir vārstuļu bojājums.