Pediatriskā populācijā vīrusa transmisija ir vertikāla, pamatā virzoties caur fizioloģiskajiem dzemdību ceļiem, [2] bet ap 12,5 % vīrusa transmisijas gadījumu notiek transplacentāri. [4] Riska faktori vīrusa transmisijai ir māte ar kondilomām grūtniecības laikā vai anamnēzē, prolongētas vaginālas dzemdības virs desmit stundām, mātes vecums zem 20 gadiem un pirmdzimtais bērns, [5] bet uzņēmību pret CPV infekciju ietekmē noteiktu gēnu alēliskie varianti vai gēnu iztrūkums un imūnās sistēmas defekti. [6]
Pieaugušo populācijā REP var izpausties kā vertikālas transmisijas ceļā iegūta vīrusa latentās formas aktivācija vai tieša kontakta ceļā iegūta infekcija. [2] Pēc transmisijas CPV inficē respiratorā trakta gļotādas bazālo slāni, vīrusam piemīt potenciāls integrēt savu DNS šūnas genomā un aktivēt epidermālā augšanas faktora receptora ceļu. [6]
ASV statistikas dati par 2023. gadu rāda, ka REP sastopamība pediatriskajā populācijā ir viens no 23 300, bet pieaugušo populācijā viens no 55 550. [1]
Lai gan izpausmes elpceļos parādās reti, CPV infekcija sastopama bieži, seksuāli aktīvās un pret CPV nevakcinētās populācijas iespējamība dzīves laikā inficēties ir virs 80 %. [7]
Distāla REP izplatība raksturīga 2—5 % gadījumu, bet plaušu iesaiste tikai 1 %, [8] tāpēc klīniskais gadījums atspoguļo retu slimības izpausmi. Turklāt slimības agresivitāte, norise un iznākums ļoti atšķiras, tādējādi apgrūtinot vienotu vadlīniju izstrādi, tāpēc katra REP gadījuma analīze ir nozīmīga. Līdzšinējos pētījumos aprakstītie sistēmiskās terapijas ar bevacizumabu rezultāti ir daļēja vai stabila remisija elpceļos 83,3 % gadījumu un plaušās 75 % gadījumu, [9] šajā gadījumā elpceļos novērotā terapijas efektivitāte atbilst literatūrā aprakstītajiem rezultātiem, bet plaušās — neatbilst.
Literatūras apraksts
Klīniskā aina
REP visbiežāk izpaužas ar klasisko triādi: progresīva disfonija ar balss piesmakumu, stridors un respirators distress, kas izpaužas ar elpas trūkumu, tahipnoju, elpošanas palīgmuskuļu iesaisti.
Retāk vērojams hronisks klepus, hemoptīze, rekurentas respiratoriskās infekcijas, augšanas aizture, disfāgija. [10]
Progresējušas slimības gadījumā iespējama arī afonija, pulmonāla hipertensija un plaušu sirds jeb sirds labā kambara paplašinājums → mazspēja. [11] Visbiežāk bērnībā sākušās REP klīniskās pazīmes sāk izpausties 2—6 gadu vecumā. [12]
Diagnostika
Rekomendētais REP diagnostikas algoritms ietver sākotnējo konsultāciju pie bērnu otorinolaringologa un fibrolaringoskopiju, kam seko apstiprinošā metode ar tiešo laringoskopiju un bronhoskopiju ar biopsijas materiāla iegūšanu, tālāku histoloģisku analīzi un vīrusa genotipēšanu ar PĶR. Nākamā kontroles tiešā laringoskopija un bronhoskopija veicama pēc klīniskām indikācijām, bez noteikta laika intervāla.
Ja aizdomas par plaušu iesaisti, veicama krūškurvja Rtg → datortomogrāfija un bērnu pneimonologa konsultācija. Augsta HIV un tuberkulozes infekcijas riska populācijās apsver specifiskos mikrobioloģiskos testus. Iespējamo cēloņu noskaidrošanai veicama ģenētiskā un imunoloģiskā izmeklēšana. [10]
Slimības aktivitātes izvērtēšanai rekomendē izmantot klīniskās un anatomiskās stadijas novērtējumu jeb Derkay score, kas sastāv no sešiem jautājumiem par papilomu radītajiem simptomiem un nepieciešamo ķirurģisko iejaukšanos biežumu, kā arī no elpceļu attēldiagnostikas izvērtējuma, nosakot papilomu izmēru katrā no 25 izdalītajām lokalizācijām, ietverot balseni, traheju, plaušas, degunu, rīkli un barības vadu. [13] Papildus tam iespējams izvērtēt arī balss invaliditātes indeksu (voice handicap index–10), kas sastāv no desmit jautājumiem par balss traucējumiem un to ietekmi uz dzīves kvalitāti. Abi šie rīki tieši korelē ar slimības aktivitāti. [14]
Ārstēšana
Mūsdienās primārā ārstēšanas metode ir ķirurģiska papilomu ekstirpācija, visbiežāk ar oglekļa dioksīda (CO₂) lāzeru, [15] bet konkrēts aprīkojums un personāla iemaņas ļauj izmantot arī cita veida lāzeru, piemēram, tūlija, kālija, titāna, fosfāta vai pulsētās krāsas, [16] konservatīvu rezekciju, radiofrekvences katetra ablāciju, [10] argona plazmas koagulāciju, [17] krioablāciju. [18] Ap 20 % gadījumu ķirurģiska ārstēšana jāpapildina ar lokālu vai sistēmisku terapiju. [19]
Lokālas terapijas medikaments tiek injicēts tieši papilomu skartajā rajonā, šim nolūkam izmanto pretvīrusu grupas medikamentu cidofovīru vai bioloģiskās mērķterapijas grupas, VEGF inhibitoru bevacizumabu. [19] Atsevišķos gadījumos aprakstīta fotodinamiskā terapija, kuras pamatā ir intravenoza fotosensibilizējoša aģenta ievade, kas trīs dienu laikā uzkrājas šūnās ar augstu proliferācijas ātrumu, kāds raksturīgs papilomu epitēlija šūnām. Tad papilomas tiek apstarotas ar sarkano gaismu, kas aktivē brīvo skābekļa radikāļu kaskādi un rada citotoksisku efektu uz šūnu, un skartās šūnas tiek destruētas. [20]
Sistēmiska jeb intravenoza papildu terapija apsverama, ja raksturīga ātra papilomu ataugšana ar negatīvu ietekmi uz elpceļiem, gadā nepieciešamas vairāk nekā četras ķirurģiskas iejaukšanās un novērota slimības distāla izplatība, īpaši ar plaušu iesaisti. [10] Agrāk visbiežāk to nodrošināja ar interferonu α2a, bet lielā blakusparādību sloga dēļ medikaments netiek rekomendēts kā pirmā izvēle. [15]
Mūsdienās biežāk tiek izmantots bevacizumabs, kam novērota gan augsta efektivitāte, jo papilomās pierādīta paaugstināta VEGF ekspresija, [21] gan mazs blakņu slogs, kas visbiežāk ir pašlimitējoša arteriāla hipertensija, proteinūrija vai kreatinīna līmeņa paaugstināšanās. [22] Atsevišķās iestādēs mainījusies REP ārstēšanas paradigma un sistēmiska terapija ar bevacizumabu kļuvusi par pirmās līnijas metodi iepretī ķirurģiskai papilomu ekstirpācijai. [23] Aprakstīta sistēmiska terapija arī ar pretvīrusu medikamentiem cidofovīru vai aciklovīru, ciklooksigenāzes–2 selektīvo inhibitoru celekoksibu, uztura bagātinātāju inodol–3–karbinolu, karstuma šoka proteīnu E7, [10] programmētās šūnu nāves proteīna–1 inhibitoru pembrolizumabu, [15] A vitamīna aktīvajiem metabolītiem un histamīna–2 receptoru antagonistu cimetidīnu. [8] Tomēr nevienam no šiem medikamentiem oficiālo indikāciju sarakstā šobrīd REP nav iekļauta.
Papildu ārstēšanas metode, kas rekomendēta visiem REP pacientiem, ir kvadrivalentā vai nonavalentā CPV vakcīna.
Atšķirību starp abām vakcīnām nenovēro, jo abas satur antigēnus pret 6. un 11. CPV tipu, kas ir īstās REP ierosinātāji. [24] No simptomātiskās terapijas metodēm aprakstīta traheostomija, kas veicama diseminētas slimības gadījumā ar nozīmīgu elpceļu obstrukciju, kā arī protonu sūkņu inhibitoru lietošana, ja aizdomas par gastroezofageālā refluksa slimību (GERS) vai ja pierādīta GERS, jo skābes reflukss paasina REP norisi un negatīvi ietekmē pēcoperācijas brūču dzīšanu. [10]
Klīniskais gadījums
Anamnēze
Paciente, piecus gadus veca, dzimusi laicīgās vaginālās dzemdībās. Ģimenes anamnēzē mātei ģenitāliju kondilomas sēžas rajonā vairākus gadus pirms grūtniecības, bet grūtniecības pēdējā mēnesī novērota diseminācija. Ķeizargrieziens netiek veikts, vecākiem tiek izskaidrots, ka vīrusa migrācijas risks uz elpceļiem ir pietiekami zems. Agrīnas augšanas un attīstības periodā būtiskas novirzes no normas nekonstatē.
Gada un mēneša vecumā paciente sāk apmeklēt bērnudārzu, parādās sūdzības par balss aizsmakumu, dzirdamu troksni elpošanas laikā, elpošanas grūtībām un klepu. Tiek stacionēta, izmeklēta un ārstēta kā akūta traheolaringīta pacients. Šāda epizode atkārtojas pēc trīs mēnešiem. Pēc epizodēm ilgstoši persistē balss piesmakums, sakarā ar to notiek konsultācijas ar vairākiem bērnu otorinolaringologiem, veikts alerģiju panelis, kas novirzes no normas neuzrāda. Divu gadu vecumā paciente tiek stacionēta BKUS balsenes izmeklēšanai ar tiešo laringoskopiju, tiek diagnosticēta balsenes papilomatoze.
Klīniskā aina
Pacientei novēro klasisko REP triādi ar persistējošu disfoniju, stridoru un respiratoru distresu. Epizodiski vēro arī afonijas lēkmes, rekurentas respiratoriskās infekcijas, kuras izpaužas ar ķermeņa temperatūras paaugstināšanos, sēkšanu, rinītu, produktīvu klepu, kas izsauc vemšanas epizodes.
Diagnostika un rezultāti
No 2020. gada decembra līdz 2024. gada februārim tiešā laringoskopija veikta 25 reizes, novēro bāli rozā ziedkāpostiem līdzīgus veidojumus balsenē un elpceļu stenozi. Pirmās procedūras laikā tiek iegūts biopsijas materiāls, veikta histoloģiska izmeklēšana, atrade apstiprina papilomatozes diagnozi — fibrovaskulāra serde, ko klāj daudzkārtains, plakans, pārragots epitēlijs, minimāla iekaisuma šūnu infiltrācija, šūnu atipiju nenovēro. Pēc trahejas iesaistes konstatēšanas kopš 2022. gada augusta tiešā laringoskopija papildināta ar lokano vai cieto bronhoskopiju. Pirmajiem trahejas veidojumiem atkārtoti veikta biopsija un histoloģiska izmeklēšana, kas apstiprina papilomatozi. Vīrusa genotipēšana netiek veikta.
Krūškurvja Rtg veikta 5 × aizdomu dēļ par sadzīvē iegūtu pneimoniju, bet tiek konstatēti bronhu drenāžas traucējumi bez pneimonijas ainas. Krūškurvja datortomogrāfiju bez kontrastvielas kopš 2022. gada augusta veic 5 ×, sākotnēji sakarā ar paasinājumu, bet tiek konstatēti veidojumi trahejā un plaušās, vēlāk novēro arī trahejas stenozi. Dinamikas kontrolē tiek novērota veidojumu augšana izmērā un skaitā:
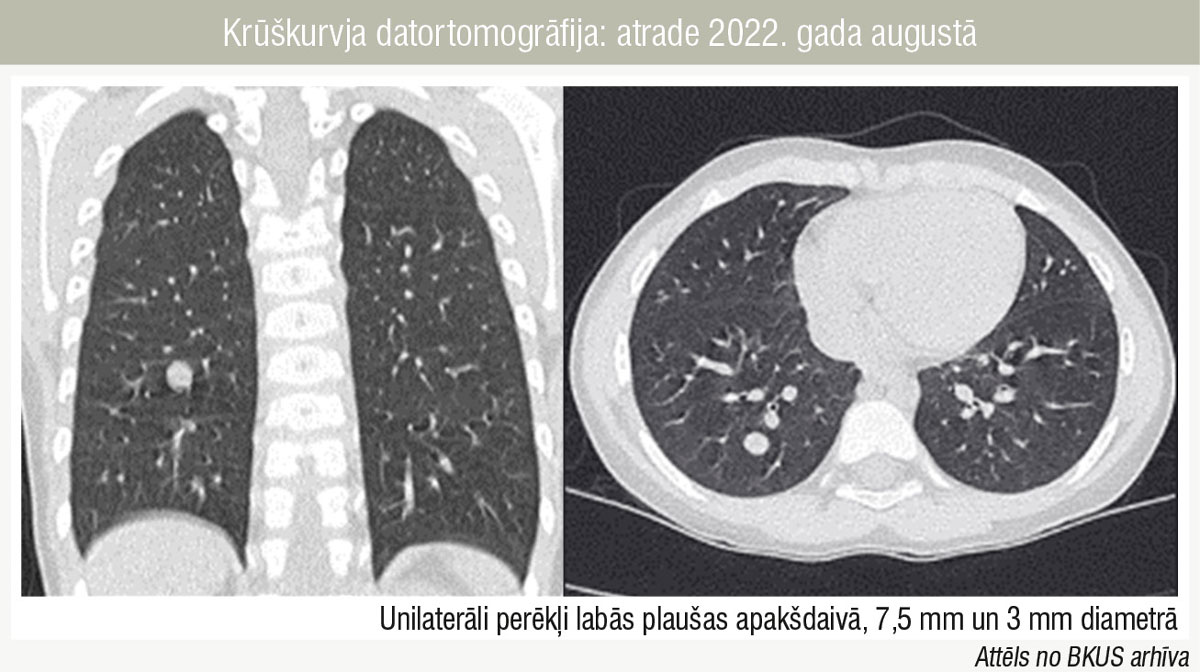
- 2022. gada augusts: labās plaušas apakšdaivā divi veidojumi, 3 mm un 7,5 mm diametrā,
- 2022. gada septembris: labās plaušas apakšdaivā divi veidojumi, 3,5 mm un 8 mm diametrā,
- 2023. gada februāris: labās plaušas apakšdaivā divi veidojumi, 5 mm un 9,3 mm diametrā, vidusdaivā 4 mm, augšdaivā 2,5 mm, kreisās plaušas apakšdaivā multipli sīki perēkļi līdz 3 mm,
- 2023. gada aprīlis: labās plaušas apakšdaivā divi veidojumi, 6 mm un 9,3 mm diametrā, vidusdaivā 4 mm, augšdaivā 2,5 mm, kreisās plaušas apakšdaivā multipli sīki perēkļi līdz 3 mm,
- 2024. gada janvāris: labās plaušas apakšdaivā multipli veidojumi, lielākais 14 mm diametrā ar kavitāciju, labās plaušas vidusdaivā un augšdaivā multipli perēkļi līdz 7 mm diametrā, kreisās plaušas augšdaivā līdz 5 mm diametrā un apakšdaivā līdz 10 mm diametrā ar kavitāciju, trahejas stenoze bez veidojumiem lūmenā.
Regulāri veikta laboratoriskā izmeklēšana, nozīmīgākās izmaiņas ir periodiska leikocitoze ar neitrofilozi, paaugstināts CRO, IL6 un kreatinīna līmenis, elektrolītu disbalanss, hipoksija arteriālo asiņu gāzēs. Atkārtoti veic trahejas un bronhu satura mikrobioloģisko uzsējumu ar antibiotiku jutības noteikšanu, visbiežāk izolētās baktērijas ir Ps. aeroginoza, Str. aureus un St. maltophillia, retāk alfa hemolītiskais Str. viridans, Str. pyogenes un H. influenza rezistents pret trimetoprimu/sulfametoksazolu.
Atkārtoti tiek veikta Covid–19 diagnostika un kontroles nolūkā arī tuberkulozes tests; infekcijas nekonstatē. Cēloņa noteikšanai veic ģenētisko un imunoloģisko testēšanu, novirzes no normas nekonstatē.
Ārstēšana
Pamata metode ir ķirurģiska papilomu ekstirpācija tiešās laringoskopijas un bronhoskopijas kontrolē, kas no 2020. gada decembra līdz 2024. gada februārim veikta 25 reizes, no kurām 23 reizes lieto CO₂ lāzeru, un 3 × argona plazmas koagulācija ar krioterapiju. Atšķirības starp metodēm nenovēro. Procedūras atkārto pēc klīniskām indikācijām paasinājumu gadījumā, kas liecina par masu ataugšanu. Pēc ekstirpācijas veic balsenes un trahejas balondilatāciju stenozes profilaksei.

Tabula
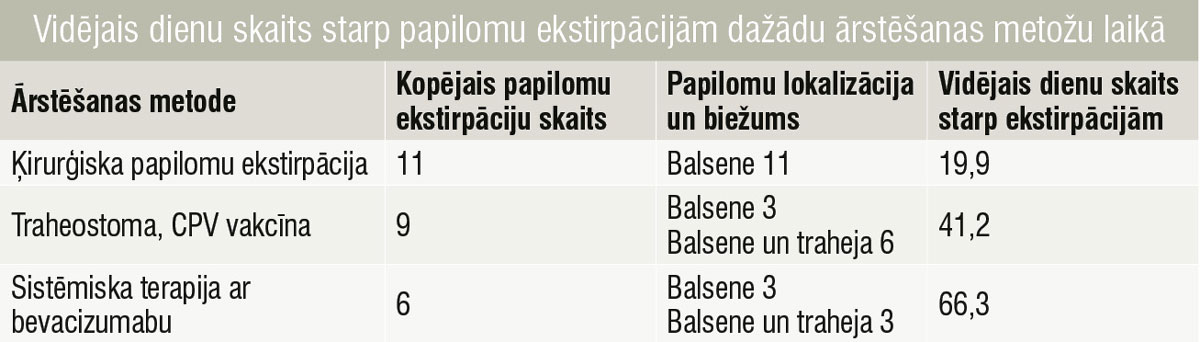
Vidējais dienu skaits starp papilomu ekstirpācijām dažādu ārstēšanas metožu laikā
No 2021. gada janvāra līdz jūlijam paciente saņem trīs devas nonavalentās CPV vakcīnas Gardasil–9. Pēc vakcīnas otrās devas novēro paasinājumu, kas izpaužas ar papilomas masu ataugšanas ātruma un apjoma pieaugumu, sakarā ar to 2021. gada maijā veic akūtu traheostomiju, bet jūnijā tiek ievietota pastāvīga traheostoma. 2023. gada oktobrī mēģina veikt traheostomas izņemšanu, bet, izmeklējot elpceļus, konstatē papilomatozes recidīvu, tāpēc izlemj to neveikt. Līdz kaniles izņemšanai paciente veic elpošanas vingrinājumus un izmanto traheostomas korķi nomoda laikā.

1. attēls
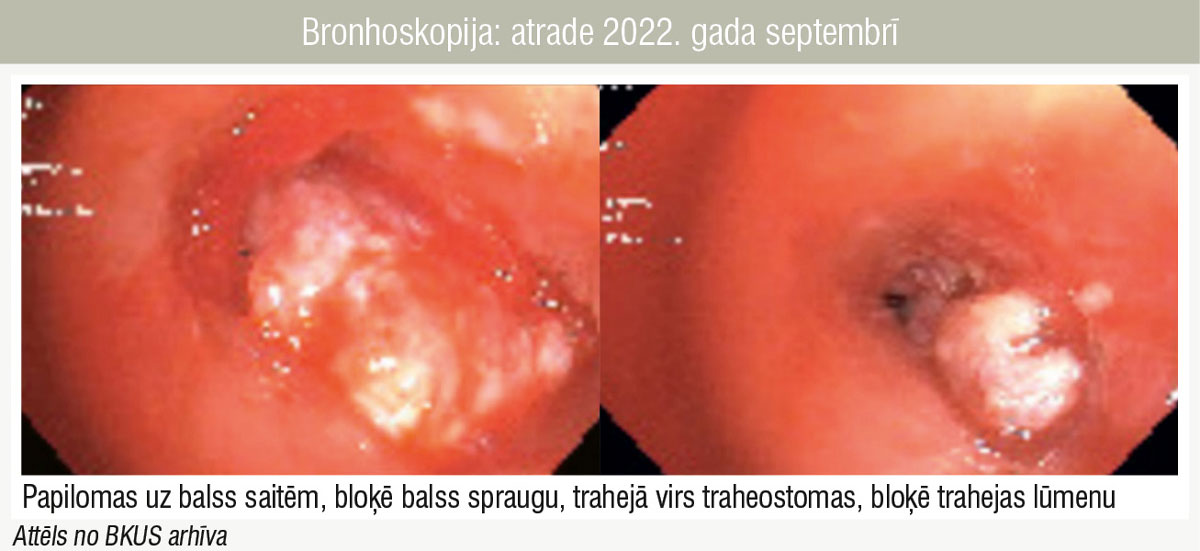
Bronhoskopija: atrade 2022. gada septembrī
Sakarā ar plaušu veidojumu straujo dinamiku 2023. gada februārī sāk terapiju ar bioloģisko preparātu bevacizumabu. Deva indukcijas fāzē 10 mg/kg jeb 190 mg ik trīs nedēļas 6 × un uzturošajā fāzē 10 mg/kg jeb 190 mg ik trīs mēnešus. Panāk īslaicīgu remisiju, bet 2023. gada oktobrī konstatē papilomas elpceļos un 2024. gada janvārī plaušu veidojumu pieaugumu skaitā un izmērā. Tiek organizēta saziņa ar speciālistiem no ASV, pēc kuru ieteikuma 2024. gada februārī sākts atkārtots un koriģēts ārstēšanas kurss ar bevacizumabu. Atkārtotās indukcijas fāzes laikā medikaments tiek ievadīts devā 10 mg/kg jeb 230 mg ik trīs nedēļas 8 × un uzturošās fāzes laikā paredzēts saņemt to pašu devu, bet medikamenta ievades biežumu samazināt pakāpeniski, sākumā ik sešas nedēļas 6—8 ×, tad ik astoņas nedēļas 6—8 × un ik 12 nedēļas 6—8 × vai līdz brīdim, kad sasniegta stabila remisija.

2. attēls
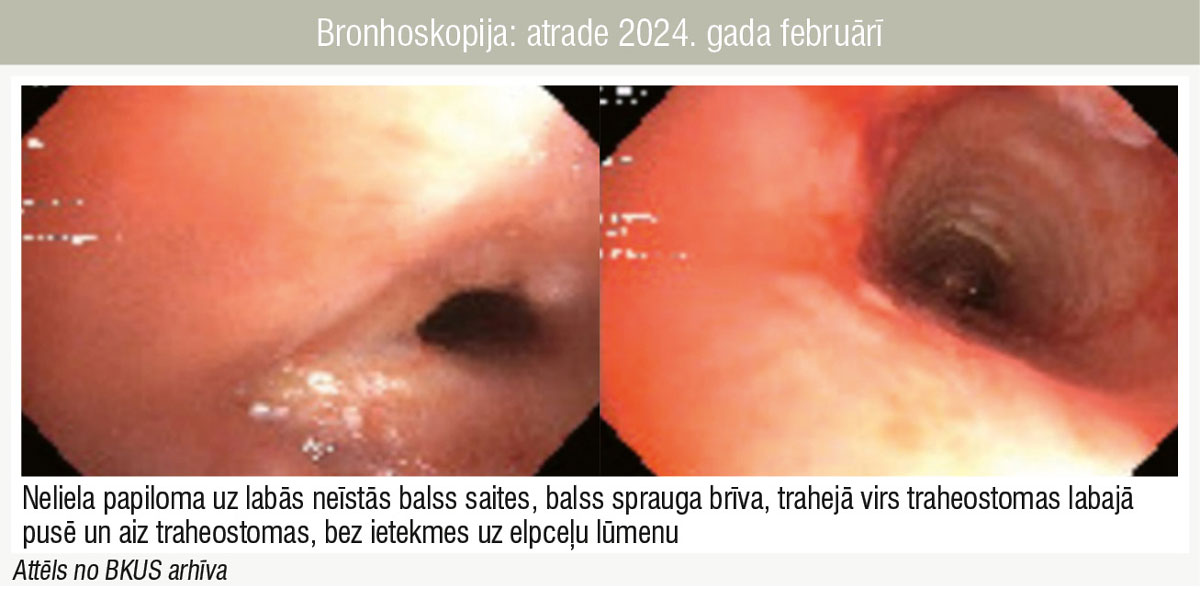
Bronhoskopija: atrade 2024. gada februārī
Paralēli REP ārstēšanas metodēm veikta plaša simptomātiska ārstēšana:
- sāpes traheostomas rajonā — metamizols, ibuprofēns,
- paaugstināta ķermeņa temperatūra — paracetamols,
- elektrolītu disbalanss — intravenozs sāļu—elektrolītu šķīdums, orālās rehidratācijas līdzeklis,
- gastroezofageālā atviļņa simptomi — omeprazols,
- respiratorā distresa simptomi — salbutamola, ipratropija un budezonīda inhalācijas, metilprednizolons intravenozi,
- rinīta simptomi — mometazona aerosols, klemastīns intravenozi,
- akūta bakteriāla respiratoriska infekcija — amoksiklāvs, ciprofloksacīns, azitromicīns.

3. attēls
Krūškurvja datortomogrāfija: atrade 2022. gada augustā
Rezultāti un secinājumi
Elpceļu drenāžas traucējuma un traheostomas kā svešķermeņa dēļ novēro elpceļu kolonizāciju ar vairāku sugu baktērijām. Profilaktiska antibakteriālā terapija izskaušanai netiek lietota, bet regulāri tiek veikta traheostomas kopšana un kaniles maiņa. Atkārtotu ķirurģisku iejaukšanos dēļ vēro trahejas stenozi, ko paredzēts koriģēt ar balondilatāciju. Ja tas izdosies veiksmīgi, šis gadījums var palīdzēt ieviest jaunu virzienu agrīnas stenozes ārstēšanā, jo līdz šim aprakstīta tikai rekonstruktīvā ķirurģija REP pacientiem ar elpceļu stenozi. Nepieciešama tālāka pētniecība šajā jomā. Paasinājums pēc 2. vakcīnas devas nav aprakstīts nevienā citā gadījumā un nav iespējams pierādīt, vai šajā gadījumā tas norit kā komplikācija vakcīnai, tāpēc drošus secinājumus izteikt nevar.
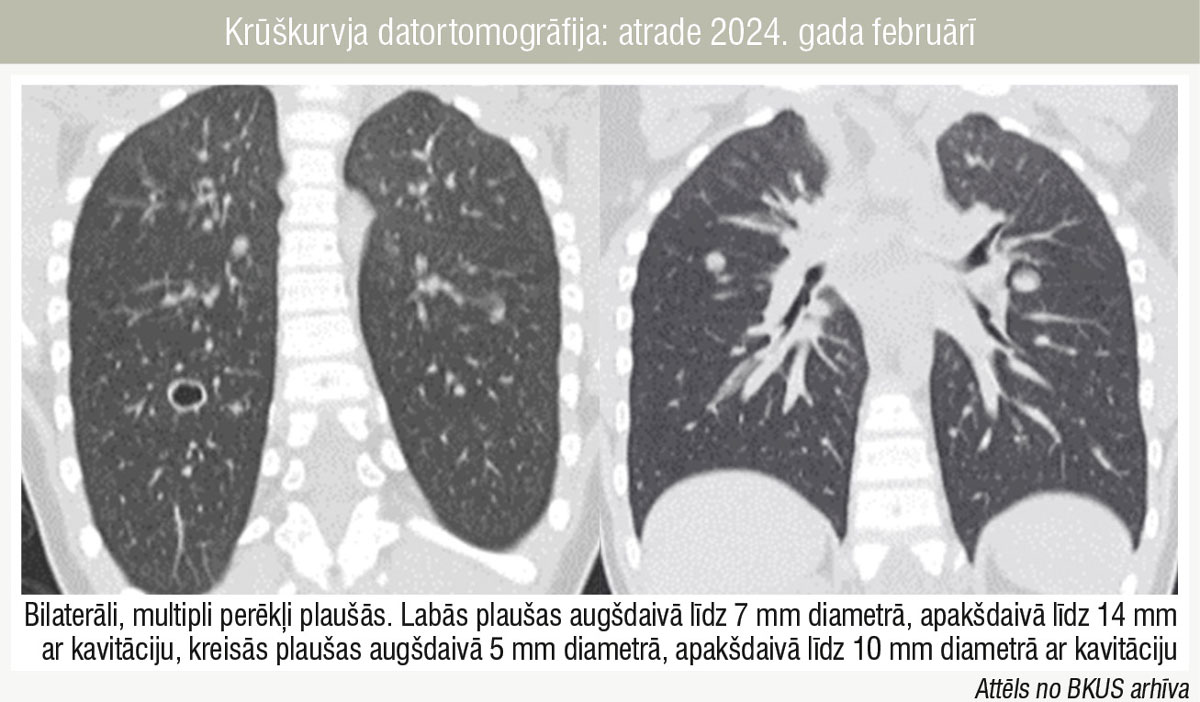

4. attēls
Krūškurvja datortomogrāfija: atrade 2024. gada februārī
Iespējams salīdzināt terapijas efektivitāti dažādos ārstēšanas posmos, izmantojot vidējo laika intervālu starp ekstirpācijas procedūrām. Ķirurģijas monoterapijas laikā tas ir 19,9 dienas, pēc traheostomas un CPV vakcinācijas tas ir 41,2 dienas un pēc sistēmiskas terapijas sākšanas ar bevacizumabu — 66,3 dienas (tabula).
Elpceļu endoskopiskā aina pirms bevacizumaba lietošanas 2022. gada septembrī atspoguļo lielas eksofītas masas, kas veido konglomerātus (1. attēls), bet pēc terapijas 2024. gada februārī masas ir plakanas un solitāras (2. attēls). Šie rezultāti liecina, ka sistēmiska terapija ar bevacizumabu visefektīvāk samazina papilomas masu ataugšanas ātrumu un izmēru elpceļos. Pretstatā elpceļiem plaušās vēro izteikti negatīvu dinamiku. 2022. gada augustā perēkļi atrodami tikai labās plaušas apakšdaivā (3. attēls), bet 2024. gada janvārī perēkļi plaušās ir bilaterāli, palielināti gan skaitā, gan izmērā un lielākajiem vēro arī kavitāciju (4. attēls). Visticamākais iemesls nepilnvērtīgai atbildreakcijai uz bevacizumabu ir straujā medikamenta ievades intervāla pagarināšana uzturošajā fāzē, kas atkārtotā kursa laikā tiks koriģēta, nepieciešama pētniecības turpināšana teorijas apstiprināšanai.
Kopumā ķirurģiska REP ārstēšana sniedz tūlītēju, bet īslaicīgu efektu. Papildu terapijas pievienošana paildzina papilomu ataugšanas laiku, samazina ataugušo masu izmēru. Veidojumi plaušās prasa ilgstošāku un intensīvāku bevacizumaba kursu, lai sasniegtu slimības remisiju.