Pirmā daļa rakstam bija par sievietes aprūpi pēc dzemdībām, kur autores izklāsta gan fizioloģiskās izmaiņas, kas sagaida sievieti, gan aprūpes principus stacionārā. Šajā raksta daļā sniegts apkopojums par sāpju pārvaldību un izrakstīšanos no stacionāra.
Sāpes pēcdzemdību periodā un to mazināšana
Atsāpes pēcdzemdību periodā ir 50 % sieviešu, parasti pirmajās 48 stundās pēc vaginālām dzemdībām vai ķeizargrieziena operācijas. [22] Sāpes ir intermitējošas un intensīvākas zīdīšanas laikā oksitocīna izdalīšanās dēļ.
Atsāpes biežāk novēro multiparām sievietēm vai sievietēm ar ievērojamu dzemdes iestiepumu pirms dzemdībām, dvīņu grūtniecību, polihidramniju un sievietēm ar dismenoreju anamnēzē. Atsāpes spontāni izzūd pirmās pēcdzemdību nedēļas laikā. Efektīvi ir vieglie pretsāpju līdzekļi (acetaminofēns, ibuprofēns, diklofenaka svecītes). [23] Nesteroīdie pretiekaisuma līdzekļi (NSPL) ir tikpat efektīvi kā acetaminofēns (paracetamols). Ja vienas zāles nav bijušas pietiekami efektīvas, var lietot abu zāļu kombināciju.
Opioīdi atsāpju mazināšanai nav nepieciešami. Izteiktas atsāpes pēc vaginālām dzemdībām ir netipisks gadījums, kam jāmeklē cits iemesls.
NSPL vai acetaminofēns ir ieteicamie sākotnējie pretsāpju līdzekļi pēc vaginālām dzemdībām. Opioīdu lietošana pēc vaginālām dzemdībām palielina risku pastāvīgai nevajadzīgai opioīdu lietošanai nākotnē pat pēc sūdzību izzušanas. [24] Pētījumi liecina, ka sievietēm pēc vaginālām dzemdībām atkarība no opioīdu lietošanas var attīstīties 0,59—1,7 % gadījumu. Vienmēr jāatceras par pretsāpju zāļu devu un medikamentu kāpināšanas kāpnēm, sākot ar viegliem pretsāpju līdzekļiem un tikai nobeigumā pievienojot opioīdus.
Sāpju mazināšanai starpenē kā pirmās izvēles terapija lietojami viegli perorālie pretsāpju līdzekļi un lokāla konservatīva ārstēšana (piemēram, aukstas vai siltas aplikācijas 10—20 minūtes); dažām pacientēm labi palīdz lokālie anestēzijas līdzekļi. Jāizvairās no opioīdu lietošanas, lai gan nelielai daļai sieviešu tie īslaicīgi nepieciešami, lai ārstētu mērenas sāpes.
Pēcoperācijas analgēzija pēc ķeizargrieziena ietver multimodālu pieeju sāpju kontrolei, lai paciente ātrāk atveseļotos, lai viņai būtu vieglāk rūpēties par jaundzimušo un lai mazinātu vajadzību pēc operācijas lietot opioīdus. [25] Pretsāpju zāļu lietošanā jāizmanto kāpinoša pieeja, līdzekļi ar dažādiem darbības mehānismiem. Pacientes pieredzi pēc ķeizargrieziena ietekmē vairāki faktori, un viens no apmierinātības rādītājiem ir adekvāta atsāpināšana. Pētījuma dati liecina, ka opioīdu īslaicīga lietošana akūtu sāpju mazināšanai saistīta ar palielinātu opioīdu atkarības risku nākotnē 0,33—2,2 % gadījumu. [26]
Lielākā daļa pretsāpju līdzekļu ir droši mātēm, kuras baro ar krūti. Sīkāku informāciju par zālēm var atrast UpToDate zāļu informācijas datubāzē, ZVA zāļu aprakstos LactMed datubāzē. Ieteicamās zāles:
- acetaminofēns — nonāk mātes pienā, bet Zīdīšanas medicīnas akadēmija (ABM) uzskata, ka tas ir piemērots pretsāpju līdzeklis sievietēm, kas bērnu baro ar krūti; [27]
- NSPL — ibuprofēna un diklofenaka rektālas svecītes, kurām ir īss eliminācijas periods (< 6 h), ir drošas zīdīšanas periodā. Jāizvairās no naproksēna lietošanas, jo ir alternatīvi NSPL, un tam ir ilgs pussabrukšanas periods (> 6 h), tātad lielāka iespēja uzkrāties zīdaiņa plazmā. To jaundzimušo mātes, kuriem ir no arteriālā vada atkarīga sirdskaite, barošanas ar krūti periodā nedrīkst lietot nevienu NSPL; [28]
- intravenozi vai perorāli ketorolaku var lietot kopā ar acetaminofēnu vai ibuprofēnu, lai ārstētu mērenas sāpes sievietēm, kas zīdaini baro ar krūti. Aktīvās vielas koncentrācija mātes pienā ir minimāla. Ketorolaka un acetaminofēna vai ibuprofēna kombinācija var nodrošināt mērenu analgēziju, lai izvairītos no opioīdu lietošanas;
- adekvāta mātes atsāpināšana ir svarīgs faktors zīdīšanas procesā, tomēr opioīdu lietošana pēcdzemdību periodā var ietekmēt jaundzimušā modrību un zīšanas aktivitāti. [29] Aprūpes speciālistam, izrakstot šos medikamentus, jāņem vērā ieguvumi un riski, jaundzimušā toksicitātes pazīmes (piemēram, samazināts muskuļu tonuss, slikta zīšana, grūtības pamodināt). Jebkura opioīda lietošana jāierobežo līdz mazākajai efektīvajai devai un jānozīmē īslaicīgai akūtu sāpju ārstēšanai. Opioīdu lietošanu var samazināt, izmantojot multimodālo pieeju sāpju kontrolēšanai un reģionālo anestēziju, piemēram, transversus abdominis vai quadratus lumborum plaknes blokādi. Amerikas Pediatrijas akadēmijas medikamentu komiteja priekšroku dod butorfanola, morfīna vai hidromorfona lietošanai nekā citiem opiātiem. [30]
Zīdīšanas periodā rekomendē izvairīties no kodeīna un tramadola lietošanas, jo ir dažādi citohroma CYP2D6 ģenētiskie varianti, kas var dažādi ietekmēt zāļu metabolismu organismā.
Rezultātā asins plazmā var uzkrāties augsts metabolītu līmenis, kas vēlāk nonāk mātes pienā, un izraisīt pārmērīgu zīdaiņa sedāciju. Šīs mutācijas biežumu nosaka etniskā piederība, kopējais biežums ASV populācijā ir 4—5 %. Pētījuma dati liecina, ka kodeīna lietošana zīdīšanas periodā zīdaiņa CNS nomāc pēc četrām dienām, iespējams, morfīna uzkrāšanās dēļ kodeīna metabolisma rezultātā, tāpēc kodeīnu nevajadzētu lietot ilgāk par četrām dienām.
Meperidīna lietošana barojošām mātēm nav rekomendēta, jo saņemti ziņojumi par no devas atkarīgu jaundzimušo CNS nomākumu, tā metabolītiem ir ilgs pussabrukšanas periods un akumulācijas risks. Aspirīns piesardzīgi jālieto sievietēm, kuras baro ar krūti, teorētiska Reja sindroma attīstīšanās riska dēļ. Lai gan Reja sindroms biežāk saistīts ar aspirīna lietošanu zīdaiņiem virālu infekciju gadījumā, taču metabolīta — salicilāta koncentrācija mātes pienā skaidri nav zināma.
Mazas aspirīna devas (75—325 mg dienā) saistītas ar zemu salicilātu līmeni serumā, tātad tas neizdalās mātes pienā, un teorētiski to var lietot laktācijas periodā sievietēm, kam nepieciešama antiagregantu terapija, tomēr Nacionālā Reja sindroma asociācija neiesaka aspirīnu lietot mātēm, kas bērnu baro ar krūti.
Lai gan zināms, ka NSPL izraisa asinsspiediena paaugstināšanos hipertensīvām sievietēm, pieejamie dati neliecina par negatīvu ietekmi hipertensīvām sievietēm pēcdzemdību periodā. Amerikas Dzemdību speciālistu un ginekologu kolēģija (ACOG) iesaka apsvērt NSPL kā pirmās izvēles līdzekļus pēcdzemdību sāpju mazināšanai visām sievietēm. [31]
Izrakstīšanās no stacionāra
ACOG iesaka grūtniecēm prenatālajā periodā izstrādāt pēcdzemdību aprūpes plānu un nepieciešamības gadījumā šo plānu pēc dzemdībām atjaunināt. Pacientes pēc vaginālām dzemdībām parasti tiek izrakstītas trešajā dienā, pēc ķeizargrieziena — ceturtajā dienā, ja pēcdzemdību periods norit fizioloģiski. [32] PVO ekspertu grupa piekrita lielākajai daļai publicēto vadlīniju, kas nosaka, ka māte un vesels, iznēsāts jaundzimušais pēc dzemdībām kvalificētiem medicīnas darbiniekiem ir jāuzrauga 24—48 stundas pēc dzimšanas.
Epidemioloģiskie dati rāda, ka pirmās 24—48 stundas pēc dzemdībām ir viskritiskākais laiks sievietei un jaundzimušajam, tāpēc aprūpe stacionārā var būt dzīvību glābjoša. ACOG iesaka: ja pacienti no stacionāra izraksta 48 stundas pēc vaginālām dzemdībām vai 72 stundas pēc ķeizargrieziena operācijas (izņemot dzemdību dienu), ir jāievēro noteikti kritēriji: stabili mātes vitālie rādītāji, apmierinoši izdalījumi no dzimumceļiem jeb lohijas, blīva dzemde, adekvāta urīna izdale, adekvāta sāpju kontrole, spēja staigāt un rūpēties par sevi un jaundzimušo, nav infekcijas pazīmju, nav traucēta brūču dzīšana, nav norādījumu par garīgi emocionālu nestabilitāti.
Pirms izrakstīšanās Rh negatīvai pacientei jāsaņem anti–D imūnglobulīns pēc nepieciešamības. Sievietei jāsniedz rekomendācijas par pēcdzemdību vingrojumiem un atbalsta iespēju resursiem.
Jāpārrunā brīdinājuma simptomi par nopietnām pēcdzemdību komplikācijām gan mātei, gan jaundzimušajam, jāsniedz informācija, kā sazināties ar veselības aprūpes sniedzēju vai kur meklēt medicīnisko palīdzību.
Sarkanā karoga simptomi
Paciente pirms izrakstīšanas jāizglīto par paredzamajām fizioloģiskajām pēcdzemdību pārmaiņām un par personīgo (krūšu, starpenes) un jaundzimušā aprūpi. Aprūpes speciālistam jāinformē par iespējamu komplikāciju pazīmēm, kad sievietei būtu nepieciešams meklēt medicīnisko palīdzību, un tās ir:
- stipra pēcdzemdību asiņošana (piemēram, ar svaigām asinīm pilnas pirmās divas dienas paketes stundas laikā),
- paaugstināta ķermeņa temperatūra virs 37,5 °C, mērot elkoņa locītavas ielokā,
- jaunas vai stiprākas sāpes starpenē vai dzemdē,
- dizūrija,
- krūšu problēmas: apsārtums, strutaini izdalījumi, sablīvējums, paaugstināta ķermeņa temperatūra; šīs problēmas var atrisināt ambulatori ginekologs vai ģimenes ārsts,
- aizdusa, sāpes krūtīs, sāpes kājās vai pietūkums,
- nozīmīgi garastāvokļa traucējumi (kas ietekmē attiecības vai ikdienas aktivitāti),
- stipras sāpes jebkurā vietā (piemēram, galvā, krūtīs, vēderā).
Uzturs un fiziskās aktivitātes
Uztura bagātinātāju papildu lietošanai pēcdzemdību periodā ir maz zinātnisko pierādījumu, ja sieviete ēd veselīgi, nav specifisku uztura produktu trūkuma (gaļa, piena produkti, dārzeņi u.c.) vai anēmijas. Sievietes pēc savas vēlmes var 6—8 nedēļas pēc dzemdībām turpināt pirmsdzemdību vitamīnu un/vai papildu dzelzs kursu.
Dzelzs preparāti papildus jālieto sievietēm ar anēmiju. Ja anēmiju izraisījušas fizioloģiskas pārmaiņas vai asins zudums bez dzelzs deficīta, tad ar lielāko ticamību tā pēc dažām nedēļām izzudīs. Ja pēc dzemdībām Hb līmenis < 100 g/l, vēl trīs mēnešus perorāli jālieto 100—200 mg dzelzs dienā.
Pacientei rekomendē sākt nelielas fiziskās aktivitātes iespēju robežās pēc dzemdībām: 0.—2. nedēļā vēlami iegurņa pamatnes muskuļu spēka un izturības uzlabošanas vingrinājumi (Kēgela vingrinājumi), smagumu celšana jāierobežo līdz 3—5 kg, vēlams veikt vienkāršus vingrinājumus rumpja muskulatūrai (sākotnēji guļus stāvoklī), labākais no kardiovaskulāriem treniņiem — iešana.
Slodzi 2.—4. nedēļā pakāpeniski palielina, veicot iegurņa pamatnes un rumpja vingrojumus, palielina arī noieto attālumu un ātrumu. [33]
4.—6. nedēļā kardiovaskulārs treniņš, kas neietver aktivitātes ar triecienu, piemēram, velotrenažieris vai eliptiskais trenažieris, ņemot vērā atjaunošanās perioda gaitu, dzemdību veidu, starpenes bojājumu, kā arī to, vai ir komfortabli sēdēt uz sēdekļa.
6.—8. nedēļā rētu mobilizācija, ātrsoļošana, var palielināt intensitāti un ilgumu kardiovaskulārajam treniņam, kas neiekļauj trieciena elementus (velotrenažieris, eliptiskais trenažieris, spēka vingrojums “vilkme” — svara pacelšana no grīdas), vingrojumu sākšana ar pretestību kājām un rumpim. 8.—12. nedēļā sāk peldēšanu, ja vien beigušies pēcdzemdību izdalījumi un rēta dzīst apmierinoši, nodarbības uz velotrenažiera, ja vien sēdēt uz trenažiera ir komfortabli.
Pēc 12. nedēļas — pakāpeniski atsāk skriet, apsver personīgā trenera piesaisti, izvērtē riska faktorus, piemēram, aptaukošanos, bet aktivitātes pielāgo pazīmēm un simptomiem.
Saprātīga pieeja ir ieteikt mātei atsākt mājasdarbus, vingrošanu un dzimumattiecības, kad viņai ir ērti veikt šīs darbības, un sievietei jāizvairās no darbībām, kas izraisa sāpes vai pārmērīgu nogurumu. Pēc vairākām nedēļām vēdera priekšējā siena atgūst lielāko daļu muskuļu tonusa. Vēdera vingrinājumu programmu var sākt jebkurā laikā pēc vaginālām dzemdībām, ja sieviete to vēlas. Vingrojumi var novērst muskuļu diastāzi, taču nav noteikts, cik lielā mērā vingrinājumi vai citi pasākumi atrisina vai paātrina diastāzes izzušanu.
Dzimumdzīvi var atsākt jau divas nedēļas pēc dzemdībām, ja vien starpene ir sadzijusi, ir pieejama kontracepcija un paciente ir gatava, tomēr lielākā daļa nebūs gatava dzimumattiecības atsākt noguruma, vāja libido dēļ, sāpju, maksts sausuma vai izdalījumu dēļ, reliģisku apsvērumu dēļ, psiholoģisku faktoru, pēcdzemdību skumju vai depresijas dēļ. Lielākā daļa sieviešu seksuālās attiecības atsāk 5—6 nedēļas pēc dzemdībām, kad parasti nozīmēta arī vizīte pie ginekologa. Pēcdzemdību konsultācijas par kontracepciju uzlabo līdzestību medikamentu lietošanai un samazina neplānotu grūtniecību skaitu.
Kontracepcija
Sievietēm, kas bērnu baro gan ar krūti, gan ar piemaisījumiem, ovulācija var notikt jau 25 dienas pēc dzemdībām, tāpēc kontracepcija jāsāk ne vēlāk kā trešajā pēcdzemdību nedēļā. Savukārt sievietēm, kas bērnu baro tikai ar krūti, ovulācija atgriežas vēlāk un ir mazāk paredzama.
Pirmajos sešos mēnešos pēc dzemdībām mātēm, kas bērnu baro tikai ar krūti, grūtniecības risks ir < 5 %, ja sieviete nelieto papildu uztura bagātinātājus, saglabājas amenoreja un samazina zīdīšanas pārtraukumus dienas un nakts laikā, bet pēc sešiem mēnešiem grūtniecības risks palielinās, tāpēc jāsāk izmantot kontracepcija.
Kontracepcijas sākšanas laiks agrīnā pēcdzemdību periodā atkarīgs no metodes, jo dažas hormonālās metodes var ietekmēt laktāciju, piemēram, jāizvairās no estrogēna—progestīna kontracepcijas līdzekļiem sievietēm, kas baro ar krūti un kam ir mazāk nekā 30 dienas pēc dzemdībām.
Intrauterīnās kontracepcijas ievietošana pirmajās desmit minūtēs pēc placentas atdalīšanās ir efektīva, ilgstošas darbības un laba alternatīva sterilizācijai. Ierīci var ievietot pēc vaginālām dzemdībām vai ķeizargrieziena operācijas, tomēr ir lielāks intrauterīnās spirāles ekspulsijas biežums nekā tad, ja to ievieto sešas nedēļas pēc dzemdībām. Olvadu nosiešanu jeb sterilizāciju var veikt 24 stundu laikā pēc dzemdībām vai ķeizargrieziena operācijas laikā.
Pēcdzemdību vizīte
Agrīna pēcdzemdību vizīte 1—2 nedēļas pēc dzemdībām jāapsver sievietēm ar ķeizargriezienu, hroniskam slimībām, kam nepieciešama cieša uzraudzība, un sievietēm, kurām ir pēcdzemdību depresijas risks (piemēram, depresijas epizodes, garastāvokļa traucējumi ģimenes anamnēzē).
Tradicionāli pēcdzemdību vizīte tika ieteikta 4—6 nedēļas pēc dzemdībām. 2018. gadā ACOG ieteica sievietēm pirmajās trīs pēcdzemdību nedēļās personīgi vai pa tālruni sazināties ar aprūpes sniedzēju, lai risinātu akūtas sūdzības, vajadzības gadījumā nodrošinot nepārtrauktu aprūpi un nākamo vizīti ne vēlāk kā 12 nedēļas pēc dzemdībām.
PVO iesaka pēcdzemdību novērtēšanu trešajā dienā pēc dzemdībām, 1.—2. nedēļā un 6. nedēļā. Sievietes ar hipertensīvām slimībām grūtniecības laikā jāinformē par hipertensijas komplikāciju pazīmēm un simptomiem, asinsspiediena kontroli pirmajās divās nedēļās pēc izrakstīšanās. Nepieciešamības gadījumā terapijas kontrole pie ģimenes ārsta vai ginekologa.
Ministru kabineta noteikumi Nr. 611 paredz, ka dzemdību palīdzību nedēļniecei (42 kalendārās dienas pēc dzemdībām) sniedz viena no ārstniecības personām: ginekologs (dzemdību speciālists) vai vecmāte. Ārstniecības personai (ginekologam, vecmātei) pēcdzemdību vizītes laikā jāspēj novērtēt pacientes pielāgošanās spējas jaunajam dzīves posmam ar zīdaini un jāatjauno pacientes slimību vēsture.
Apmeklējuma laikā jāuzklausa pacientes sūdzības, jānovērtē pacientes psihoemocionālais stāvoklis, jāpārrunā kontracepcijas plāns, atgriešanās pie dzimumdzīves, jāuzklausa sūdzības saistībā ar zīdīšanu, jāpārrunā jautājumi par atpūtu un aktivitātēm pēcdzemdību periodā, personīgo higiēnu, uzturu, zīdīšanu un jaundzimušā ēdināšanu, drošības pasākumiem, kas jāievēro, lai netiktu apdraudēta jaundzimušā veselība un dzīvība. Objektīvi novērtē sievietes vitālos rādītājus, vairogdziedzeri, krūtis (plaisas, jutīgumu, sablīvējumus, ādas izmaiņas), vēdera priekšējo sienu (diastāze, trūces), ārējos dzimumorgānus/starpeni (brūču dzīšana, fistulas), maksti, dzemdes kaklu, dzemdi ar piedēkļiem (izmērs, jutīgums, palpatori veidojumi) un ekstremitātes.
Optimālais laiks nākamajai grūtniecībai ir pēc 18—59 mēnešiem, tomēr šis starplaiks var nebūt labākais risinājums sievietēm, kas vecākas par 35 gadiem, vai tām, kuru ģimenes anamnēzē ir agrīna menopauze.
Skrīningi
Garīgās veselības traucējumi, pašnāvības, slepkavības un narkotisko vielu lietošanas traucējumi ir galvenie mātes mirstības cēloņi ASV. Visām sievietēm ir jāveic pēcdzemdību depresijas skrīnings pēc ACOG rekomendācijām. Edinburgas pēcdzemdību depresijas anketa ir oficiāli pieņemta un apstiprināta anketa, ko visbiežāk izmanto grūtnieču un sieviešu pēc dzemdībām depresijas skrīningam. Pēcdzemdību depresija nebūt nav reta parādība, tāpēc kombinācija “skrīnings un atbalsta sniegšana” uzlabo klīniskos rezultātus un ārstēšanu (īpaši ar biheiviorālo terapiju).
Ginekologam, ģimenes ārstam vai vecmātei jāveic smēķēšanas, alkohola, narkotisko vielu lietošanas skrīnings ar standartizētiem rīkiem, piemēram, NIDA ātrais tests (National institute on drug abuse quick screen), lai izvērtētu nepieciešamību pacienti nosūtīt pie narkologa (tabula).
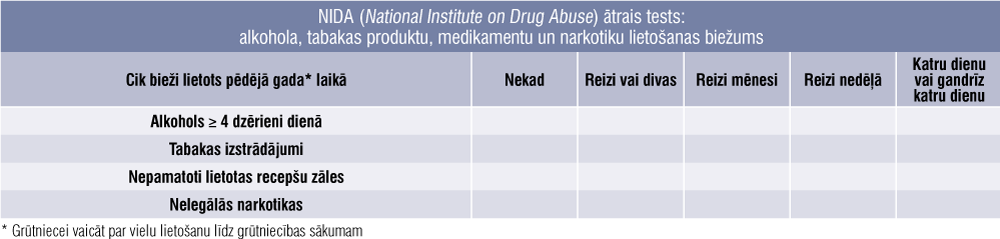

Tabula
NIDA (National Institute on Drug Abuse) ātrais tests: alkohola, tabakas produktu, medikamentu un narkotiku lietošanas biežums
Vīzītes laikā jānoskaidro arī par sievietes partneri un iespējamu vardarbību ģimenē. Ideālā gadījumā skrīnings būtu jāveic sākotnējā pirmsdzemdību vizītē, vismaz reizi trimestrī un vēlreiz pēcdzemdību aprūpes laikā. Skrīnings regulāri jāveic sievietēm, kurām nav bijusi antenatālā aprūpe vai kurām ir šādas pazīmes: redzami ievainojumi, hroniskas neizskaidrojamas sāpes vēderā un galvassāpes, seksuāli transmisīvās infekcijas u.c. Ir vairāki apstiprināti skrīningi.
Pacientei ar gestācijas diabētu 6—8 nedēļas pēc dzemdībām jāveic orālais glikozes tolerances tests.
Sieviete jāinformē par turpmāko paaugstināto risku cukura diabēta attīstībai, pat ja pēcdzemdību glikozes tolerances tests ir normāls. Šādai sievietei var rekomendēt dzīvesveida maiņu, fiziskas aktivitātes un liekā svara samazināšanu.
Sievietēm ar gestācijas diabētu, gestācijas hipertensiju vai priekšlaicīgām dzemdībām ir paaugstināts risks sirds un asinsvadu sistēmas slimību attīstībai nākotnē, pat ja pēcdzemdību asinsspiediens un glikozes tolerances testi ir normāli.
ACOG iesaka aprūpes speciālistiem informēt pacientes par paaugstināto kardiovaskulārās sistēmas slimību risku. Sievietēm ar preeklampsiju jānozīmē ikgadēja asinsspiediena, lipīdu, glikozes līmeņa tukšā dūšā noteikšana asinīs un ķermeņa masas indeksa novērtēšana. Labāka informētība par savu kardiovaskulāro risku var palielināt sievietes motivāciju samazināt modificējamos riska faktorus un dzīvot veselīgāk.
Dzemdes kakla skrīningā jāievēro pieņemtās vadlīnijas.