Otrās līnijas imūnmodulējoša terapija multiplās sklerozes pacientiem Latvijā
Latvijā pastāvīgi pieaug no jauna diagnosticēto multiplās sklerozes pacientu skaits. Multiplās sklerozes ārstēšanas pamatprincipi postulēti 2018. gadā NVD apstiprinātajās “Multiplās sklerozes klīniskajās vadlīnijās”, taču medikamentu skaits ir pieaudzis.
Lai novērstu progresējošu un neatgriezenisku neiroloģisku traucējumu attīstību, multiplās sklerozes pacientiem agrīni jāsāk imūnmodulējoša terapija. Latvijā multiplās sklerozes pacientus tūlīt pēc aktīvas multiplās sklerozes diagnozes apstiprināšanas sāk ārstēt ar pirmās līnijas imūnmodulējošiem medikamentiem, tādiem kā interferons bēta 1a, interferons bēta 1b, glatiramēra acetāts, teriflunomīds vai dimetilfumarāts.
Regulāri novērtējot klīnisko stāvokli un kontrolējot magnētiskās rezonanses attēlveidošanas (MRA) izmeklējumus, tiek izvērtēta slimības aktivitāte. Par aktīvu multiplās sklerozes norisi liecina jaunu demielinizējošu perēkļu veidošanās galvas un muguras smadzenēs, kā arī klīniskie paasinājumi. Pirmās līnijas medikamentu nepanesības vai neefektivitātes gadījumā terapija savlaicīgi jāmaina uz otrās līnijas medikamentiem, t.i., jāveic terapijas eskalācija.
Šobrīd otrās līnijas imūnmodulējošie medikamenti Latvijā ir ofatumumabs, natalizumabs, okrelizumabs, kladribīns un fingolimods.
Šajā rakstā analizējam Latvijā pieejamo multiplās sklerozes otrās līnijas imūnmodulējošo medikamentu indikācijas, darbības mehānismu, efektivitāti, blaknes un terapijas laikā kontrolējamos parametrus.
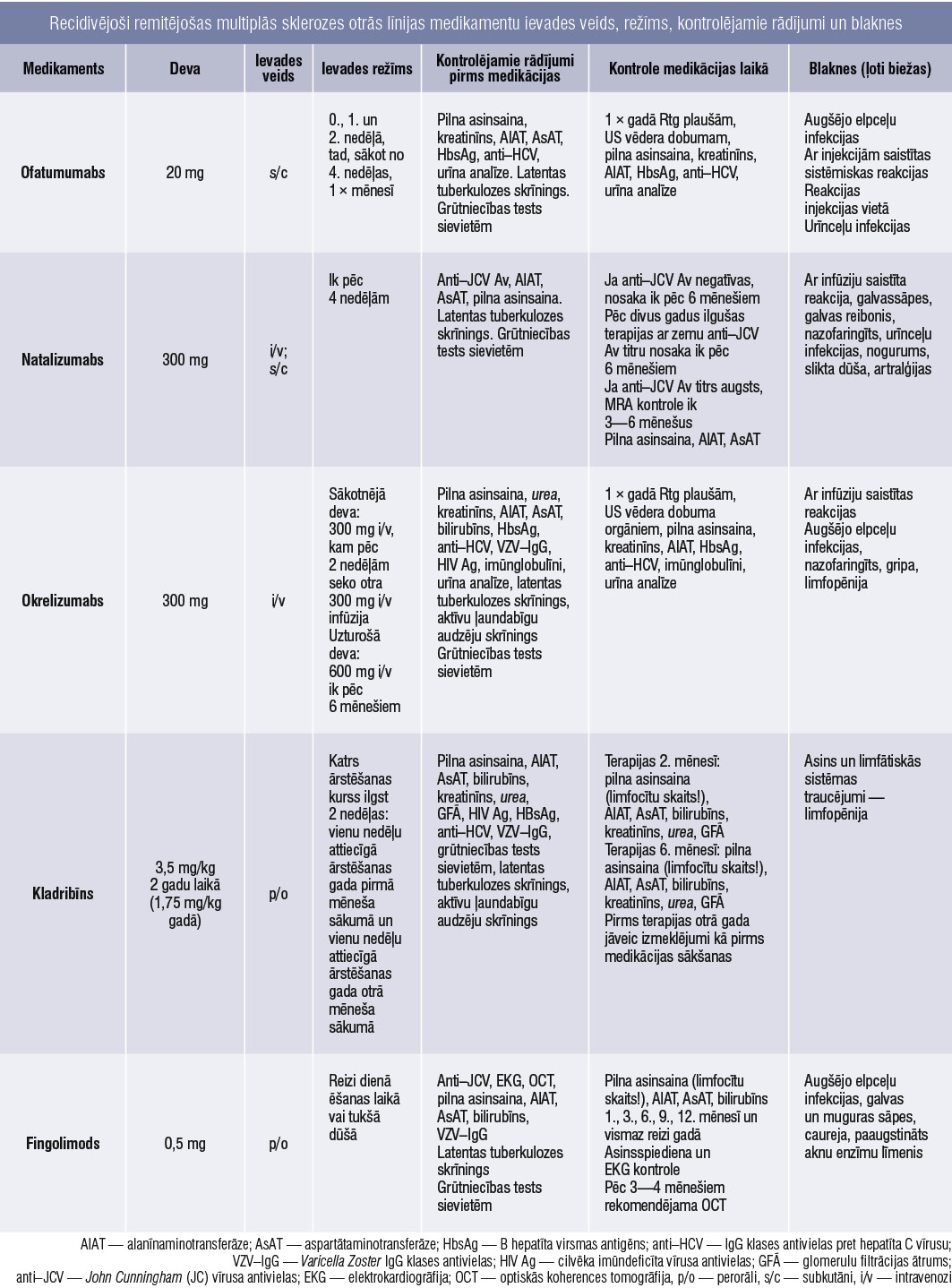
Otrās līnijas medikamentu lietošanas veids un režīms, kontrolējamie rādījumi un blaknes apkopoti tabulā.

Ofatumumabs
Ofatumumabu lieto pacientiem ar recidivējošām multiplās sklerozes formām un aktīvu slimību, par ko liecina klīniskas vai MRA izmeklējumā atklātas pazīmes. Kontrindikācijas: pastiprināta jutība pret aktīvo vielu vai jebkuru no palīgvielām, pacienti smagā imūnkompromitētā stāvoklī, smaga aktīva infekcija, līdz tā nav izārstēta, kā arī zināms aktīvs ļaundabīgs audzējs.
Ofatumumabs ir cilvēka izcelsmes anti–CD20 monoklonāla imūnglobulīna G1 antiviela. CD 20 molekula ir transmembranozs fosfoproteīns, kas ekspresēts uz B limfocītiem no B limfocītu priekšteču šūnām līdz B limfocītu nobriedušajai stadijai. CD20 molekula ir ekspresēta arī uz nelielas aktivēto T šūnu daļas. Ofatumumaba saistīšanās ar CD20 izraisa CD20+ B limfocītu līzi, kas notiek galvenokārt caur no komplementa atkarīgu citotoksicitāti un mazākā mērā caur no antivielām atkarīgu šūnu mediētu citotoksicitāti. Ofatumumabs samazina arī CD 20 ekspresējošo T šūnu skaitu.
Ofatumumaba efektivitāte un drošums novērtēts divos nejaušinātos, divkārt maskētos III fāzes pētījumos ASCLEPIOS I un ASCLEPIOS II ar identisku plānojumu. Šajos pētījumos attiecīgi 927 un 955 pacienti ar recidivējošu MS nejaušināti tika iedalīti grupās 1 : 1 un saņēma vai nu subkutānu 20 mg ofatumumaba injekciju ik pēc četrām nedēļām, vai arī iekšķīgi 14 mg teriflunomīda dienā. Abos III fāzes pētījumos ofatumumabs, salīdzinot ar teriflunomīdu, parādīja ievērojamu recidīvu biežuma samazinājumu gada griezumā attiecīgi par 50,5 % un 58,5 %. Ofatumumabs salīdzinājumā ar teriflunomīdu ievērojami samazināja trīs mēnešu apstiprinātas invaliditātes progresēšanas (AIP) risku par 34,4 % un sešu mēnešu AIP risku par 32,5 %. Ofatumumabs salīdzinājumā ar teriflunomīdu ievērojami samazināja kontrastvielu uzkrājošu T1 bojājumu skaitu par 95,9 % un jaunu vai palielinājušos T2 bojājumu biežumu par 83,5 % (vērtības norāda vidējo samazinājumu abos pētījumos).
Svarīgākās un biežāk ziņotās nevēlamās blakusparādības ir augšējo elpceļu infekcijas (39,4 %), ar injekcijām saistītas sistēmiskas reakcijas (20,6 %), reakcijas injekcijas vietā (10,9 %) un urīnceļu infekcijas (11,9 %). Dati par ofatumumaba lietošanu grūtniecēm ir ierobežoti.
Dati no pētījumiem ar dzīvniekiem rāda, ka ofatumumabs var šķērsot placentāro barjeru un izraisīt augļa B limfocītu izsīkumu.
Sievietēm reproduktīvā vecumā, lietojot ofatumumabu, kā arī sešus mēnešus pēc pēdējās ofatumumaba ievadīšanas jālieto efektīva kontracepcijas metode (kas nodrošina grūtniecības varbūtību zem 1 %). [1]
Natalizumabs
Natalizumabs paredzēts pacientiem ar ļoti aktīvi noritošu recidivējoši remitējošu multiplo sklerozi. Šobrīd pieejams infūziju veidā un pilnšļirču veidā subkutānai ievadīšanai reizi mēnesī. Kontrindicēts, ja pacientam ir pastiprināta jutība pret natalizumabu, ir diagnosticēts aktīvs ļaundabīgs audzējs, izņemot ādas bazālo šūnu karcinomu (bazaliomu), kombinācijā ar citu imūnmodulējošu vai imūnsupresīvu medikamentu, ir progresējoša multifokāla leikoencefalopātija (PML) un pacientiem ar imūnsistēmas darbības traucējumiem.
Natalizumabs ir rekombinēta IgG4k monoklonāla antiviela. Natalizumabs piesaistās α4β1 integrīnam, bloķējot tā mijiedarbību ar receptoru, asinsvadu šūnu piesaistīšanas molekulu–1 (VCAM–1), ligandu osteopontīnu un alternatīvi savīto domēnu fibronektīnu, tā savienošanās segmentu–1 (CS–1). Natalizumabs bloķē α4β1 integrīna mijiedarbību ar tā gļotādu šūnu adhēzijas molekulu–1 (MadCAM–1). Bloķējot šos receptorus, leikocīti tiek cauri endotēlijam iekaisušajos parenhīmas audos, tālāk nomācot iekaisuma reakciju slimajos audos un kavējot turpmāku imūnsistēmas šūnu nonākšanu iekaisušajos audos. [2; 3]
Natalizumaba klīniskā efektivitāte pierādīta dažādos pētījumos, piemēram, AFFIRM par 942 dalībniekiem ar RRMS, kurš bija nejaušināts, divkārt maskēts, ar placebo kontrolēts pētījums, ilga divus gadus un kurā tika pierādīta natalizumaba efektivitāte: par 68 % samazinājās paasinājumu skaits gada laikā, par 42 % samazinājās invaliditāte divu gadu laikā, kā arī par 83 % samazinājās jaunu perēkļu skaits MRA izmeklējumā divu gadu laikā, salīdzinot ar placebo grupu, un par 92 % samazinājās gadolīniju krājošo perēkļu skaits, salīdzinot ar placebo grupu.
Pētījumā SENTINEL par 1171 RRMS pacientu tika salīdzināta kombinētā terapija: natalizumabs ar IFN–β–1a 30 µg i/m reizi nedēļā un placebo kombinācijā ar IFN–β–1a 30 µg i/m reizi nedēļā. Arī tika pierādīta lielāka efektivitāte natalizumaba grupā, samazinot paasinājumu skaitu, invaliditāti divu gadu periodā un perēkļu skaitu MRA.
Savukārt pētījumā ASCEND tika iekļauti 887 multiplās sklerozes pacienti ar sekundāri progresējošu slimības norisi. Šajā pētījumā tika salīdzināts natalizumabs ar placebo grupu. Netika novērota atšķirība slimības progresēšanā, taču natalizumaba grupā tika novērots perēkļu skaita samazinājums un gadolīniju krājošo perēkļu skaita samazinājums. Šajos pētījumos tika novērotas arī blaknes, nopietnākā no tām ir progresējoša multifokāla leikoencefalopātija. Tātad natalizumaba lietošana saistīta ar palielinātu progresējošas multifokālas leikoencefalopātijas un nosacīti patogēno infekciju risku, kuru izraisa John Cunningham vīruss (JCV), un iznākums var būt letāls vai arī var izraisīt smagu invaliditāti. Taču, kā jau iepriekš minēts, šī nopietnā blakne sastopama reti, turklāt natalizumaba lietošanas laikā tiek ļoti cītīgi uzraudzīta.
Biežākās novērotās blaknes ir galvassāpes (32 %), nazofaringīts (27 %), nogurums (23 %), urīnceļu infekcijas (16 %), slikta dūša (15 %), artralģijas (14 %), galvas reibonis (11 %) un ar infūziju saistīta reakcija (23,1 %). [2] Natalizumabu nav ieteicams lietot grūtniecības laikā, jo nav pietiekamu un labi kontrolētu pētījumu par sievietēm grūtniecības laikā, taču to drīkst lietot, ja tā ir absolūta nepieciešamība, izvērtējot riskus un ieguvumus.
Ja slimība ir ļoti aktīva, natalizumabu lieto pirmo trimestri, tad pārtrauc un atsāk iespējami drīz pēc dzemdībām. Taču barošana ar krūti, lietojot natalizumabu, ir kontrindicēta, jo tas izdalās mātes pienā un nav zināma tā ietekme uz zīdaini. [2; 5]
Okrelizumabs
Okrelizumabu lieto gan recidivējošas, gan progresējošas multiplās sklerozes ārstēšanā. Līdz šim tas ir vienīgais medikaments, kura efektivitāte pierādīta primāri progresējošas multiplās sklerozes (PPMS) ārstēšanā. Okrelizumabs kontrindicēts gadījumos, kad novērota pastiprināta jutība pret aktīvo vielu vai jebkuru no palīgvielām, pacientam ir aktīvi noritoša infekcija, smagi imūnsistēmas darbības traucējumi (piemēram, limfopēnija, neitropēnija, hipogammaglobulinēmija), kā arī zināms aktīvs ļaundabīgs audzējs vai novērošanās attiecībā uz iespējamu jaunveidojuma recidīvu, grūtniecība.
Okrelizumabs ir humanizēta monoklonāla anti CD20 receptoru antiviela, kas selektīvi samazina B šūnu ar CD20 antigēnu ekspresiju skaitu, saglabājot B šūnām raksturīgo humorālo imunitāti, neietekmējot T šūnu skaitu, tādējādi neizmainot adaptīvās imūnās sistēmas atbildreakcijas.
Okrelizumaba efektivitāte un drošums recidivējošas multiplās sklerozes (RMS) ārstēšanai novērtēts divos pētījumos (1656 pacientiem), vidējais recidīvu skaits ar okrelizumabu ārstētajiem pacientiem bija gandrīz divreiz mazāks nekā pacientiem, kurus ārstēja ar interferonu bēta–1a (0,16 pret 0,29 recidīviem gadā).
Efektivitāte primāri progresējošas multiplās sklerozes ārstēšanā pierādīta pētījumā ORATORIO, kurā piedalījās 732 pacienti. Okrelizumaba grupā tika konstatēts mazāk pacientu ar simptomu pasliktināšanos, kas ilgst vismaz 12 nedēļas (30 %), nekā placebo grupā (34 %). Okrelizumaba ievadei jānotiek ārsta speciālista uzraudzībā, kura rīcībā ir piemēroti līdzekļi un aprīkojums anafilaktisku reakciju kontrolei.
Svarīgākās nevēlamās blakusparādības, par kurām ziņots biežāk, ir reakcijas, kas saistītas ar infūziju (infusion-related reactions jeb IRR), un infekcijas. IRR novēroja 40,1 % RMS pacientu, smagas IRR bija 2,4 % pacientu, bet 0,1 % pacientu bija dzīvībai bīstamas IRR; PPMS pacientiem IRR novēroja 40,1 % pacientu, 1,4 % pacientu bija smagas IRR. Infekcijas RMS pacientiem novēroja 58,5 % gadījumu, no tām nopietnas infekcijas 1,3 % pacientu, PPMS pacientiem infekcijas 72,2 % gadījumu, no tām nopietnas infekcijas 6,2 % pacientu.
Biežāk laboratorisko analīžu rezultātu novirzēs novēroja limfocītu līmeņa pazemināšanos RMS gadījumā 20,7 %, PPMS gadījumā 26,3 % un kopējā imūnglobulīnu, galvenokārt IgM, līmeņa pazemināšanos.
Pacientiem ar nieru darbības traucējumiem okrelizumaba deva nav jāpielāgo. Pacientiem ar vidēji smagiem vai smagiem aknu darbības traucējumiem okrelizumaba lietošana nav novērtēta. Tāpat nav novērtēta medikamenta lietošana bērnu un pusaudžu vecumā.
Sievietēm reproduktīvā vecumā okrelizumaba lietošanas laikā un vēl 12 mēnešus pēc pēdējās tā infūzijas jāizmanto droša kontracepcijas metode. Sievietēm jāiesaka terapijas ar okrelizumabu laikā pārtraukt bērnu barot ar krūti. [6]
Kladribīns
Kladribīns paredzēts lietošanai pieaugušiem pacientiem, lai ārstētu ļoti aktīvu recidivējošu multiplo sklerozi, kuras aktivitāte definēta saskaņā ar klīniskajiem vai radioloģiskās izmeklēšanas kritērijiem.
Kladribīns kontrindicēts pacientiem ar pastiprinātu jutību pret aktīvo vielu vai jebkuru no palīgvielām, pacientiem ar aktīvu ļaundabīgu audzēju, nopietnu aktīvu, hronisku infekcijas slimību (HIV, tuberkulozi, hepatītu). Kladribīnu nedrīkst nozīmēt pacientiem ar imūnsistēmas darbības traucējumiem, pacientiem, kuri saņem imūnsupresīvas vai mielosupresīvas terapijas līdzekļus, kā arī pacientiem ar vidēji smagiem vai smagiem nieru darbības traucējumiem jeb kreatinīna klīrensu < 60 ml/min.
Kladribīna terapeitiskās iedarbības mehānisms MS gadījumā nav pilnībā skaidrs, tomēr uzskata, ka tā dominējošā iedarbība uz B un T limfocītiem pārtrauc MS raksturīgo imūnsistēmas notikumu kaskādi. Atklāts, ka kladribīna iedarbība ir ilgstoša un ka pārsvarā tā skar limfocītus un autoimūnos procesus, kas iesaistīti MS patofizioloģijā.
Iekšķīgi lietota kladribīna efektivitāte un drošums izvērtēti nejaušinātā, divkārt maskētā, ar placebo kontrolētā klīniskā pētījumā CLARITY par 1326 pacientiem ar recidivējoši remitējošu MS. Pētījuma mērķi bija izvērtēt kladribīna efektivitāti salīdzinājumā ar placebo attiecībā uz ikgadējā recidīvu skaita samazināšanos, invaliditātes progresēšanas samazināšanos un aktīvo bojājumu skaita samazināšanos MRA izmeklējumā. Pacienti saņēma vai nu placebo (n = 437), vai arī kumulatīvu kladribīna devu 3,5 mg/kg (n = 433) vai 5,25 mg/kg ķermeņa masas (n = 456) divos ārstēšanas kursos pētījuma periodā (96 nedēļas jeb divus gadus). Pacientiem ar recidivējoši remitējošu MS, kas saņēma kladribīnu 3,5 mg/kg, konstatēja statistiski ticamu uzlabošanos attiecībā uz ikgadējo recidīvu skaitu (ikgadējais recidīvu skaits (95 % TI) 0,14* (0,12; 0,17), pacientu proporciju, kurai 96 nedēļu laikā nenovēroja recidīvu (79,7 % ), pacientu daļu, kurai 96 nedēļu laikā nenovēroja stabilu invaliditātes progresēšanu, un laiku līdz trīs mēnešus ilgai EDSS progresēšanai (10. procentile (mēneši) 13,6) salīdzinājumā ar pacientiem placebo grupā.
Svarīgākās un biežāk ziņotās nevēlamās blakusparādības ir infekcijas slimības (Herpes zoster), asins un limfātiskās sistēmas slimības (limfopēnija 20—25 %), imūnās sistēmas traucējumi (pastiprināta jutība, nieze, nātrene, izsitumi un retos gadījumos angioneirotiskā tūska — 11,8 %), aknu bojājums, ādas un zemādas audu bojājumi (izsitumi, alopēcija).
Sievietēm reproduktīvā vecumā pirms kladribīna sākšanas 1. un 2. ārstēšanas gadā jāizslēdz grūtniecība, terapijas laikā un vismaz sešus mēnešus pēc pēdējās kladribīna devas lietošanas jāizsargājas no grūtniecības, izmantojot efektīvu kontracepcijas metodi. Terapijas laikā un vismaz četras nedēļas pēc pēdējās kladribīna devas lietošanas katrā ārstēšanas gadā sievietēm, kuras lieto sistēmiskas darbības hormonālās kontracepcijas līdzekļus, papildus jālieto arī barjermetode.
Tā kā kladribīns kavē DNS sintēzi, iespējama nevēlama ietekme uz cilvēku gametoģenēzi, tāpēc vīriešiem terapijas laikā un vismaz sešus mēnešus pēc pēdējās kladribīna devas lietošanas jāizmanto kontracepcijas līdzekļi, lai izsargātos no partneres grūtniecības. Nav zināms, vai kladribīns izdalās cilvēka pienā. Ņemot vērā iespējamās nopietnās nevēlamās blakusparādības ar krūti barotiem zīdaiņiem, barošana ar krūti ir kontrindicēta terapijas ar kladribīnu laikā un nedēļu pēc pēdējās devas lietošanas. [7]
Fingolimods
Fingolimodu lieto pacientiem ar recidivējoši remitējošu multiplās sklerozes formu, kad slimība ir aktīva, norit strauji un klīniskie simptomi ir smagi.
Kontrindikācijas: pastiprināta jutība pret aktīvo vielu vai jebkuru no palīgvielām, pacienti imūnkompromitētā stāvoklī, smaga aktīva infekcija, līdz tā nav izārstēta, vai aktīva hroniska infekcija, zināms aktīvs ļaundabīgs audzējs, smagi aknu darbības traucējumi, sirds ritma traucējumi, grūtniecība.
Fingolimods darbojas, bloķējot sfingozīna–1–fosfāta receptoru darbību uz T šūnu virsmas. Šie receptori iesaistīti T šūnu pārvietošanās regulācijā organismā, tādējādi medikaments ierobežo T šūnu pārvietošanos uz centrālo nervu sistēmu un demielinizējošu perēkļu veidošanos.
Trīs pamatpētījumos pieaugušajiem pierādīts, ka fingolimods ir efektīvāks par placebo un bēta–1a–interferonu pacientiem ar recidivējoši remitējošu multiplās sklerozes formu. Galvenais efektivitātes rādītājs visos pētījumos bija pacienta recidīvu skaits gada laikā.
Divos no šiem pētījumiem, kuros kopā piedalījās 2355 pacienti, fingolimods divus gadus tika salīdzināts ar placebo. Ar fingolimodu ārstētajiem pacientiem bija aptuveni uz pusi mazāk recidīvu nekā pacientiem, kuri saņēma placebo.
Trešajā pētījumā, kurā piedalījās 1292 pacienti, fingolimods vienu gadu tika salīdzinātas ar bēta–1a–interferonu. Ar fingolimodu ārstētajiem pacientiem bija aptuveni uz pusi mazāks recidīvu skaits nekā pacientiem, kuri lietoja bēta–1a–interferonu. Svarīgākās un biežāk ziņotās nevēlamās blakusparādības ir augšējo elpceļu infekcijas, Varicella zoster infekcija, galvas un muguras sāpes, caureja, sirds ritma traucējumi, makulas tūska, paaugstināts aknu enzīmu līmenis, depresija un trauksme.
Fingolimodu nedrīkst lietot grūtniecības laikā, jo bērniem novērotais iedzimtu anomāliju risks ir divreiz lielāks nekā vispārējā populācijā. Visbiežāk ziņotās anomālijas ir sirds, nieru sistēmas un balsta—kustību aparāta anomālijas. Fingolimoda lietošanas periodā nedrīkst bērnu barot ar krūti, jo medikaments nonāk mātes pienā un ir risks nopietnu blakusparādību attīstībai bērnam. [8]
Noslēgumā
Kopumā Latvijā pieejamie otrās līnijas medikamenti ir efektīvi un labi panesami, turklāt 100 % valsts kompensēti multiplās sklerozes pacientiem. Medikamenta izvēli nosaka pacienta vēlmes par medikamenta ievades veidu un biežumu, slimības aktivitātes rādītāji un paredzamās blaknes, kā arī grūtniecības plānošana.
Šobrīd trūkst klīnisko pētījumu par otrās līnijas medikamentu savstarpēju maiņu nepanesības vai neefektivitātes gadījumā, taču aizvien biežāk tiek uzsvērta nepieciešamība agrīni sākt iespējami efektīvāko multiplās sklerozes terapiju, tādējādi nepieļaujot slimības progresēšanu.
Literatūra
- www.ema.europa.eu/en/documents/product-information/kesimpta-epar-product-information_lv.pdf
- www.ema.europa.eu/en/documents/product-information/tysabri-epar-product-information_lv.pdf
- www.tysabri.com/content/dam/commercial/tysabri/pat/en_us/pdf/tysabri_prescribing_information.pdf
- Brandstadter R, Katz Sand I. The use of natalizumab for multiple sclerosis. Neuropsychiatric Disease and Treatment, 2017; 13: 1691-1702. doi:10.2147/ndt.s114636
- Simone IL, Tortorella C, Ghirelli A. Influence of Pregnancy in Multiple Sclerosis and Impact of Disease-Modifying Therapies. Front Neurol, 2021; 12: 697974. doi: 10.3389/fneur.2021.697974
- www.ema.europa.eu/en/documents/product-information/ocrevus-epar-product-information_lv.pdf
- www.ema.europa.eu/en/documents/product-information/mavenclad-epar-product-information_lv.pdf
- www.ema.europa.eu/en/documents/product-information/gilenya-epar-product-information_lv.pdf