Migrēnas komplikācijas

Migrēnas komplikācijas nosacīti var iedalīt vairākās apakšgrupās: pirmkārt, saistītas ar migrēnas lēkmi — status migrenosus, kardiovaskulāri notikumi (migrenozs insults vai infarkts), ieilgusi aura, migrenoza epilepsija, otrkārt, saistītas ar neārstētu vai ilgstoši neadekvāti ārstētu slimību vai arī saistītas ar ļaundabīgu slimības gaitu — hroniska migrēna, migrēnu pavadošie simptomi (depresija, trauksme utt.), treškārt, saistītas ar medikamentu lietošanu.
Taču, sekojot ICHD 3 (International Classification of Headache Disorders 3rd edition) klasifikācijai, par komplikācijām tiek uzskatītas tieši ar lēkmi saistītās izpausmes. Tā kā pēdējā laikā arī Latvijā par migrēnu tiek runāts daudz, šajā reizē pievērsīsimies tieši šai mazāk iztirzātajai migrēnas komplikāciju tēmai, īpaši akcentējot biežākās no tām.
Kardiovaskulāri notikumi
Migrenozs cerebrāls infarkts
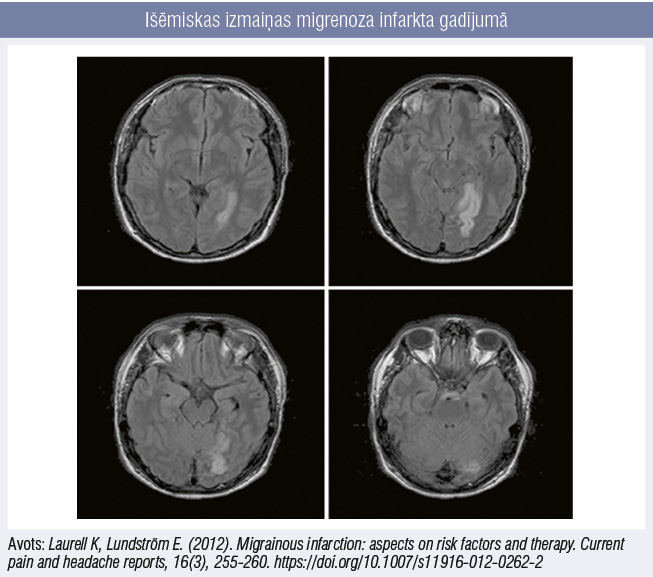

Raksturīgs viens vai vairāki migrēnas auras simptomi, kuri kombinējas ar radioloģiski pierādītu smadzeņu bojājumu (1. attēls), kas laika ziņā un teritoriāli atbilst auras izpausmei. Biežāk izpaužas jaunām sievietēm mugurējā cirkulācijas baseinā.
Diagnostiskie kritēriji pēc ICHD:
- A — migrēnas auras kritēriji atbilst B un C,
- B — izpaužas pacientiem ar migrēnu ar auru ar tipiskām lēkmēm, ja viens vai vairāki auras simptomi ilgst virs 60 minūtēm,
- C — radioloģiskā atrade atbilst auras simptomātikai,
- D — nav ticamākas diagnozes.
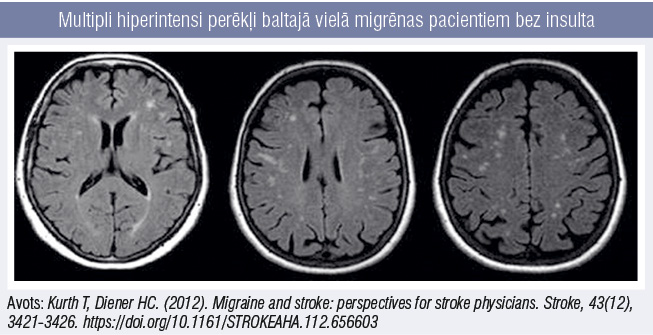

Jāpatur prātā, ka multipli hiperintensi perēkļi baltajā vielā migrēnas pacientiem var būt arī bez insulta (radioloģiski atainoti 2. attēlā), kas izskaidrojams ar migrēnas patoģenēzi (skatīt tālāk tekstā).
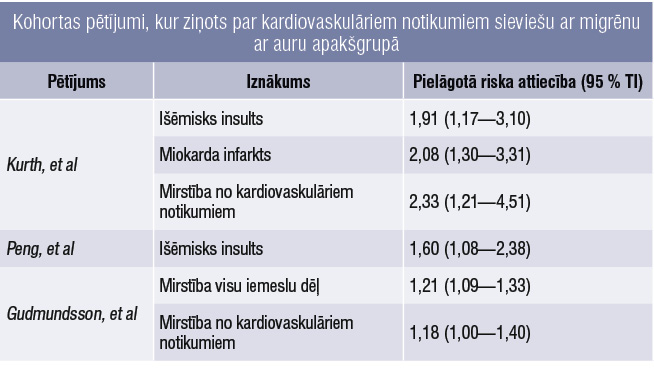
Pēdējā laikā daudz tiek runāts par to, ka migrēna ar auru var palielināt kardiovaskulāro notikumu risku (tabula). Tā kā biežāk tas attiecināms uz jaunām sievietēm, šai problēmai būtu jāpievērš īpaša uzmanība. Atgādinājumam — epizodiskai migrēnai raksturīgas stipras līdz ļoti stipras galvassāpes ar vai bez fokālas neiroloģiskas simptomātikas (migrēnas ar auru gadījumā), kas var saglabāties 4—72 stundas.

Aura raksturīga vidēji vienam no trīs pacientiem, un tās izpausmes var būt dažādas: vizuālas (bieži: gaisma, mirgošana acu priekšā, redzes lauka defekts), audiālas (trokšņi ausīs), somatosensoriskas (tirpšana, kņudināšana, ožas traucējumi u.tml.), veģetatīvas (svīšana, pastiprināta kuņģa—zarnu trakta motorika, slikta dūša), motoriskas (muskuļu krampji, parēzes kādā ķermeņa daļā).
Biežākā ir optiskā aura, un tipiskā gadījumā tai seko galvassāpes. Parasti aura ilgst līdz vienai stundai (biežāk 30—40 minūtes).
Migrēnas lēkmju skaits mēdz būt variabls. Lēkmes var būt ļoti reti, reizi gadā vai pat retāk, bet var būt vairākas reizes nedēļā. Ja migrēnas epizodes ir vairāk nekā 15 dnn mēnesī, to sauc par hronisku migrēnu.
Patoģenētiskie mehānismi, kas saistīti ar kardiovaskulāro risku
Migrēnai ir daudzfaktoru etiopatoģenēze, kas joprojām nav līdz galam skaidra. Ja runājam par migrenozu insultu, pirmkārt, jāņem vērā tradicionālie riska faktori: arteriāla hipertensija, dislipidēmija, ģenētika (MTHFR C677T polimorfisms, ACE–DD polimorfisms u.c.), kontracepcijas preparātu lietošana, smēķēšana.
Otrkārt, migrēna, īpaši migrēna ar auru, ir sistēmiska slimība, kam raksturīga endotēlija disfunkcija un pastiprināta trombocītu agregācija. Treškārt, migrēnas ar auru pacientiem 50 % gadījumu novēro PFO, kas var radīt paradoksālu embolizāciju. Ceturtkārt, ilgstoša imobilizācija migrēnas lēkmes laikā sāpju dēļ var provocēt venozas trombozes. Piektkārt, migrēnas pacienti lēkmes laikā bieži lieto NSPL, kas arī palielina risku kardiovaskulāro notikumu attīstībai.


Noteikti nevar ignorēt arī komorbīdas slimības, īpaši tādas kā antifosfolipīdu sindroms, sarkanā vilkēde u.c. vaskulīti (3. attēls).
Hormonu nozīme
Nevar neskart šo tēmu, ņemot vērā statistiku. Jau minēts, ka biežāk migrēna sākas pubertātes vecumā un lēkmes mazinās vai pazūd pēcklimktēriskajā periodā. Turklāt ir vispārzināma migrēnas lēkmju saistība ar menstruālo ciklu (premenstruālā, menstruālā periodā lēkmes mēdz būt biežāk vai raksturīgas tikai šim periodam), grūtniecību (lēkmes mēdz pazust vispār vai kļūst ievērojami retākas), kombinēto kontraceptīvu lietošanu (vairākumā gadījumu lēkmes tomēr ir biežākas, lai gan pastāv uzskats, ka lēkmju skaits tāpēc nemainās).
Ir pētījumu dati, ka sievietēm ar augstāku testosterona līmeni migrēnas novēro retāk. Viss iepriekš minētais nešaubīgi parāda milzīgo estrogēna lomu šajā procesā.
Ir vairāki nopietni pētījumi, kuros pacienti (70 % sieviešu) novēroti 20 gadu garumā un kuri rāda kardiovaskulāros riskus migrēnas pacientiem, arī kardiovaskulārās nāves riskus (tabula).
Migrēna un PFO (persistējoša foramen ovale)
Migrēnas sastopamības biežuma rādītājs pacientiem ar PFO un insultu vai TIL ir 35—60 %. Kaut arī ir vairāki novērojumi par to, ka FO slēgšana samazina migrēnas lēkmju skaitu (novērojumi gadījumos, kad šī manipulācija tika veikta, piemēram, sakarā ar kriptogēnu insultu), migrēna nav indikācija šai manipulācijai.
Ir ļoti uzmanīgi jāizsver visi apstākļi, un to veic tikai īpašos gadījumos (atkārtoti TIL vai insulti — lai gan pacients lieto medikamentus, kontrindicēti medikamenti vai pacients tos nevēlas lietot mūža garumā, augsta riska PFO). Turklāt nevajag aizmirst, ka PFO sastop vidēji 25 % populācijā arī bez migrēnas simptomiem.
Migrenoza insulta un TIL ārstēšana būtiski neatšķiras no medikamentozas pārējo insultu terapijas. Taču jāņem vērā, ka medikamentu izvēle migrēnas pacientiem ir specifiska, piemēram, vairākos pētījumos pierādīts, ka cilostazols — antiagregants, kas inhibē fosfodiaesterāzi 3 un kam ir arī vazodilatējošs efekts, var izprovocēt galvassāpes, kas ļoti līdzinās migrēnai (23 % gadījumu), kā arī izprovocēt lēkmi pacientiem ar migrēnu anamnēzē.
Šā medikamenta provocētas migrēnas gadījumā palīdz triptāni. Lai samazinātu galvassāpju rašanos, cilostazols jāsāk dot nelielās devās, tās pamazām palielinot divu nedēļu laikā. Dipiridamols ir fosfodiesterāzes–5 inhibitors, un ir aprakstīta tā spēja ierosināt migrēnas ar auru lēkmi.
Ārstējot pacientus ar migrēnu un paaugstinātu asinsspiedienu, ieteicams izvēlēties Ca kanālu blokatorus, bēta blokatorus, sartānus (pierādīti efektīvi ir kandesartāns, olmesartāns) vai lizinoprilu. Ja insults kombinējas ar hiperholesterinēmiju, no statīniem ieteicams atorvastatīns vai simvastatīns 20 mg (reducē CGRP ekspresiju, mazina migrēnas sāpes).
Status migrenosus (G43.2)
Pēc ICHD klasifikācijas tā ir stipra, nepārejoša migrēnas lēkme, kas ilgst vairāk nekā 72 stundas un kam raksturīgi tipiski iepriekš reģistrēti ieilguši migrēnas simptomi, un šīs galvassāpes nav saistāmas ar citām slimībām.
Migrēna ir komplekss sindroms ar dažādām izpausmēm. Status migrenosus gadījumā prevalē izteiktas, grūti kupējamas sāpes, hipersensitivitāte, gastrointestināli traucējumi (atkārtota vemšana), kas var izraisīt elektrolītu disbalansu, dehidratāciju, hipotensiju un pat šoku.
Šo stāvokli provocē nepareiza vai pārmērīga medikamentu lietošana, stress, depresija, diētas kļūdas, hormonāli faktori, arī dažādas infekcijas (respiratoriskie vīrusi, uroģenitālās u.c. infekcijas).
Status migrenosus pēc ICHD diagnostiskajiem kritērijiem:
- A — galvassāpes atbilst kritērijiem B un C,
- B — izpaužas pacientiem ar migrēnu bez auras un/vai migrēna ar auru ar tipiskiem simptomiem iepriekš, izņemot lēkmes ilgumu un stiprumu,
- C — divi no nākamajiem trim kritērijiem:
- D — nepārejoša lēkme virs 72 stundām;
- E — sāpes un/vai pavadošie simptomi ir ļoti mokoši;
- F — nav citas atbilstošākas diagnozes.
Jāpiebilst, ka remisijas līdz 12 stundām sakarā ar medikamentu lietošanu vai miegu ir pieņemamas. Vieglākos gadījumos, ja neatbilst C2 kritērijiem, var būt uzskatāma par iespējamu migrēnu bez auras.
NB! Status migrenosus var sajaukt ar medikamentu pārmērīgas lietošanas izraisītām galvassāpēm, kā arī šī galvassāpju forma var izraisīt migrenozu statusu, tāpēc jāuzmanās ar diferenciāldiagnozi un diagnožu kodiem.
Status migrenosus diferenciāldiagnozes
- Intoksikācija (smagie metāli, acidoze, alkaloze, medikamenti).
- Metaboliskie traucējumi (endokrinopātijas, aknu, nieru mazspēja u.tml.).
- Intra– un ekstrakraniālas infekcijas.
- Iekaisīgās slimības (vaskulīti, citas autoimūnas slimības).
- Subarahnoidāla hemorāģija.
- Venozo sinusu vai kortikālo vēnu trombozes.
- Pseudotumor cerebri jeb idiopātisks intrakraniālās hipertensijas sindroms — cerebrospinālā likvora producēšana ir pastiprināta vai resorbcija nepietiekama.
Ārstēšana
Pacienti ir hospitalizējami un stacionārā parasti pavada 2—4 dienas, dažkārt līdz septiņām dienām. Jāņem vērā prevalējošie simptomi un predisponējošie faktori. Tādējādi ārstēšana ietver gan pretsāpju, gan rehidratācijas terapiju, gan arī dažādu psihiatrisko stāvokļu (trauksmes, depresijas, apātijas utt.) korekciju.
Nākamajā sarakstā apkopoti pasaulē biežāk lietotie medikamenti un to lietošanas algoritms (Latvijā var būt variācijas sakarā ar pieejamību) no ICHD 2020. gada rekomendācijām, papildu komentāri no izmantotās literatūras avotiem.
Dihidroergotamīns (DHE) intravenozi
- Metoclopramidum 10 mg i/v 60 sekundēs.
- Gaidīt 5 minūtes.
- DHE 0,25—0,5 mg i/v.
- Gaidīt 5 minūtes.
- Atkārtot DHE 0,25—0,5 mg i/v.
Var atkārtot ik pēc 8 h 3—5 dienas. Blaknes: slikta dūša, dedzināšana, muskuļu krampji, paaugstināts asinsspiediens, sāpes krūtīs, galvassāpes, diareja. Nelietot pacientiem ar sirds slimībām, jo var palielināt miokarda išēmijas risku. Ja minētie medikamenti tiek lietoti vairāk nekā piecas dienas, ievērojami pieaug blakņu risks. Efektivitāte 70—90 % (pacienti atzīmē būtisku uzlabošanos).
Intravenozi ievadīti valproāti
- Deva variē līdz pat 500 mg stundā vai 750—1000 mg 24 stundās.
- Valproātu līmenis asinīs jāuztur zem 100 µg/ml.
- Blaknes: slikta dūša, reibonis, galvassāpes, izteikta miegainība.
- Efektivitāte 70 %.
Intravenozi ievadīts droperidols
- Metode:
- 1 mg droperidola i/v 60 sekundēs;
- 2,5 mg droperidola i/v 60 sekundēs;
- Blaknes: sedācija, akatīzija, trauksme, īslaicīga depresija, diskomforts.
- Efektivitāte 70—90 %.
Citi dopamīna antagonisti
- Chlorpromazinum.
- Prochlorperazinum.
- Metoclopramidum.
Intravenozi ievadīts lidokaīns
Metode — bolus 1 mg/kg vai infūzija 2 mg/min. 48 stundās. Blaknes: hipotensija, aritmija, hiperkaliēmija, slikta dūša, sāpes krūtīs, trauksme, paroksismāli stāvokļi. Rezultāti ir variabli.
Triptāni
Triptāni migrenoza statusa gadījumā maz efektīvi (30—40 % migrēnas pacientu triptāni ir neefektīvi), turklāt jāņem vērā kontrindikācijas: kardiovaskulārās slimības, grūtniecība, bazilārā migrēna, hemiplēģiska migrēna, slikti koriģējama arteriālā hipertensija.
Steroīdi
Pieminēti, bet rezultāti nav apkopoti (skatīt tālāk).
Opioīdi
Var lietot, bet īpaši piesardzīgi. Migrēnām tie nav īpaši efektīvi (vairāku autoru dati).
Kombinācijas un citi
Smagas migrēnas lēkmes ārstēšanai ieteicama arī kombinācija (var izmantot status migrenosus gadījumā):
- 1 l bolus i/v NaCl 0,9 % šķīduma,
- 10 mg i/v prochlorperazinum,
- 25 mg i/v diphenhydraminum,
- 30 mg i/v vai i/m ketorolacum, devu var atkārtot ik pēc 6 h (maksimāli 120 mg/dn),
- 10 mg i/v dexamethasonum, var lietot arī i/m. Nemazina sāpes, bet mazina varbūtību, ka migrēnas lēkmes atkārtosies nākamajās 72 stundās.
Jaunākie dati liecina, ka var izmantot celekoksibu un arī lasmiditānu, selektīvu serotonīna 5–HT receptoru agonistu, kas bloķē CGRP atbrīvošanos un sāpju impulsa pārvadi, nerada vazokonstrikciju atšķirībā no triptāniem, tāpēc var lietot, ja triptāni ir kontrindicēti. Jāpiebilst, ka ļoti dārgs, Latvijā nav pieejams.
Persistējoša migrēnas aura bez insulta
Samērā reti. Saskaņā ar ICHD 3 kritērijiem tā ir migrēnas aura, kas ilgst vairāk nekā vienu nedēļu un radioloģiski nav cerebrāla infarkta pierādījumu (veicot funkcionālos radioloģiskos izmeklējumus, raksturīga hipoperfūzija noteiktos smadzeņu garozas rajonos).
Šī migrēnas aura dažkārt var ilgt mēnešiem vai pat gadiem (diskutējams jautājums, vajadzīgi papildu pētījumi). Diagnostiskie kritēriji:
- A — aura atbilst kritērijiem B,
- B — izpaužas pacientiem ar migrēnu ar auru un tipisku auras simptomātiku iepriekš, kas šoreiz izpaužas ilgāk par vienu nedēļu,
- C — radioloģiski nav izmaiņu,
- D — nav ticamākas diagnozes.
Ārstēšana
Parasti neiedarbojas tādi bieži lietojamie medikamenti kā karbamazepīns, nifedipīns, flunarizīns, bēta blokatori. Izmantojami (ar daļēju efektu) valproāti, lamotrigīns, kā arī no bēta blokatoriem atenolols 25 mg ar furosemīdu 40 mg (efekts saistāms ar kālija vielu maiņu).
Migrēnas ar auru provocēta epilepsijas lēkme
Diagnostiskie kritēriji:
- A — epilepsijas lēkme, ko izraisījusi migrēna ar auru un kāds no B kritērijiem,
- B — izpaužas pacientiem ar migrēnu ar auru tās laikā vai stundas laikā kopš migrēnas ar auru sākuma,
- C — nav ticamākas diagnozes.
Migrēnai un epilepsijai ir līdzīgas izpausmes, runājot par paroksismālām smadzeņu izpausmēm. Arī epilepsijas gadījumā var būt migrēnai līdzīgas galvassāpes. Dažkārt epileptiskās lēkmes var izpausties migrēnas lēkmes laikā, un to apraksta kā migralepsiju, bet šis fenomens ir rets (termins ir novecojis), var būt arī epilepsijas provocētas migrēnas tipa galvassāpes, turklāt jautājums par to, kas ir primārs, kas — sekundārs, ir diskutabls un izaicinošs, vajadzīga detalizētāka analīze.
Ārstē kā epilepsijas lēkmes gadījumā un, ja nepieciešams, papildus lieto pretsāpju medikamentus.
Secinājumi
Lai gan migrēna ir sen zināma slimība ar diezgan skaidriem diagnostiskajiem kritērijiem, tomēr bieži tā netiek laikus atpazīta un atbilstoši ārstēta. Tas var radīt pamatu komplikāciju attīstībai.
Taču arī gadījumos, kad migrēna tiek atbilstoši koriģēta, var rasties komplikācijas. Kaut arī ir daudz jaunu un efektīvu medikamentu, ne vienmēr tie ir efektīvi. Tas saistāms ar ļoti variablo šīs slimības patoģenēzi. Tāpēc ļoti svarīgi ir izglītot gan pacientus, gan ārstus, lai šīs komplikācijas būtu retākas un vieglākas.
Kopsavilkums
- Par migrēnas komplikācijām pārsvarā tiek uzskatītas tieši ar lēkmi saistītās izpausmes.
- Komplikācijas ir status migrenosus, kardiovaskulāri notikumi (migrenozs insults vai infarkts), ieilgusi aura, migrenoza epilepsija.
- Rakstā apskatīti migrēnas komplikāciju diagnostiskie kritēriji pēc ICHD 3 (International Classification of Headache Disorders 3rd edition) un sniegtas ārstēšanas rekomendācijas.
Literatūra
- Burstein R, Collins B, Jakubowski M. Defeating migraine pain with triptans: a race against the development of cutaneous allodynia. Ann Neurol, 2004; 55: 1-19.
- PMC 2021 Dec 6 Migraine and Stroke: In Search of Shared Pathways, Mechanisms, and Risk Factors. Alexander Muacevic, John R Adler Mohammad Hassan, et al.
- Jessica Ailani, Rebecca C. Burch, Matthew S. Robbins, on behalf of the Board of Directors of the American Headache Society First published: 23 June 2021. The American Headache Society Consensus Statement: Update on integrating new migraine treatments into clinical practice.
- Hann J, Sluis P, Sluis LH, et al. Acetazolamide treatment for migraine aura status. Neurology, 2000; 55: 1588-1589.
- Headache Classification Committee of the International Headache Society. The international classification of headache disorders. Cephalalgia, 2004; 24[Suppl 1]: 32.
- International Classification of Headache Disorders (ICHD) (3rd Edition), 2018.
- Saurabh Gupta, Richard Oosthuizen, Simon Pulfrey, CCFP(EM), 2014; 60(1): 47-49. Treatment of acute migraine in the emergency department.
- Todd J Schwedt, Ivan Garza, Section Editor: Jerry W Swanson, Acute treatment of migraine in adults, Oct 20, 2021.
- Wang SJ, Silberstein SD, Young WB. Droperidol treatment of status migrainosus and refractory migraine. Headache, 1997; 37: 377.
- Elgendy, Stephen E. Nadeau, et al; on behalf of the American College of Cardiology Cardiovascular Disease in Women Committee, 11 Nov 2019. An Under-Appreciated Risk Factor for Cardiovascular Disease in Women.
- www.ihs-headache.org/ichd-guidelines 2018
- Tilgale B, Jeršova D. Cerebrāls infarkts jauniem pacientiem. Etioloģija. Doctus, 30.12.2016.
- Headache Pain, 2011; 12(3): 287-288. Published online 2011 Apr 24. Migraine triggered seizures and epilepsy triggered headache and migraine attacks: a need for re-assessment.
- Michele Viana, Grazia Sances, et al. The Journal of Headache and Pain, vol. 19, Article no: 77 (2018). Prolonged migraine aura: new insights from a prospective diary-aided study.
- Roldão Faleiro de Almeida, Inês Alice Teixeira Leão, et al. 2009 Apr. Migraine with Persistent Visual Aura: Response to Furosemide.
- www.j-stroke.org/journal/view.php
- J Headache Pain, 2011; 12(3): 289-294. Migralepsy, hemicrania epileptica, post-ictal headache and “ictal epileptic headache”: a proposal for terminology and classification revision.
- Neurology, 2000; 55: 1588-1589. Acetazolamide treatment for migraine aura status.
- Neurology, 2009; 72(21): 1864-1871. Migraine and cardiovascular disease.
- Curr Cardiol Rep, 2014; 16(9): 524. doi: 10.1007/s11886-014-0524-1. Migraine and the risk for stroke and cardiovascular disease.
- Updated: Oct 01, 2021. Jasvinder Chawla. Migraine Headache Treatment & Management.
- David B. Clemow, Kirk W. Johnson, et al. The Journal of Headache and Pain, 2020. Lasmiditan mechanism of action – review of a selective 5-HT1F agonist.
- Neurology, 2018; 91(24): e2222-e2232. Bernice Kuca, Stephen D. Silberstein, et al. Lasmiditan is an effective acute treatment for migraine. A phase 3 randomized study.
- Couch JR. Complexities of presentation and pathogenesis of migraine headache. In: Cady RK, Fox AW, eds. Treating the headache patient. Marcel Dekker, Inc., 1994: 15-40.
- Lancet Neurol, 2018; 17(2): 174-182. doi: 10.1016/S1474-4422(17)30435-0. Epub 2017 Dec 8. The pathophysiology of migraine: implications for clinical management.