Klīniskā gadījuma demonstrācijas mērķis — aktualizēt retu neiroloģisku sindromu, raksturot terapijas iespējas un efektivitāti un parādīt Latvijā veiktā pētījumā iegūtus datus par sindroma biežumu, klīnisko ainu, agrīnas diagnostikas un ārstēšanas nozīmi.
Klīniskais gadījums
Slimības anamnēze
Pusgadu veca meitene 26.08.2014. stacionēta plānveida izmeklēšanai ar sūdzībām par to, ka no 1.08.2014. vecāki novērojuši lēkmes, sākotnēji ar acu rotatorām kustībām (deviāciju) uz augšu, vēlāk sērijveidā ar pēkšņu roku un kāju fleksoru saliekšanos un propulsiju. Lēkmes ilgst apmēram 10 minūtes. Šādas lēkmju sērijas atkārtojas klasteros trīs reizes dienā. Vecāki novērojuši arī psihomotorās attīstības regresu. Bērns pārstājis smaidīt, apstājusies kustību aktivitāšu attīstība.
Citu slimību anamnēze
Bērns dzimis mātei 30 gadu vecumā, pirmajās dzemdībās. Pēc dzimšanas bērna vispārējais stāvoklis apmierinošs, fenotipiski — Dauna sindroma pazīmes. Dzīves 3. stundā novēroti tranzitori asins koagulācijas traucējumi, plaušu asiņošana, magnētiskās rezonanses (MR) izmeklējumā konstatēts plašs išēmisks insults ACM sinistra baseinā. Dinamikā bērna vispārējais stāvoklis uzlabojas. Trīs nedēļu vecumā vispārēji stabilā stāvoklī bērnu izraksta tālākai ambulatorai aprūpei.
Objektīvi
Vispārējais stāvoklis apmierinošs. Fenotips atbilst 21. hromosomas trisomijai. Skatienu nofiksē īslaicīgi, vada. Trakcijā galvu notur, bet viegls aksiāls hipotonuss. Vienlaikus salīdzinoši augstāks muskuļu tonuss labajā rokā, vērojama kustību asimetrija, labās rokas spastiska monoparēze. Meitene nepārveļas, vertikalizējot atbalsts uz kājām vājš.
26.08.2014.veic elektroencefalogrāfiju (EEG), kur konstatē hipsaritmiju, kas, miegam padziļinoties, kļūst fragmentēta. Stacionārā meitenei novēro sērijveida infantilo spazmu lēkmes. Starp spazmu sērijām pašsajūta laba.
Klīniskā diagnoze
Simptomātiska epilepsija, Vesta sindroms. Sekas pēc neonatāla išēmiska insulta ACM sinistra baseinā. (27.02.2014.) Labās rokas spastiska monoparēze. 21. hromosomas trisomija.
Tālākā slimības gaita
Sākta terapija ar vigabatrīnu (250 mg 2 × dienā). Stāvoklis dinamikā nemainās. 8.09.2014.veic MR galvai, kreisajā puslodē ACM baseinā konstatē smadzeņu vielas malāciju. Viduslīnija nedaudz nobīdīta pa kreisi. Kreisais laterālais vēderiņš platāks. Izvērtējot angiogrāfiju, kreisajā pusē ACM oklūzija, vāji vizualizējas kolaterāles. Palielināta vigabatrīna deva (250 mg no rīta un 375 mg vakarā, līdz 500 mg 2 × dienā). Tā kā infantilo spazmu lēkmes turpinās (8 mēnešu vecumā), papildus vigabatrīnam 500 mg 2 × dienā ordinēts prednizolons pēc starptautiskās vadlīnijās noteiktajām devām.
27.10.2014. veic EEG miegā: hipsaritmija, periodiski fragmentēta. Salīdzinot ar iepriekšējo EEG, bez uzlabojumiem. Pacientei izteiktas obstipācijas, ko ārstē ar Forlax, neirogēna urīnpūšļa disfunkcija un persistējoša urīnceļu infekcija, kas attiecīgi ārstēta ar Bactrim un Furamag, apsvērta uroseptiķu lietošana ilgstošai profilaksei.
Diētas maiņa
Meitene (10 mēnešu vecumā) stacionēta plānveida terapijai ar ketogēnu diētu. Vigabatrīna, glikokortikoīdu un to kombinācijas lietošana bez būtiska efekta. EEG saglabājas hipsaritmija. Stacionēšanas brīdī lēkmes vairāk nekā 10 × dienā. Pastāvīgi terapijā saņem vigabatrīnu 500 mg dienā. Ketogēno diētu sāk pierašanas režīmā: ketogēns uzturs 2 × dienā, mērot cukura un ketonu līmeni asinīs 2 × dienā (no rīta un vakarā), kā arī nepieciešamības gadījumā (ja bērns kļūst apātisks, sākas vemšana vai pastiprinās krampju lēkmes), vēlāk ketogēnā proporcija 2:1. Pirmajā nedēļā pēc ketogēnās diētas sākšanas lēkmes un hipsaritmija izzūd. Pie ketogēnās diētas proporcijas 2:1 ketonvielu līmenis 3—6 mmol/l, glikozes līmenis stabils. Meitenei papildus konstatē neirogēnu urīnpūšļa disfunkciju, hiperreflektīvu urīnpūsli, biežas urīnceļu infekcijas. Pēc uroloģiskajiem izmeklējumiem — urīnpūšļa katetrizācija 2 × dienā (māte apgūst, kā tas darāms).
Psihomotorā attīstība
Psihomotorā attīstība dinamikā progresē: priekšmetam seko, priekšmetu satver ar kreiso roku, ar labo pietur. Muskuļu tonuss nedaudz pazemināts. Labās puses ekstremitātēs neliela spastika. Galvas kontrole laba. Uz vēdera atbalsts uz elkoņiem. Bērns lalina.
Norādījumi izrakstoties
Precizē terapijas plānu: turpināt ketogēnu diētu pēc līdzšinējām receptēm, proporcija 2:1, pakāpeniski atcelt vigabatrīnu pēc šādas shēmas: 250 mg no rīta, 500 mg vakarā 1 nedēļu, 250 mg 2 × dienā 1 nedēļu, 250 mg vakarā 1 nedēļu, tad atcelt. Vienā no pēdējām kontroles EEG (26.05.2015.) miega struktūra saglabāta, pamatritma asimetrija — novājināta virs kreisās puslodes. Fokāla epileptiforma aktivitāte labajā puslodē fronto—centrāli un kreisajā puslodē temporo—okcipitāli. Klīniskā interpretācija: EEG atradē nespecifiskas kreisās puslodes disfunkcijas pazīmes, samērā nespecifiska fokāla epileptiforma aktivitāte. Neepileptiska miega mioklonija. Hipsaritmija izzudusi.
Komentē J. Strautmanis
Ņemot vērā pacientes ģenētisko slimību, pēcdzemdību grūto periodu ar komplikācijām, šajā gadījumā Vesta sindroma diagnostikas un terapijas shēmas izpildījums bijis profesionāls un dinamisks process. Vesta sindroma terapijas mērķis ir “visu vai neko” — lai bērnam būtu iespējama psihomotorā attīstība, jāreducē gan klīniskā, gan elektroencefalogrāfiskā aina, proti, spazmām jāizzūd un hipsaritmijai jādzēšas pilnīgi.
Ne vienmēr Vesta sindroms tiek atpazīts, ja tiek — iespējams, novēloti. Latvijā nereti diskriminē National Institute for Health and Clinical Excellence (NICE) vadlīnijās noteikto Vesta sindroma terapiju, kas bērna psihomotorās attīstības tālāko prognozi, iespējams, padara neatgriezeniski nelabvēlīgu.
Literatūras apskats
Infantilās spazmas (IS) jeb Vesta sindroms (VS) ir plaši lietots termins bērnu neiroloģijā, bet vēsturiskas detaļas zināmas ne katram. 1841. gadā V. Džeims Vests, ģimenes ārsts no Tonbridžas, nosūtīja gadījuma ziņojumu medicīniskā žurnāla Lancet redaktoram, lai kolēģu uzmanību pievērstu ļoti retām un īpatnējām zīdaiņu konvulsijām, vēstulē aprakstot gan pacienta objektīvu atradi, gan izmisuša tēva izjūtas par savu slimo bērnu.
Definīcija
Vesta sindroms ir no vecuma atkarīgs multietioloģisks ļaundabīgs epileptisks sindroms, ko raksturo klasiskā triāde: epileptiskas spazmas, EEG izmaiņas — hips-aritmija, psihomotorās attīstības regress — iemaņu zaudēšana. Hipsaritmija ir haotiska cerebrāla aktivitāte, kam EEG raksturīgi asinhroni, aritmiski, plašas amplitūdas lēni viļņi, ko caurvij multifokāli asi pīķi. Epileptiskās spazmas ir īslaicīgas aksiālas kustības, aptuveni 0,2—2 sekundes garas, biežāk fleksoras nekā ekstensoras. Sindroma sastopamība 2,9—4,5 gadījumi uz 100 000 dzīvi dzimušiem, kura pēdējos 30 gados nav mainījusies. Latvijā ik gadu atklāj 2—2,5 jaunus Vesta sindroma gadījumus. Sindroms izpaužas 3—9 mēnešu vecumā, bet var sākties arī neilgi pēc dzimšanas un līdz pat piecu gadu vecumam.
Etioloģija
Apkopojot daudzās valstīs veiktu pētījumu rezultātus, var secināt, ka VS biežākais etioloģiskais faktors ir centrālās nervu sistēmas strukturāls bojājums (60—90 % gadījumu), bet simptomātiska VS gadījumā 7—25 % pamatslimība ir tuberozā skleroze. Izdala simptomātisku jeb zināmas etioloģijas un idiopātisku Vesta sindromu. ILAE pēdējie ieteikumi attiecas uz terminoloģijas korekcjām: “idiopātisks, simptomātisks, kriptogēns” attiecīgi aizstāt ar “ģenētisks, strukturāli metabolisks, nezināmas izcelsmes”VS. Zināmas etioloģijas VS var vēl klasificēt šādi: prenatāls, perinatāls, postnatāls (klasifikācija atspoguļota 1. tabulā).
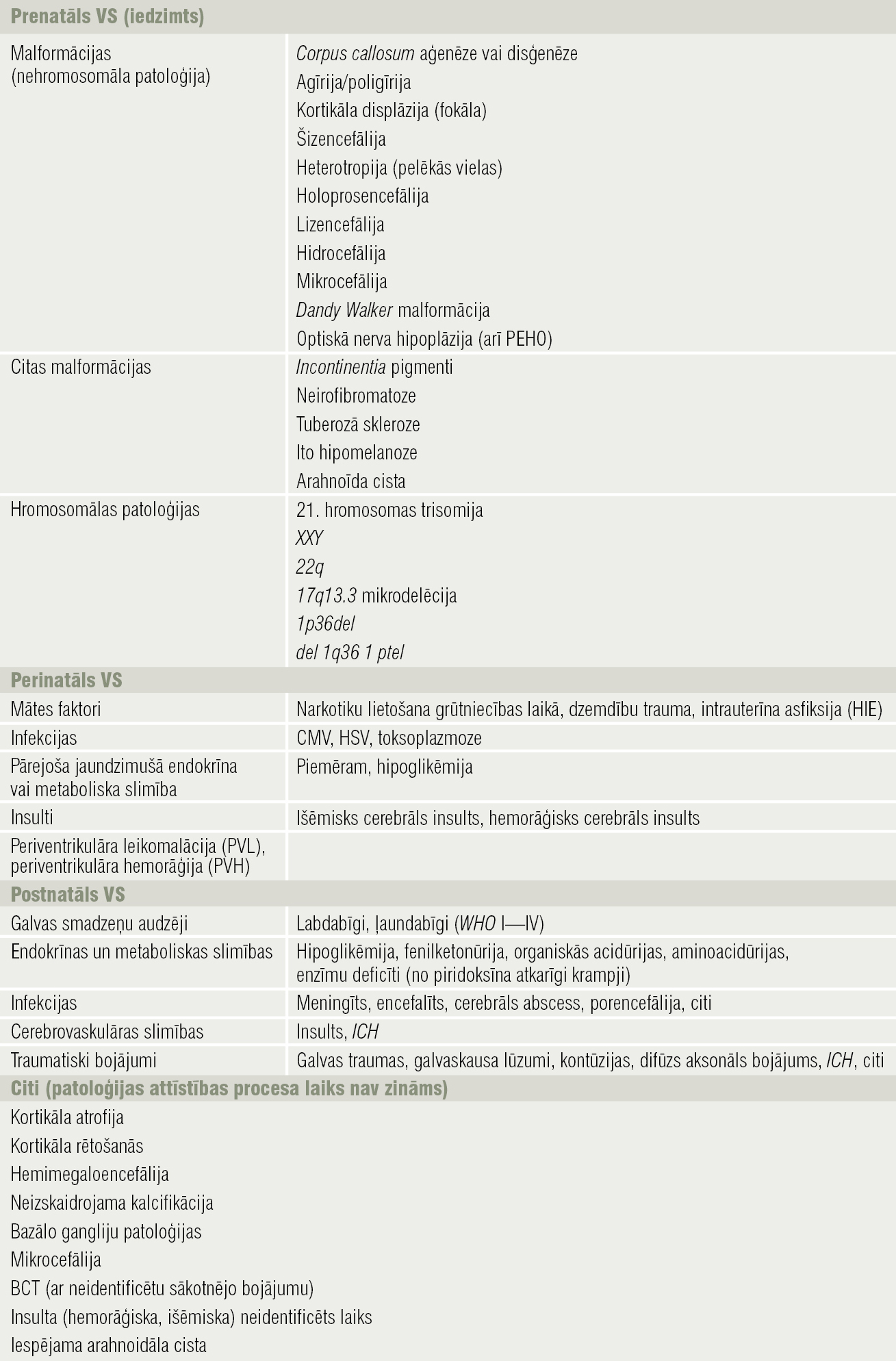

1. tabula
Zināmas etioloģijas Vesta sindroma klasifikācija
Vesta sindroma diferenciāldiagnostika
Diemžēl daudziem pacientiem diagnozi nosaka novēloti, bieži infantilo spazmu tipiskās fleksorās noraustīšanās, pēc kurām mēdz sekot bērna raudāšana, asociē ar zarnu kolikām, gastrointestinālo refluksu, invagināciju, kā arī ar citiem stāvokļiem, piemēram:
- labdabīgā zīdaiņu miokloniskā epilepsija — proti, klastera tipa neepileptiskas spazmas, zīdaiņu EEG atrade un psihomotorā attīstība ir vecumam atbilstīga;
- labdabīgs neepileptisks zīdaiņu mioklonuss — atgādina epileptiskās spazmas, taču PMA un EEG atrade normāla;
- hiperekpleksija — neiroloģiski traucējumi, kas klīniski izpaužas kā hipertonija un pēkšņa hiperreflektora startle tipa reakcija uz taktiliem vai akustiskiem stimuliem;
- toniskas lēkmes;
- Sandifera sindroms — spazmatiska torsionāla distonija ar opistotoniskām un rigidām ķermeņa pozām, tās var būt paroksizmālas;
-
Jactatio capitis nocturna — labdabīga galvas atkārtota noraustīšana vai atmešana iemiegot;
-
spasmus nutans — reta oftalmoloģiska slimība, ko raksturo klīniskā triāde: nistagms, galvas noliekšana— pamāšana, torticollis;
- biotīna (B7) deficīts un neketotiska hiperglikēmija — var būt periodiskas spazmas, kas saistītas ar fokālu vai multifokālu epilepsiju, EEG — periodiski kompleksi ar lēniem viļņiem, ko caurvij paroksizmāla ātra aktivitāte;
- agrīnas elpas aiztures lēkmes — var sekot distoniskas pozas un miokloniska noraustīšanās;
- PEHO sindroms (progresējoša encefalopātija ar tūsku, hipsaritmiju un optisko nervu atrofiju) — rets neirodeģeneratīvs sindroms, kas var izpausties ar hipotoniju, gausu zīšanu, epileptiskām spazmām līdzīgām kustībām, patoloģiskām okulārām opscilopsijām, redzes zudumu (neiroloģiski izmeklējot — nesekos priekšmetam ar acīm), psihomotorās attīstības aizturi, tūsku — izteiktāku ekstremitātēs;
- Moro reflekss — var būt līdzīgs infantilām spazmām, taču Moro reflekss neatkārtojas vairākas reizes, bet infantilās spazmas mēdz būt klasteros; Moro refleksu var izprovocēt ar skaļu skaņu.
Ārstēšana
VS pirmās līnijas medikamentu izvēle atkarīga no etioloģiskā faktora, piemēram, vigabatrīns efektīvāks ir tuberozās sklerozes, kortikālas displāzijas, simptomātiska VS gadījumā, bet terapija ar glikokortikoīdiem (AKTH, prednizolonu) — idiopātiska vai išēmisku pārmaiņu radīta VS gadījumā. Epileptisko spazmu kontrole un prognoze atkarīga galvenokārt no VS etioloģijas.
Par glikokortikoīdu devām nav vienota nolikuma, piemēram, 2 nedēļas prednizolonu lietot mazās devās (2 mg/kg/dienā) un tikpat ilgi lielās devās (4—8 mg/kg/dienā), — shēmām pierādīts vienlīdzīgs efekts (75 % epileptisko spazmu kontrole). Kušingoīda tipa blaknes novēro pat 100 % gadījumu, kas dažreiz ir smagas, terapijas letalitāte mērojama 2—5 % robežās.
Vigabatrīns atzīts pirms aptuveni 20 gadiem, kad pētījuma rezultāti rādīja 43—70 % pilnīgu epileptisko spazmu kontroli iepriekš refraktārām infantilajām spazmām, drīz pēc tam tas kļuva par pirmās izvēles medikamentu monoterapijā. Pētījumā par vigabatrīna dozēšanu izrādījās, ka lielu vigabatrīna devu (100—150 mg/kg/dienā) lietošana salīdzinājumā ar mazākām (≤ 40 mg/kg/dienā) divās nedēļās dod labākus rezultātus. Vigabatrīna nozīmīgākā blakne ir retināla toksicitāte, kam var sekot perifēro redzes lauku funkciju zudums. Blaknes saistītas ar vigabatrīna kumulatīvo efektu: tas attīsta taurīna deficītu un veicina fototoksicitāti. Perifēro redzes lauku funkcijas zudumu nenovēro bērniem, kas medikamentu saņēmuši nepilnus 15 mēnešus. Reftraktāru infantilo spazmu gadījumos var apsvērt ketogēno diētu. Antiepileptiskie medikamenti tiek uzskatīti par neefektīviem, tas pierādīts atvērtos klīniskajos pētījumos, piemēram, valproāts un klonazepāms kontrolē apmēram 25—30 % IS gadījumu, bet epileptisko spazmu atkārtotas atsākšanās varbūtība ir ļoti liela. IS pasliktināšanās novērota, lietojot karbamazepīnu. Ilgtermiņa prognoze Vesta sindroma pacientiem ir neskaidra un atkarīga no sindroma etioloģijas. Pēdējās NICE vadlīnijās minēts, ka nepieciešams pētniecisks ieguldījums VS terapijas efektivitātes izvērtēšanā, jo pašlaik nav precīzi zināms, vai agrīna un adekvāta ārstēšana uzlabo Vesta sindroma pacientu prognozi.
Pētījums: Vesta sindroms Latvijā
Latvijā veikts aprakstošs retrospektīvi perspektīvs pētījums, kurā izmantoti BKUS “Torņkalns” pacientu dati no 2004. gada janvāra līdz 2015. gada janvārim. Pētījumā iekļauti dati par 28 (27 simptomātiskiem, 1 idiopātisku) Vesta sindroma pacientiem — tikai par tiem, kam VS izpaudās ar raksturīgo triādi (epileptiskas spazmas, EEG izmaiņas — hipsaritmija, psihomotorās attīstības regress — iemaņu zaudēšana).
Rezultāti
Pacientu vidējais vecums VS izpausmes brīdī 6,2 mēneši (jaunākais pacients — 7 dienas vecs, vecākais — 1 gadu 8 mēnešus vecs). No visiem VS pacientiem BCT attīstījusies 25 % gadījumu, no tiem spastiskā forma — 85 %, kombinētā — 15 %. Etioloģiskie faktori parādīti 2. tabulā.
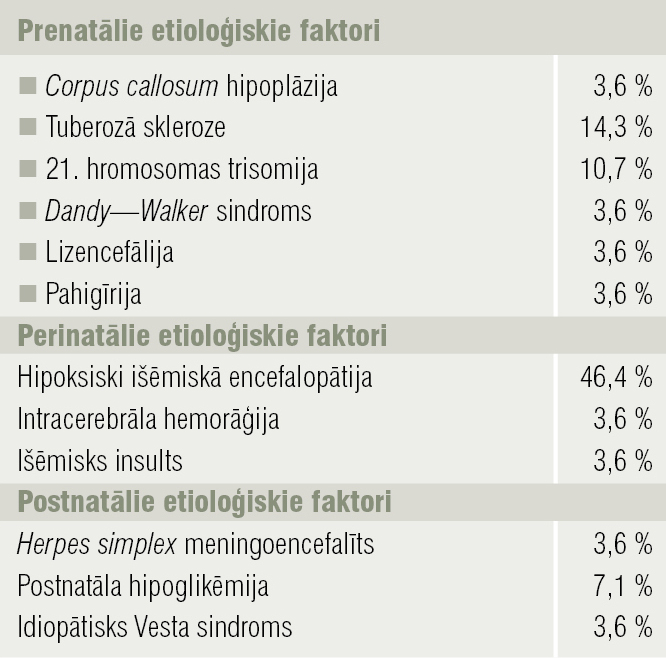

2. tabula
Simptomātiska Vesta sindroma etioloģiskie faktori Latvijā
Desmit gadu laikā vismaz 46,4 % ārstēto VS pacientu kā pirmā izvēles terapija ordinēta tāda, kas pasaulē atzīta kā neefektīva tieši šā sindroma gadījumā (valproātskābe, fenobarbitāls, levetiracetāms). Zināms, ka 1—8 mēnešos 25 % pacientu medikācija mainīta uz vigabatrīnu, 3,6 % uz prednizolonu, 17,9 % uz citu antiepileptisko medikamentu, 53,5 % tālākā ārstēšanas taktika nav zināma. 7,2 % tika lietota ketogēnā diēta, abiem pacientiem klīniska uzlabošanās, taču blakņu un līdzestības trūkuma dēļ viens pacients terapiju pārtrauca, otrs (šā klīniskā gadījuma pacients)veiksmīgi turpina.
VS agrīnai diagnostikai un ārstēšanai ir nozīme, arī šajā pētījumā trim pacientiem (10,8 %) pēdējā EEG atbilst vecuma normai, hipsaritmiju nomainījušas nespecifiskas ģeneralizētas un fokālas izmaiņas, kas nodrošina normālu vai labāku bērna psihomotoro attīstību. Hipsaritmijas izzušanas laiks pēc medikācijas sākšanas izvērtēts 11 pacientiem, īsākais periods — 3 nedēļas, ilgākais — 15 mēneši.
Noslēgumā
Pētījuma rezultātu statistisko ticamību ierobežoja nelielais pacientu skaits, taču iegūtā informācija jau tagad ļauj izdarīt secinājumus, kas ar laiku palīdzēs VS diagnosticēt un ārstēt veiksmīgāk nekā līdz šim.