Idiopātiska pulmonāla fibroze (IPF) ir viena no idiopātiskām intersticiālām pneimonijām, pie kurām pieder vēl septiņas citas nozoloģiskas formas, bet IPF ir visbiežāk sastopamā un prognostiski vissmagākā forma. Pēc definīcijas IPF ir nezināmas etioloģijas progresējoša intersticiālas plaušu slimības forma, ko raksturo īpašu klīnisko, radioloģisko un histoloģisko pazīmju kopums. Šoreiz klīniskajā gadījumā - paciente ar sarežģītu diagnozi. Demonstrējot šo klīnisko gadījumu, diferenciāldiagnozē tika minēta arī sarkoidoze, jo bija paaugstināta angiotenzīna konvertāze, kas var būt paaugstināta arī dažu aknu slimību gadījumā.
Klīniskā gadījuma demonstrācija
(Dr. Marija Tokmanceva)
Anamnēze
Paciente, 51 gadu veca, 2009. gada rudenī akūti stacionēta ar ģimenes ārsta nosūtījumu progresējoša elpas trūkuma dēļ, kas parādās minimālas fiziskas slodzes laikā. Ģimenes ārsta nosūtīšanas diagnozes - idiopātiska plaušu fibroze, elpošanas mazspēja. Izteiktas aizdomas par sarkoidozi, jo, ambulatori izmeklējot, konstatē paaugstinātu angiotenzīna konvertāzi - 140,83 U/l (N 15-70).
Slimības anamnēze
Pacientei elpas trūkums ir jau apmēram piecus gadus, bet pēdējā gada laikā tas izteikti progresē, parādās klepus ar bālganām krēpām. Jau 2008. gadā paciente izmeklēta P. Stradiņa KUS 14. nodaļā, veikta torakoskopija ar biopsiju, plaušu datortomogrāfija, noteikta diagnoze - difūza plaušu fibroze, alveolīts. Biopsijas materiāla histoloģiska izmeklēšana: intersticiāla plaušu patoloģija ar difūzu, samērā izteiktu alveolu starpsienu fibrozi, alveolārā epitēlija hipoplāziju. Morfoloģiskā aina nav raksturīga alveolītam, kaut arī to pilnība neizslēdz.
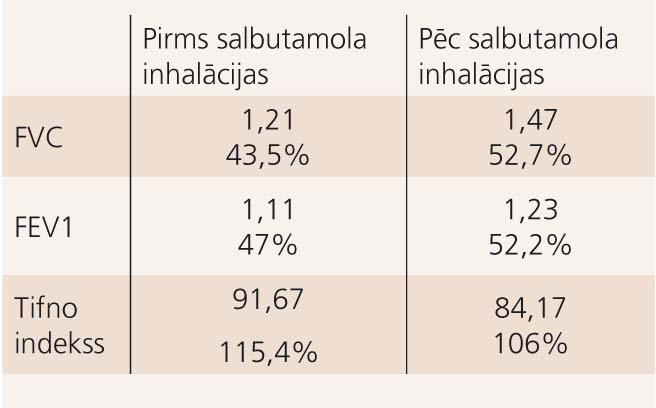

Tabula
Bronhodilatācijas testa rezultāti
Dzīves anamnēze
Dzīves anamnēzē paciente strādājusi ar karstu metālu, bijusi smēķētāja, pirms gada smēķēšanu atmetusi. Slimo ar hronisku autoimūnu tireoidītu, lieto L-thyroxin 50 µg reizi dienā p/o.
Objektīvā izmeklēšana
Objektīvi vispārējais stāvoklis vērtējams kā vidēji smags. Āda pabāla, sausa, silta. Palielinātus perifēros limfmezglus nepalpē. Perifēru tūsku nav. TA 130/80 mm/Hg, sirdsdarbība paātrināta, 110 x min. Ir tahipnoja 26 x min. Elpošana abpusēji vezikulāra. Abu plaušu lejasdaļā auskultē krepitāciju ieelpas beigu fāzē. SpO2 - 93%. Vēders, virspusēji palpējot, - mīksts, nesāpīgs. Palielinātas aknas vai liesu nepalpē. Zarnu peristaltika dzirdama. Nieru rajons apklauvējot nesāpīgs.
Darba diagnoze: idiopātiska plaušu fibroze ar smagas pakāpes elpošanas mazspēju. Sarkoidoze ? Hronisks autoimūns tireoidīts.
Laboratorie un instrumentālie izmeklējumi:
- asinsaina: ER- 4,15*1012/l¯, HGB- 110g/l¯, EGĀ- 57mm/h;
- bioķīmiskā analīze: AlAT- 44U/l, AsAT- 71U/l, albumīns- 27g/l¯. Seruma proteīnu elektroforēze: albumīns 45,5%¯, gglobulīns 30,4% ;
- bronhodilatācijas tests: izteikti samazināta gāzu difūzijas kapacitāte;
- EKG: sinusa ritms 85xmin. Nespecifiskas ST, T izmaiņas.
Paciente 2009. gada 24. septembrī tiek pārvesta uz 6. torakālās ķirurģijas nodaļu, kur veikta video asistētā torakoskopija ar kreisās plaušas marginālu lingulas rezekciju un starpdaivu limfmezgla biopsiju.
Patohistoloģiskā izmeklēšana: limfmezglā multiplas sīkas, ieapaļas histiocītu granulomas ar sīkfokālu fibrozēšanos. Plaušu alveolārā arhitektūra deformēta. Intersticijā fibroze, mērena limfocītu un plazmocītu infiltrācija. Vietām alveolas deformētas, izveidojot "bišu šūnas". Saistaudu briedums intersticijā dažāds. Slēdziens: nespecifiska intersticiāla pneimonija ar fibrozes veidošanos, temporālas nehomogenitātes un hroniskas norises pazīmēm. Morfoloģiskā aina var atbilst fibrozējošam alveolītam.
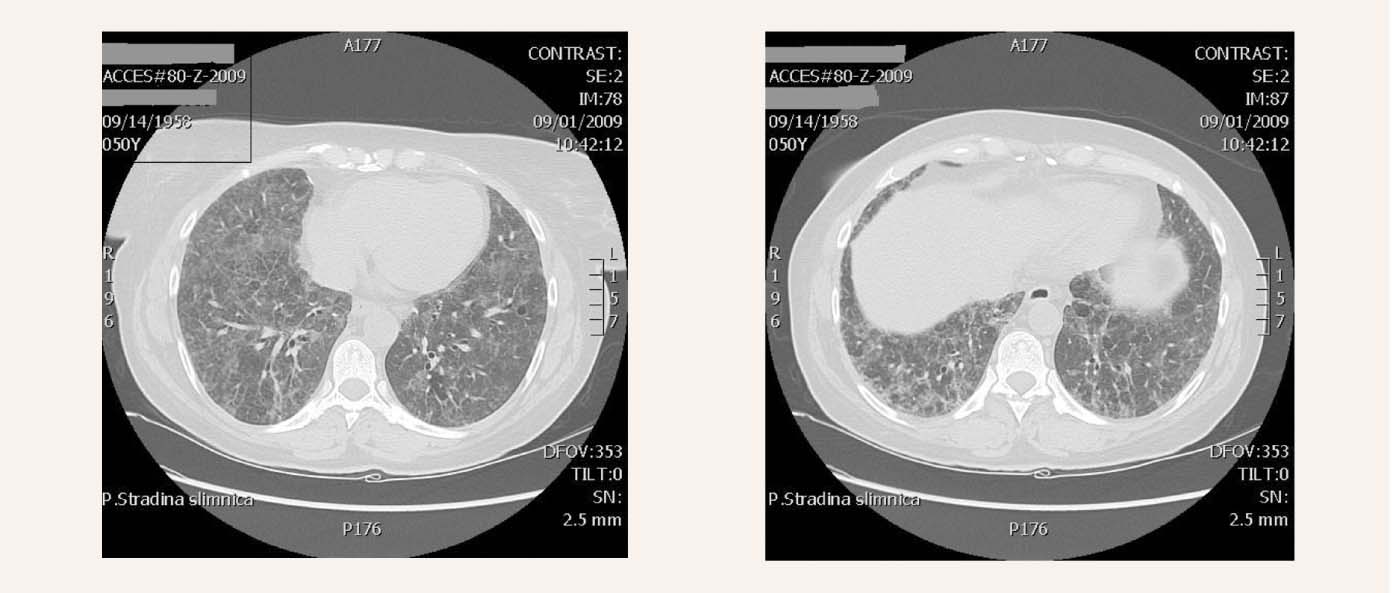

1. attēls
Datortomogrāfija plaušām – difūzas fibrotiska rakstura pārmaiņas ar šūnainību, diezgan izteiktu matstikla aizēnojumu
Bronhu dilatācijas tests - slēdziens: smagas pakāpes restriktīva tipa ventilācijas funkcijas mazspēja. Bronhodilatācijas testa rezultātus skatiet tabulā.
Datortomogrāfija plaušām (2009. gada 1. septembrī un 2009. gada 26. oktobrī, skat. 1. un 2. attēlu). 2009. gada 1. septembrī konstatē difūzas fibrotiska rakstura pārmaiņas ar šūnainību, diezgan izteiktu matstikla aizēnojumu, kas varētu liecināt par to, ka process ir akūtā stadijā. 2009. gada 26. oktobrī - mazinās matstikla aizēnojums, var bazāli labāk redzēt šūnainību.
Galīgā klīniskā diagnoze
- Idiopātiska plaušu fibroze.
- Smaga restriktīva plaušu ventilācijas funkcijas mazspēja.
- Hronisks, autoimūns tireoidīts.
- Normohroma anēmija.
Saņemtā terapija
2009. gada 28. septembrī sāk tab. Medroli 48 mg/d p/o (rekomendē turpināt ambulatori 1 mēnesi), tab. Quamateli 20 mg x 2 p/ o, tab. Verapamili 80 mg x 2 p/ o, tab. Imdur 60 mg x 1 p/o, sol. Amoxiclavi 1,2 x 3 i/v, sol. Euphyllini 2,4% 5,0 x 2 i/v.
2009. gada 1. oktobrī apmierinošā stāvoklī paciente tiek izrakstīta tālākai ambulatorai terapijai ģimenes ārsta un pulmonologa uzraudzībā. Paciente nav darba spējīga, tādējādi nosūtāma uz VDEĀK.
Slimības gaita dinamikā
Nākamā stacionēšanas reize ir pēc 5 mēnešiem - 2010. gada 14. februārī, kad paciente stacionēta akūtā kārtā ar sūdzībām par izteiktu elpas trūkumu, sliktu dūšu. Atsākta terapija ar Medrol 32 mg/dn p/o, ko paciente pārtraukusi lietot pirms mēneša. Ir zināms, ka stacionēšanas dienā paciente lietojusi arī alkoholu.
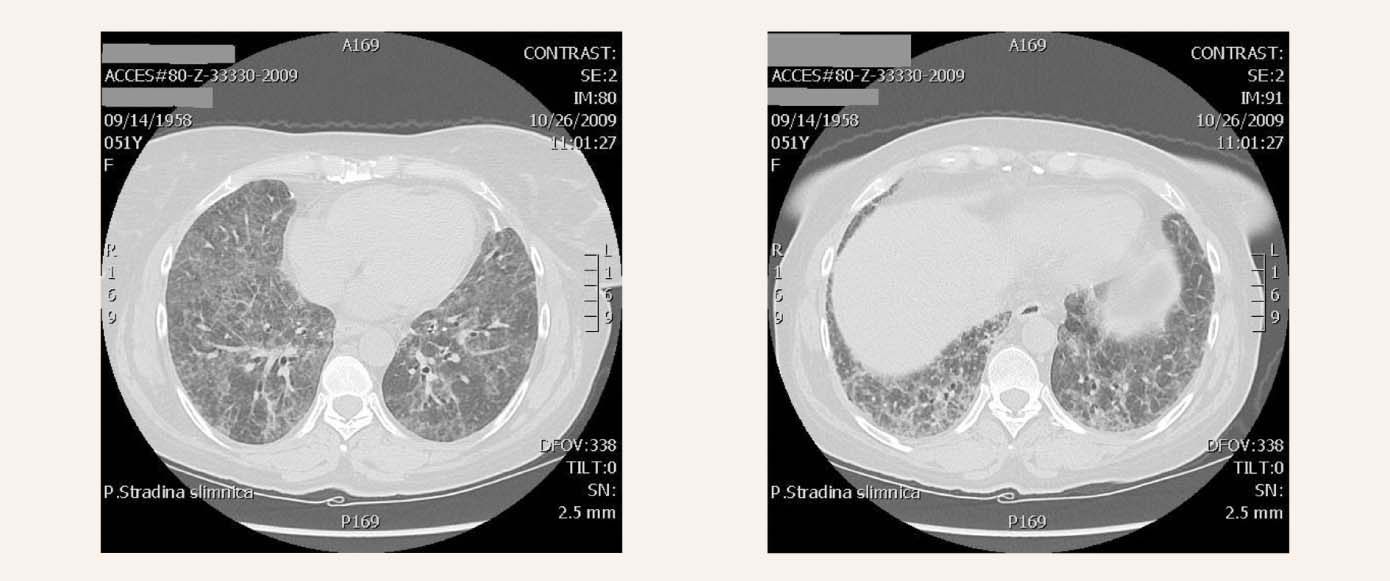

2. attēls
Datortomogrāfija plaušām – mazinās matstikla aizēnojums, var bazāli labāk redzēt šūnainību
Objektīvā izmeklēšana
Vispārējais stāvoklis ir relatīvi apmierinošs, TA 120/80 mm/Hg, pulss 92 x min., ritmisks. Perifēro tūsku nav. Ir tahipnoja līdz 26 x min. Auskultējot - abpusēji krepitācija ieelpas beigās, kreisajā pusē elpošana bazāli novājināta. Veic O2 inhalācijas ar masku. Vēders palpatori mīksts, nesāpīgs. Peristaltika dzirdama. Mēle balta, aplikta, valga.
Laboratorie rādītāji:
- asinsaina: ER 5,25*1012/l, HGB- 105g/l¯. Koagulogramma- protrombīna indekss 64,2%¯, fibrinogēns 1,5g/l¯, D-dimēri 45µg/l. Etanols asinīs- 3,81‰;
- Rtg plaušām- pēc Rtg ainas visticamāk jādomā par alveolītu;
- EKG- sinusa bradikardija 55xmin. Labā ātrija hipertrofijas pazīmes. Išēmiskas pazīmes priekšējā sienā?
- TSH- 0,123mlU/ml¯, fT4- 0,69ng/dl¯, fT3- 1,16pg/ml¯.
- DT plaušām un videnei: sākot jau no plaušu galotnes zonām, pieaugot bazāli, vērojamas difūzas, škiedrainas, fibrotiska rakstura pārmaiņas ar šūnainību. Vērojams arī viegls matstikla aizēnojums.
Secinājums: fibrozējošs alveolīts. Salīdzinot ar izmeklējumu 2009. gada 26. oktobrī, bez būtiskas dinamikas.
Bronhu dilatācijas tests - vieglas pakāpes restriktīva tipa ventilācijas funkcijas nepietiekamība. Šis izmeklējums liecina, ka Medroli terapijas kurss bija devis efektu.
Saņemtā terapija nodaļā
Sol. Medroli 500 mg i/v x 3, tab. Medroli 48 mg x 1 p/o, kaps. Omeprazoli 20 mg x 2 p/o, tab. Spirix 25 mg x 1 p/o, tab. L-Thyroxin 75 µg x 1 p/o, sol. Ceftriaxoni 1,0 i/v x 1.
Jau četras dienas pēc stacionēšanas un sāktās terapijas pacientes stāvoklis uzlabojas, ir pozitīva dinamika. Paciente izrakstīta no stacionāra pēc pašas vēlēšanās. Terapijā rekomendēts turpināt tab. Medroli 32 mg x 1 p/o. Tālāka uzraudzība ambulatori pie ģimenes ārsta.
Diagnoze
- Idiopātiska plaušu fibroze, nestabila remisija.
- Restriktīva tipa plaušu ventilācijas funkcijas mazspējaI.
- Hronisks autoimūns tireoidīts.
Diskusija
Prof. V. Pīrāgs: Interesanti, kas ar šo pacienti noticis pēdējā gada laikā. Ja mēs diagnozē rakstām "idiopātisks", tad īstenībā iešifrējam to, ka mēs nezinām, kas tā īsti ir par slimību, bet tikai redzam, kā tā izpaužas. Divas reizes veikta plaušu audu morfoloģiskā izmeklēšana, un abās reizēs ir neskaidra atbilde. Protams, šai pacientei ir daudzi riska faktori, ieskaitot smēķēšanu, darbu ar metāliem utt. Bet limfmezglu biopsijā bija daudz histiocītu, un viņai ir sekundāra hipotireoze. Tas varētu liecināt par to, ka histiocītiem līdzīgas šūnas var būt infiltrējušas arī hipofīzi. Tad to sauc par histiocitozi X. Vai jums domas par šādu diagnozi neradās?
Doc. V. Šiliņš: Par histiocitozi X domas neradās, jo radioloģiskā diagnoze bija idiopātiska pulmonāla fibroze. Bet bija diferenciāldiagnoze ar sarkoidozi. Idiopātiska pulmonāla fibroze attīstās lēnām. Ja mēs diferenciāldiagnozē izvirzām histiocitozi X, tad mums vajadzētu bronhoskopiju ar bronhiālo lavāžu. Taču laboratorija mums pārāk bieži nedod smalku, diferencētu slēdzienu.
Prof. J. Pokrotnieks: Morfoloģija, histoloģija tomēr ir zelta standarts. Pārējais, ko jūs minējāt, īstenībā tam neatbilst.
Dr. Z. Kravale: Jā, diagnozes apstiprināšanai vajadzētu veikt histoloģisko verifikāciju. Bet, kā jūs redzējāt, arī tā nav absolūta, un pat pacientiem, kam histoloģiski tiek konstatēta nespecifiskā intersticiālā pneimonija, ir jāatbilst zināmiem kritērijiem, lai šī diagnoze būtu droša.
Doc. V. Šiliņš: Par zelta standartu - histoloģiju. Jā, tā grāmatās raksta, bet klīniski dažreiz ir pavisam citādi. Man ir bijusi paciente, kurai pēc grūtniecības radiologs raksta pārliecinošu slēdzienu - limfoleiomiomatoze, bet histologs - sarkoidoze. Vēl gribu uzsvērt, ka mēs kā akūtās palīdzības slimnīca varam mēģināt maksimāli strauji noņemt šo izteikto elpas trūkumu, bet pārējais faktiski paliek uz ambulatorās medicīnas un dienas stacionāra rēķina, kur šī paciente jāizmeklē detalizētāk un galvenais - jākontrolē. Šai pacientu grupai terapijā ir divas medikamentu grupas - glikokortikoīdi un imūnsupresanti. Literatūrā aprakstītas dažādas devas, terapijas ilgums. Mēs parasti ordinējam 48 mg kā maksimālo devu, ko cenšamies iespējami mazināt, kad redzam, ka gāzu difūzija turas pieņemamās robežās. Bet, ja nav terapijas efekta ar glikokortiokoīdiem, tad dažreiz kombinējam ar imūnsupresantiem. Arī šeit ir ļoti dažādas shēmas, pēc kurām šie pacienti tiek ārstēti. Taču jāatceras, ka glikēmijas līmeņa izmaiņas, svara izmaiņas, iespējams, arī aterosklerozes progress - tas viss ir mūsu terapijas blakusefekts. Šajā ziņā šī slimnieku grupa mums ir un paliek problemātiska, jo, turpinot ārstēties, ambulatori tas prasa daudz darba, laika un piedomāšanas par šo cilvēku.
Prof. V. Pīrāgs: Man ir interesanti vērot, kā dažādas iekšķīgo slimību apakšspecialitātes tiek galā ar šīm diagnozēm, kas tiešām ieiet tajā pelēkajā zonā, kur mēs īsti nezinām, kas tas ir, bet zinām, ka tas nav lipīgs. Protams, medicīnā ir progress un pirms 100 gadiem 70% slimību bija idiopātiskas, respektīvi, no grieķu valodas - ar savdabīgu patoģenēzi. Kāpēc mēs esam sasnieguši šo progresu? Domāju, galvenokārt tiešām pateicoties patologiem un mūsu spējai molekulārā līmenī diagnozi noteikt un arī ārstēt. Šajā gadījumā par ārstēšanu ir skaidrs, ka glikokortikoīdu terapijai bija efekts. Arī granulomatozo slimību gadījumos, kas, manuprāt, bija galvenā diferenciāldiagnoze, glikokortikoīdiem ir labs terapijas efekts. Varbūt pietrūka azatioprīna?
Teorētiskā daļa
(Dr. Zane Kravale)
Sinonīmi
Idiopātiskas pulmonālas fibrozes (IPF) sinonīmi: alveolokapilārais bloks, kriptogēns fibrozējošs alveolīts, difūzs fibrozējošs alveolīts, Hamman-Rich sindroms, intersticiāla difūza pulmonāla fibroze.
Incidence un riska faktori
10,7 gadījumi vīriešiem : 7,4 gadījumiem sievietēm uz 100 000 iedzīvotāju. Dažādās valstīs šie dati atšķiras. Nav datu par pārliecinošu prevalenci pilsētu vai lauku iedzīvotājiem, kā arī noteiktu rasu pārstāvjiem. Saslimšanas risku paaugstina smēķēšana, antidepresantu lietošana, GERS, saskarsme ar metāla vai koka putekļiem, vīrusi - EBV, gripa, paragripa, CMV, HCV, HIV-1, HSV, baktērijas: legionellas, mikoplazmas.
Ir aprakstīta arī ģimenes IPF ar šādām pazīmēm: IPF vismaz diviem pirmās pakāpes radiniekiem (diagnoze apstiprināta histoloģiski), iespējama slimības attīstība agrākā vecumā, plaušaudu iekaisuma pazīmes var konstatēt arī tiem ģimenes locekļiem, kas ar IPF neslimo. Ģimenes IPF ir 0,5-2% no visiem IPF gadījumiem.
Patoģenēzes teorijas
Patoģenēze nav precīzi zināma, bet ir izvirzītas šādas teorijas:
- lai saglabātu pareizu plaušaudu uzbūvi, nozīme ir alveolo-kapilārās barjeras- bazālās membrānas integritātei;
- šīs bazālās membrānas reepitelizācijas; reendotelizācijas traucējumu dēļ rodas patoloģiskas fibrozes;
- TGF-b ir svarīga nozīme, tomēr ar to vien nepietiek, lai attīstītos plaušu fibroze;
- parastas intersticiālas pneimonijas (UIP) attīstībā nozīme ir persistējošiem antigēniem;
- plaušu fibrozes attīstība ir saistīta ar epiteliālu-mezenhimālu transformāciju un asinsrades šūnām, kas no kaulu smadzenēm migrē uz plaušām.
Diagnostika
IPF diagnoze uzskatāma par drošu, ja histoloģiskajā preparātā, kas iegūts videotorakoskopiski vai atvērtas plaušu biopsijas ceļā, tiek konstatēta parasta intersticiāla pneimonija (UIP) un:
- tiek izslēgti citi zināmi iemesli, kā medikamentu toksicitāte, vides faktori un kolagenozes, kas var izraisīt intersticiālu plaušu saslimšanu;
- izmainīti plaušu funkcionālie izmeklējumi, kas var norādīt uz restriktīva tipa izmaiņām (samazināta VC, kā arī palielināta attiecība starp FEV1/FVC un/vai izmainīta gāzu maiņa (palielināts AaPO2 mierā vai slodzes laikā vai samazināts DLCO);
- raksturīgas izmaiņas datortomogrāfijā.
Bez histoloģiskās apstiprināšanas IPF diagnoze paliek apšaubāma; tomēr, ja pacients bez imūnsupresijas atbilst četriem lielajiem un vismaz trim no četriem mazajiem kritērijiem, tad diagnozi var uzskatīt par drošu.
Lielie kritēriji:
- citu intersticiālas plaušu slimības etioloģisko faktoru izslēgšana, kā, piemēram, toksisku medikamentu lietošana, vides faktoru ietekme un saslimšana ar kolagenozēm;
- izmainīti plaušu funkcionālie izmeklējumi, kas var norādīt uz restriktīva tipa izmaiņām;
- datortomogrāfiski atrod abpusējas bazālas šķiedrainas izmaiņas ar minimālām matstikla izmaiņām;
- transbronhiālā plaušu biopsija vai bronhoalveolārā lavāža (BAL) neapstiprina citu diagnozi.
Mazie kritēriji:
- pacienta vecums virs 50gadiem;
- pakāpeniski sākusies citādi neizskaidrojama aizdusa fiziskas slodzes laikā;
- slimības ilgums ≥3mēnešiem;
- abpusēji bazāli trokšņi ieelpā (sausi vai "Velkro" tipa).
Diferenciāldiagnoze
Azbestozes, hroniska aspirācija, radiācijas pneimonīts, hronisks hipersensitivitātes pneimonīts, iedzimtas slimības (tuberozā skleroze-limfangioleiomiomatoze) un citas intersticiālo plaušu slimību formas u.c. Tādējādi šo diagnozi 100% konstatēt ir ļoti grūti.
Sūdzības un anamnēze
Galvenā simptomātika ir sauss, mokošs klepus, aizdusa fiziskas slodzes laikā, simptomi bieži ilgāk nekā 6 mēnešus. Parasti šie pacienti ir ap 60 gadu veci, kad šie simptomi tiek saistīti ar kardioloģiskām vai citām pulmonoloģiskām saslimšanām, jo nereti šiem pacientiem ir hroniska obstruktīva plaušu slimība, viņi ir arī smēķētāji. Iespējami arī sistēmiski simptomi, kā svara zudums, subfebrīla temperatūra, artralģijas, mialģijas.
Svarīgi izvērtēt pacienta dzīves un darba apstākļus, saskarsmi ar toksiskām vielām (azbests, silīcijs), medikamentu lietošanu (amiodarons, nitrofurantoīns, bleomicīns), reimatoloģisku slimību anamnēzē, kas var radīt sekundāru pulmonālu fibrozi.
Fizikālā izmeklēšana
80% pacientu auskultē sausus "Velkro" tipa trokšņus ieelpas beigās. Sākotnēji trokšņus auskultē bazālajās daļās, vēlāk tie ascendē, 25-50% pacientu atrod bungvālīšu pirkstus, tālu progresējošas slimības gadījumā atrod cianozi, cor pulmonale, labā kambara pārslodzi, akcentētu P pulmonale, perifēru tūsku.
Laboratorie izmeklējumi
Galvenokārt kalpo, lai izslēgtu citas diagnozes. Līdz 30% šo pacientu atrod paaugstinātu ANA un RF titru, tomēr ne pārāk augstos titros, jo tas liecinās par citu diagnozi.
Plaušu funkcionālie testi
Spirogrāfiski parasti tiek atrastas norādes par restriktīva tipa ventilācijas funkcijas traucējumiem, ko raksturo samazināta kopējā plaušu kapacitāte (TLC), funkcionālā reziduālā kapacitāte (FRC) un atlieku tilpums (RV), kā arī FEV1 un FVC. Difūzijas kapacitātes mērījumi norāda uz samazinātu gāzu difūzijas spēju. Gāzu difūzijas spēju mazināšanās var apsteigt plaušu tilpuma izmaiņas.
Asins gāzu sastāvs miera stāvoklī var būt normāls, var atklāt hipoksēmiju (ventilācijas-perfūzijas attiecības izmaiņu dēļ) un respiratoru alkalozi, ko pastiprina fiziska piepūle.
Pat agrīnās IPF stadijās fiziskas slodzes laikā pacientiem var tikt konstatēta pulmonāla hipertensija. Pulmonāla hipertensija ir paredzama pacientiem, kam vitālā kapacitāte ir zem 50% no paredzamās normas vai difūzijas spēja samazinās zem 45% no paredzamās normas. Pulmonālas hipertensijas esamība ir slikts prognostisks rādītājs.
Krūškurvja RTG
Gandrīz visiem IPF pacientiem ir izmainīta krūškurvja rentgenogramma. Ap 10% pacientu ar histoloģiski apstiprinātu diagnozi rentgenoloģiskā atrade var būt normāla. IPF raksturīgas perifēras, galvenokārt bazālas, asimetriskas šķiedrainas izmaiņas. Šķiedrainās izmaiņas, kas tiek sauktas par "bišu šūnām", parādās tālu progresējušas slimības gadījumā un ir prognostiski nelabvēlīgas.
Plaušu datortomogrāfija
DT pacientiem ar IPF konstatē plankumainas, galvenokārt - perifēras, subpleirālas, abpusējas bazālas šķiedrainas izmaiņas. Var tikt atrasti arī matstikla aizēnojumi, kas parasti nav pārāk izplatīti. Slimības visvairāk skartajās vietās var atrast trakcijas bronhektāzes, bronhiolektāzes un/vai subpleirālas bišu šūnu tipa izmaiņas. Ja DT tiek konstatētas subpleirālas bišu šūnu tipa izmaiņas, trakcijas bronhektāzes un sabiezētas interlobārās septas, tad šādas izmaiņas tiek sauktas par "drošām" attiecībā uz radioloģisko IPF diagnozi.
Bronhoalveolārā lavāža
Ļoti daudzos pētījumos analizēti IPF pacientu BAL rezultāti. BAL ir nozīmīga dažādu diferenciāldiagnožu izslēgšanai, tomēr IPF diagnostikā tai ir ierobežota nozīme. Neitrofilo un eozinofilo leikocītu palielināts daudzums BAL atsevišķos pētījumos tiek saistīts ar sliktāku prognozi. Limfocitoze BAL, ko atrod mazāk nekā 20% gadījumu, tiek saistīta ar lielāku šūnu daudzumu histoloģiskajos preparātos, mazāku bišu šūnu tipa izmaiņu attīstību un labāku atbildi uz kortikosteroīdu terapiju.
Morfoloģija
Joprojām tiek uzskatīta par IPF diagnozes noteikšanas zelta standartu. Galvenais biopsijas mērķis ir apstiprināt diagnozi atipiskas IPF gadījumā. Šādos gadījumos ir iespējama alternatīva galīgā diagnoze, kas var būtiski mainīt terapijas principus un prognozi. Makroskopiski: preparāts var būt neizmainīts, bieži pleirai ir nodulāra virsma, kas atgādina cirozi. Histopatoloģiski nespecifiska vai parasta intersticiāla pneimonija. Makroskopiskais IPF preparāts var būt neizmainīts, bet bieži pleirai ir nodulāra virsma, kas atgādina cirozi. Histopatoloģiski IPF tiek aprakstīta kā parasta intersticiāla pneimonija (UIP).
UIP tipa izmaiņas var atrast arī citu saslimšanu gadījumos: fibronodulāra sarkoidoze, hronisks hipersensitivitātes pneimonīts, azbestoze, neirofibromatoze, deskvamatīva intersticiāla pneimonija, ar respiratoro bronhiolītu asociētas intersticiālās plaušu slimības, nespecifiska intersticiāla pneimonija, akūta intersticiāla pneimonija, limfocītisks intersticiāls pneimonīts, plaušu histiocitoze X, dažādu toksisku vielu izraisītas slimības u.c. Tomēr katrai no šīm saslimšanām bez UIP ir vēl kādas histoloģiskas nianses, kas nav raksturīgas IPF.
IFP paasinājums
IPF gaitai iespējama pēkšņa pasliktināšanās, ko sauc par IPF paasinājumu (AE). Konstatēts, ka 1 gada laikā AE ir 8,5% pacientu, bet 2 gadu laikā - 9,6%. Paasinājuma kritēriji pēc Kondoha: elpas trūkuma pieaugums pēdējā mēneša laikā, hipoksēmija, ko raksturo arteriālā skābekļa parciālais spiediens/ieelpotā skābekļa parciālais spiediens
Ārstēšana
Joprojām trūkst pārliecinošu pierādījumu jebkādas terapijas efektivitātei, kas nozīmīgi pagarinātu dzīvildzi vai uzlabotu dzīves kvalitāti pacientiem ar IPF. Lai gan kortikosteroīdu efektivitāte nekad nav pārbaudīta ar placebo kontrolētos pētījumos, kortikosteroīdi un imūnsupresanti tiek lietoti kā pamatterapija IPF ārstēšanai. Rekomendējamās devas ir prednizolons 0,5 mg / kg dienā perorāli 4 nedēļas; 0,25 mg/kg dienā - 8 nedēļas, pēc tam samazinot devu līdz 0,125 mg/ kg dienā vai 0,25 mg/kg katru otro dienu. Azatioprīns vai ciklofosfamīds, ko sāk ar 25-50 mg dienā perorāli, katras 7-14 dienas palielinot devu par 25 mg, pakāpeniski sasniedzot maksimālo devu - 150 mg. Vēl pēdējos gados ir pētīts N-acetilcisteīns. Ņemot vērā pozitīvo un pierādīto ietekmi pētījumos, lietošanas drošumu, to iesaka lietot IPF pacientiem 1800 mg/dienā lielā devā.
Ir veikti vairāki daudzcentru placebo kontrolēti pētījumi ar pirfenidonu, kas nomāc šūnu proliferāciju, inhibējot DNS sintēzi, kā arī samazina mRNS līmeni cilvēka miometrija un leiomiomas šūnās. Cilvēka tīklenes pigmentšūnās tas inhibē TGF-b, fibroblastu augšanas faktora inducētu fibroblastu proliferāciju un TGF-b inducētu fibroblastu kolagēna produkciju. Pašlaik IPF monoterapijai pirfenidons ir reģistrēts Japānā, ņemot vērā pozitīvos Japānā veiktā III fāzes klīniskā pētījuma rezultātus.
Joprojām tiek pētīti vairāk medikamenti, kas varētu būt efektīvi šiem slimniekiem, - INF-¡ (interferons gamma), etanercepts (anti-TNF savienojums), imatiniba mesilāts (tirozīnkināzes inhibitors), bosentāns (endotelīna receptoru antagonists), antikoagulanti (varfarīns), sildenafils.
Nefarmakoloģiskā terapija - plaušu transplantācija; vidēji 5 gadu dzīvildze ir 50-60%. Ilgstoša skābekļa terapija, rehabilitācija.
Prognoze
Vidējā pacientu dzīvildze ir 2-5 gadi pēc diagnozes noteikšanas brīža. Klīniska pasliktināšanās parasti saistīta ar slimības progresiju, tomēr bieži vien pacienta vispārējā stāvokļa pasliktināšanos var izraisīt slimības ārstēšanai lietoto medikamentu blakusparādības, pievienojusies infekcija, PATE vai bronhogēnas karcinomas attīstība (10-15% pacientu). Vislielākā nozīme ir plaušu funkcionālo rādītāju izmaiņai noteiktā laika periodā. Labāka prognoze ir:
- pacientiem zem 50gadu vecuma;
- sievietēm;
- pacientiem ar īsāku simptomātisko periodu un mazāku aizdusu;
- pacientiem, kam DT atrod matstikla aizēnojumus un šķiedrainus laukumus;
- pacientiem, kam ir palielināts limfocītu skaits (20-25%) BAL;
- tiem, kam ir laba slimības reakcija uz kortikosteroīdu terapiju, kā arī slimības gaitas stabilizācija pēc sākotnējas kortikosteroīdu terapijas;
- pacientiem, kas joprojām smēķē (iemesli neskaidri).