Elpas trūkumu kā biežu nespecifisku simptomu pacientiem praksē konstatē visu specialitāšu ārsti. Tas ne vienmēr attiecīgi tiek novērtēts. Ehokardiogrāfijai vajadzētu būt vienam no pirmajiem izmeklējumiem, kas jāveic pacientam ar sūdzībām par aizdusu. Viens no retākajiem elpas trūkuma iemesliem var būt plaušu hipertensija. Šoreiz klīniskā gadījuma apskatā paciente, kam elpas trūkumu izraisījusi pulmonāla hipertensija. Pulmonālo hipertensiju var ierosināt daudzas slimības. Kas bija ierosinājis pulmonālo hipertensiju jaunai sievietei, kas jau trīs gadus bija sūdzējusies par elpas trūkumu, lasiet šajā klīniskā gadījuma apskatā.
Klīniskā gadījuma demonstrācija
Paciente, 35 gadus veca. Pēdējos divus gadus sūdzas par elpas trūkumu fiziskas slodzes laikā. Ambulatori veiktajā ehokardiogrāfijas izmeklējumā konstatēta pulmonāla hipertensija, tās dēļ paciente stacionēta izmeklēšanai Paula Stradiņa Klīniskās universitātes slimnīcas Kardioloģijas centrā.
Anamnēze
Jau divus gadus ir sūdzības par progresējošu elpas trūkumu slodzes laikā un paātrinātu sirdsdarbību. Ar šīm sūdzībām atkārtoti vērsusies pie ģimenes ārsta, saņēmusi norādījumus par regulāras fiziskas slodzes nepieciešamību. Nekādi papildu izmeklējumi nav veikti.
Pēdējos trīs mēnešos elpas trūkums palielinājies, tāpēc paciente ambulatori veikusi krūškurvja rentgenogrammu un ehokardiogrāfiju. Konstatēta izteikta pulmonāla hipertensija (labā kambara sistoliskais spiediens 124 mmHg), labo sirds daļu dilatācija, kreisās sirds daļas normāla lieluma, kreisā kambara izsviedes frakcija normāla (69%), vārstuļu funkcija - normāla.
Sūdzības, iestājoties Latvijas Kardioloģijas centrā: pacientei ir izteikts elpas trūkums nelielas slodzes laikā un paātrināta sirdsdarbība.
Slimību anamnēze: gastrīts, holecistektomija (2009. g.). Citas nopietnas slimības, operācijas vai medikamentu nepanesību paciente noliedz.
Ģimenes un dzīves anamnēze: paciente strādā, ir precējusies, dzīvo kopā ar vīru un diviem bērniem. Nesmēķē, alkoholu lieto minimāli. Ģimenē hroniskas plaušu vai sirds-asinsvadu saslimšanas noliedz.
Objektīvā izmeklēšana
Pacientes apziņa skaidra, kontakts adekvāts. Normostēniskas miesasbūves. Āda sārta, sausa, turgors normāls, gļotādas labi caurasiņotas. Perifērie limfmezgli nav palpējami, perifēras tūskas nevēro.
Elpošana 19 ×/min., vezikulāra, trokšņus neizklausa.
Sirdsdarbība 105 ×/min., ritmiska, otrā toņa akcents uz plaušu artērijas. Virs trikuspidālās vārstules dzirdams sistolisks troksnis.
Asinsspiediens 120/85 mmHg.
Vēders palpatori mīksts, nesāpīgs. Akna līdz ar labo ribu loku.
Izmeklējumi
Pilna asinsaina: Lei 10,9 × 109/l, Er 4,34 × 1012/l, Hgb 142 g/l, Tro 197 × 109/l.
Asins bioķīmija - skat. 1. tabulu.
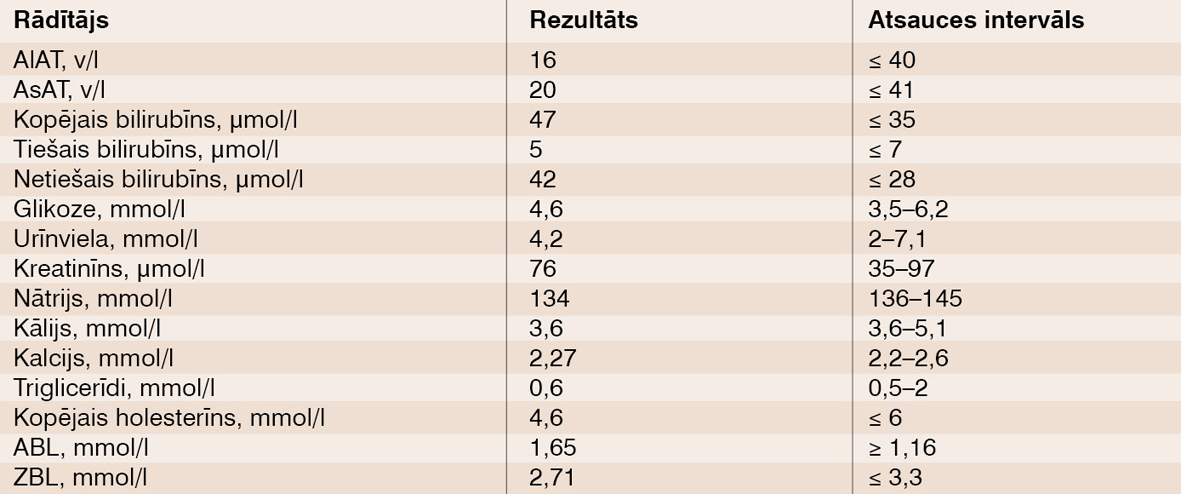

1. tabula
Bioķīmijas analīžu rezultāti
BNP - 181,4 pg/ml (N = 0-100 pg/ml). BNP (brain natriuretic peptide) ir polipeptīds, kas tiek sekretēts galvenokārt sirds kambaros kā atbilde uz kambaru tilpuma pārslodzi un pastiprinātu miokarda iestiepumu. Palielināts BNP var liecināt par sirds mazspēju, kreisā kambara disfunkciju, labā kambara pārslodzi pulmonālas hipertensijas vai akūtas plaušu artērijas trombembolijas gadījumā. Turklāt tā lielums korelē ar sirds mazspējas smagumu un prognozi.
Koagulogramma - protrombīna indekss 69,6%, INR 1,2.
Elektrokardiogramma - sinusa tahikardija 90 ×/min., labā kambara pārslodzes pazīmes.
USG vēdera dobumam - slēdziens: bez patoloģiskas atrades.
Tā kā neinvazīvo izmeklējumu rezultāti liecina par pulmonālo hipertensiju, nākamais uzdevums ir noteikt tās etioloģiju. Ehokardiogrāfijas dati ļauj izslēgt bieži sastopamo pulmonālo hipertensiju (PH) kreisās sirds puses slimību vai vārstuļu bojājumu dēļ. Ehokardiogrāfijā netiek izteiktas aizdomas par iespējamu iedzimtu sirdskaiti. Krūškurvja rentgenogrāfijā nav datu par plaušu saslimšanām. Nākamais diagnostiskais solis ir datortomogrāfija (DT) plaušām ar kontrastvielu, kas ļautu izslēgt vai apstiprināt vēl vienu nereti sastopamu, bet ne vienmēr pietiekami novērtētu PH iemeslu - hronisku plaušu artēriju trombemboliju.
Datortomogrāfija plaušām un videnei ar kontrastvielu. Slēdziens: pēc DT ainas iedzimta sirdskaite ar augstu locētu starpātriju defektu, izteiktu pulmonālo hipertensiju un anomālu plaušu vēnu drenāžu. Labās puses plaušu vēnas drenējas uz labajām sirds daļām un kreisajā pusē brahiocefālās vēnas ieplūst koronārajā sinusā.
Pēc DT redzams, ka šajā gadījumā PH iemesls ir iedzimta sirdskaite - anomāla plaušu vēnu drenāža un priekškambaru starpsienas augstu lokalizēts sinus venosus tipa defekts. Šā tipa priekškambaru starpsienas defekts mugurējā novietojuma dēļ transtorakālajā ehokardiogrāfijā bieži vien netiek konstatēts.
Iedzimtas sirdskaites izraisīta PH pieder pulmonālas arteriālas hipertensijas (PAH) grupai (skat. 2. tabulu), tāpēc nākamais diagnostikas algoritma solis ir labās sirds puses katetrizācija.
Labās sirds puses katetrizācija. Slēdziens: VCC. Hemodinamiski nozīmīgs šunts no kreisās uz labo pusi. Qp:Qs = 3:1. Mērenas pakāpes pulmonāla arteriāla hipertensija (vidējais spiediens plaušu artērijā = 37 mmHg). Nedaudz paaugstināta pulmonālā vaskulārā rezistence -3,2 Wood vienības (norma - līdz 1 Wood vienībai).
Labās sirds puses katetrizācijas laikā iegūts apstiprinājums iedzimtai sirdskaitei un PAH, noteikta attiecība starp pulmonālo (Qp) un sistēmisko (Qs) plūsmu. Attiecība Qp:Qs = 3:1 (norma 1:1, bet hemodinamiski nozīmīgs šunts no kreisās uz labo pusi, ja Qp:Qs > 1,5) norāda uz sirdskaites ķirurģiskas korekcijas nepieciešamību, bet mērena PH un tikai nedaudz palielināta pulmonāla vaskulārā rezistence ļauj cerēt uz relatīvi labu operācijas rezultātu.
Pēc izmeklējumu rezultātiem konsilijā tiek nolemts sākt PAH patoģenētisko terapiju ar T. Revatio (Sildenafil) 20 mg 3 × dienā p/o, lai uzlabotu plānotās ķirurģiskās ārstēšanas rezultātus un mazinātu komplikāciju risku.
Klīniskā diagnoze
Iedzimta sirdskaite - ātriju starpsienas defekts un anomāla plaušu vēnu drenāža.
Pulmonāla arteriāla hipertensija III FK.
Hroniska sirds mazspēja II FK.
Rekomendācijas
3. augustā paciente izrakstīta terapijai ambulatori. Rekomendācijas: ģimenes ārsta uzraudzība, spiediena un pulsa kontrole, mērena fiziskā slodze. Pēc 3 mēnešiem atkārtot EhoKG un BNP.
Pēc konsultācijas ar kardioķirurgiem tuvākajā laikā plānota ķirurģiska iedzimtas sirdskaites korekcija.
Terapija ambulatori:
- T. Revatio 20 mg × 3;
- T. Spirix 12,5 mg × 1 no rīta.
Diskusija
Ja elpas trūkums ir jaunam pacientam - kāds izmeklējums ieteicams kā pirmais?
Dr. A. Rudzītis: Pirmkārt, ja elpas trūkums ir jaunam pacientam, šis simptoms vienmēr jāvērtē kā nopietns, un tā izmeklēšanai jābūt kompleksai: klīniskās analīzes, plaušu rentgens, elektrokardiogrāfija, ehokardiogrāfija, spirometrija (bronhiālā astma, HOPS, plaušu audzējs vai citas plaušu saslimšanas, iedzimta vai iegūta sirdskaite, kardiomiopātija u.c.).
Ja pēc šiem izmeklējumiem diagnozi joprojām nevar noteikt, jāveic plaušu datortomogrāfija ar kontrasta ievadi (plaušu artērijas trombembolija), plaušu perfūzijas/ventilācijas scintigrāfija (sīko artēriju embolija).
Vai ieteikums palielināt fizisko slodzi ir adekvāts - kā tas bija šajā gadījumā?
Dr. J. Romanova: Šajā klīniskajā situācijā ģimenes ārsta ieteikums noteikti nav adekvāts, jo pacientei sūdzības par elpas trūkumu un tahikardiju bija ilgstoši, pasliktinot dzīves kvalitāti. Fiziskas slodzes laikā pacientei kļuva sliktāk. Pirms ieteikuma par fizisko slodzi bija jāveic vismaz EKG, plaušu rentgenogramma un ehokardiogrāfija.
Ja pacientam ir tahikardija - kas ambulatori būtu jāveic?
Dr. A. Rudzītis: EKG un ehokardiogrāfija. Ja tahikardija nav pastāvīga, bet paroksizmāla, jāveic Holtera monitorēšana 24-48 stundas, bet neskaidros gadījumos jāiesaka aritmologa konsultācija.
Ja ehokardiogrāfiski atklāj pulmonālas hipertensijas pazīmes, ar kādiem izmeklējumiem jāturpina?
Dr. A. Rudzītis: Pulmonālā hipertensija vienmēr ir ļoti nopietns sindroms. Ja tas nav saistāms ar noskaidrotu pamatslimību (kreisā kambara mazspēja, aortāla vai mitrāla sirdskaite, cor pulmonale), tad pacients papildus jāizmeklē stacionāra apstākļos specializētā centrā. Latvijā tāda izmeklēšana iespējama Latvijas Kardioloģijas centrā Paula Stradiņa KUS.
Vispusīga izmeklēšana ar daudziem un arī dārgiem izmeklējumiem efektīvāk un ātrāk notiek specializētā centrā. Ģimenes ārsta praksē tas prasa daudz laika, turklāt nepieciešamas specifiskas zināšanas un pieredze darbā ar pulmonālās arteriālās hipertensijas pacientiem. Ģimenes ārstam būtu svarīgi pievērst īpašu uzmanību jebkuram pacientam, kura sistoliskais arteriālais spiediens plaušu artērijā jeb labajā kambarī pēc ehokardiogrāfijas datiem pārsniedz 45 mmHg (norma < 30 mmHg), un konsultēties ar speciālistu pulmonālās arteriālās hipertensijas jomā.
Teorētiskā daļa
Anomāla plaušu vēnu drenāža


2. tabula
Pulmonālās hipertensijas klīniskā klasifikācija (Dana Point, 2008)
Pulmonālā hipertensija (PH) ir hemodinamisks un patofizioloģisks stāvoklis, ko raksturo palielināts vidējais spiediens plaušu artērijās ≥ 25 mmHg miera stāvoklī, un tas ir noteikts, izmantojot labās sirds katetrizāciju. [1] Pēc slimību izraisošajiem faktoriem PH pieņemts iedalīt piecās apakšgrupās (skat. 2. tabulu). Iedzimtu sirdskaišu izraisītu PH pieskaita pulmonālās arteriālās hipertensijas (PAH) grupai, un šajā grupā apvienotas dažādas etioloģijas saslimšanas, kam raksturīga vienāda klīniskā gaita un patoloģiskās izmaiņas plaušu mikrocirkulācijā PH gadījumā. Viena no iedzimtajām sirdskaitēm, kas var izraisīt PAH attīstīšanos, ir anomāla plaušu vēnu drenāža. Šī patoloģija tiek definēta kā šunts no kreisās uz labo pusi, kura gadījumā viena vai vairākas plaušu vēnas drenējas lielā asinsrites loka vēnās vai labajā priekškambarī. Pēc iesaistīto vēnu skaita anomālu plaušu vēnu drenāžu var iedalīt divās apakšgrupās:
- totāla anomāla plaušu vēnu drenāža - visas plaušu vēnas ieplūst lielā asinsrites loka vēnās vai labajā priekškambarī;
- daļēja anomāla plaušu vēnu drenāža - viena vai vairākas, bet ne visas plaušu vēnas drenējas lielā asinsrites loka vēnās vai labajā priekškambarī.
Abas patoloģijas veidojas embrionālās attīstības posmā, kad nenotiek normāla plaušu vēnu aizmetņu atdalīšanās no sistēmisko vēnu pinuma. Anomālas labās puses plaušu vēnas var drenēties augšējā dobajā vēnā, labajā priekškambarī, v. azygos, aknu vēnā vai vārtu vēnā. Bet kreisās puses plaušu vēnas var ieplūst kreisajā v. brachiocephalica, koronārajā sinusā un v. hemiazygos. [2] Divas reizes biežāk mēdz būt anomāla labās plaušas vēnu drenāža, kas bija arī šajā gadījumā.
Pēc pavadošajām plaušu un sirds patoloģijām anomālu plaušu vēnu drenāžu var iedalīt vairākās grupās:
- anomāla plaušu vēnu drenāža ar priekškambaru starpsienas defektu (80-90% gadījumu);
- izolēta anomāla plaušu vēnu drenāža;
- anomāla plaušu vēnu drenāža ar heterotaksijas sindromu (iedzimta sirdskaite, nepareizs iekšējo orgānu novietojums un to malformācijas);
- scimitara sindroms (labās plaušu vēnas drenāža apakšējā dobajā vēnā un labās plaušas un plaušu artērijas hipoplāzija) [3];
Arī šajā klīniskajā gadījumā pacientei bija kombinēta iedzimta sirdskaite - anomāla plaušu vēnu drenāža un priekškambaru starpsienas defekts ar šuntu no kreisās uz labo pusi.
Epidemioloģija
Daļēju anomālu plaušu vēnu drenāžu pirmo reizi aprakstījis Winslow 1739. gadā. Slimības incidence autopsijas materiālā ir 0,4-0,7% [4], tomēr domājams, ka patiesā incidence varētu būt lielāka. Lai gan šī ir reti sastopama iedzimta sirdskaite, tomēr tā novērota līdz pat 10% pacientu ar priekškambaru starpsienas defektu. [3] Pacientiem ar Tērnera sindromu daļēja anomāla plaušu vēnu drenāža novērojama salīdzinoši biežāk. [5]
No visām iedzimtajām sirdskaitēm priekškambaru starpsienas defekts vidēji ir 10% un pat 20-40% no sirdskaitēm, kam pirmā klīniskā manifestācija ir pieaugušo vecumā. Visretākais priekškambaru starpsienas defekta tips ir venozais sinuss, kas novērojams tikai 5-10% gadījumu, tomēr tas salīdzinoši visbiežāk kombinējas ar anomālu labās plaušas vēnu drenāžu (līdz pat 85%). [6]
Abas iedzimtās sirdskaites 2-3 reizes biežāk ir sievietēm.
Klīnika
Atšķirībā no totālas anomālas plaušu vēnu drenāžas, kad klīniskā aina ir smaga un parasti attīstās jau zīdaiņa vecumā, daļēji anomālas drenāžas gadījumā simptomi var attīstīties pieaugušo vecumā un var nebūt izteikti.
Klīnisko simptomu smagums un manifestācijas laiks atkarīgs no vēnu skaita, kas ieplūst sistēmiskajā cirkulācijā. Tiek uzskatīts, ka simptomi parādās, ja anomāli drenējas vairāk nekā 50% no plaušu vēnām. [7] Nozīme ir arī plaušu daivām, ko apasiņo izmainītās vēnas, tā lielāks asiņu tilpums atgriežas sistēmiskajā cirkulācijā no plaušu apakšējām daivām, attiecīgi arī smagāka klīnika novērojama gadījumos, kad nepareizi drenējas vēnas no apakšējām plaušu daivām. Tāpat arī priekškambaru starpsienas defekta klīniskie simptomi ir atkarīgi no tā lieluma un šunta apjoma no kreisās uz labo pusi.
Biežākās pacientu sūdzības ir par elpas trūkumu, kas pakāpeniski progresē, paātrinātu sirdsdarbību, pārsitieniem, sāpēm krūtīs un sinkopes epizodēm.
Diagnostika
Objektīvās izmeklēšanas rezultāti slimības sākumā var būt nespecifiski līdz pulmonālās hipertensijas attīstībai, kam raksturīgs II toņa akcents uz plaušu artērijas, pansistolisks troksnis virs trikuspidālās vārstules, diastolisks pulmonālās nepietiekamības troksnis (Graiema Stīla troksnis) un S4 tonis. [8] Slimībai progresējot, var attīstīties arī tādas labās sirds puses mazspējas pazīmes kā hepatomegālija, paaugstināts jūga vēnu spiediens, ascīts un perifēras tūskas.
Šīs parasti ir acianotiskas sirdskaites, tomēr, progresējot pulmonālajai hipertensijai, var attīstīties Eizenmengera sindroms (šunta reversija no labās uz kreiso pusi) ar tam raksturīgo cianozi, bungvālīšu pirkstiem un pulksteņstikla nagiem. [6]
Daļēja anomāla plaušu vēnu drenāža klasiski tika diagnosticēta plaušu angiogrāfijas laikā, tomēr pēdējā laikā arvien lielāku nozīmi iegūst neinvazīvas diagnostiskās metodes. Bieži izmanto transtorakālo (TTE) un transezofageālo (TEE) ehokardiogrāfija, tomēr tā ne vienmēr var dot pietiekamu informāciju par sirdskaiti. Ar lielāku precizitāti slimību var diagnosticēt, izmantojot datortomogrāfiju (DT) ar kontrastvielu un magnētiskās rezonanses (MR) izmeklējumu. [2]
Ja pacientam attīstījusies PH, diagnozes noteikšanai nepieciešama labās sirds katetrizācija. Tās laikā var noteikt šunta apjomu, ko izsaka kā attiecību starp plūsmu plaušu un sistēmiskajās artērijās (Qp:Qs). Ķirurģisku ārstēšanu rekomendē, ja ir hemodinamiski nozīmīgs šunts no kreisās uz labo pusi (Qp:Qs ≥ 2:1) neatkarīgi no klīnisko simptomu izteiktības. [2]
Venozā sinusa tipa priekškambaru starpsienas defektu tā lokalizācijas dēļ (tuvāk mugurējai sienai) TTE laikā, iespējams, nevarēs diagnosticēt, tāpēc aizdomu gadījumā jāveic TEE, DT vai MR izmeklējumi. Jāatceras, ka visiem pacientiem ar priekškambaru starpsienas defektu un jo īpaši venozā sinusa gadījumā nepieciešams mērķtiecīgi izmeklēt iespējamo anomālo plaušu vēnu drenāžu.
Ārstēšana
Daļējas anomālas plaušu vēnu drenāžas un priekškambaru starpsienas defekta pamata ārstēšanas metode ir ķirurģiska. Daļa speciālistu uzskata, ka operācija veicama visiem pediatriskajiem pacientiem pirms simptomu rašanās, bet citi par indikācijām operācijai min izteiktu šuntu no kreisās uz labo pusi (Qp:Qs ≥ 2), vienas plaušas visu vēnu anomālu drenāžu vai izteiktu klīnisko ainu ar PH un labā kambara pārslodzi, neņemot vērā šunta apjomu. [9]
Parasti tiek izmantota vidējā sternotomijas pieeja un mākslīgā asinsrite. Operācijas laikā vēnas, kas drenējas nepareizi, tiek savienotas ar kreiso priekškambari un slēgts priekškambaru starpsienas defekts. Ļoti labs operācijas rezultāts sagaidāms gadījumos, kad vēl nav attīstījusies PH un labā kambara mazspēja. Lai gan pēcoperācijas mirstība ir minimāla, tomēr nelielā pētījumā tikai 10% no operētajiem pacientiem ar izteiktu sirds mazspēju pēc operācijas ievērojami uzlabojusies labā kambara sistoliskā funkcija. [10]
Pacientiem ar smagu PH un izteiktu pulmonālo vaskulāro rezistenci vienīgā izmantojamā ārstēšanas metode ir plaušu un sirds transplantācija, tomēr arī šajā gadījumā 10 gadu dzīvildze ir ne vairāk kā 30-40%. [9]
Tā kā iedzimtu sirdskaišu izraisīta PH pieder pulmonālās arteriālās hipertensijas grupai, tās terapijā var izmantot tādus patoģenētiskos līdzekļus kā prostaglandīni (epoprostenols, iloprosts, treprostinils), fosfodiesterāzes inhibitori (sildenafils, tadalafils) vai endotelīna receptoru antagonisti (bosentāns, ambrisentāns). [1] Lai gan ar tiem var panākt klīnisku un hemodinamisku uzlabojumu, tomēr tie nevar aizstāt ķirurģisko terapiju un pamatā būtu lietojami pacientiem, kam ir kontrindikācijas operācijai, kā arī simptomu mazināšanai pirmsoperācijas periodā. Pacientu simptomātiskai ārstēšanai var izmantot diurētiķus, aldosterona antagonistus, digoksīnu un ilgstošu skābekļa terapiju.