Smagas norises astma bērniem
Aktualitāte
Smagas norises astmas bērnu vecuma pacienti ir neliela daļa no visiem astmas slimniekiem, bet ir grūti noteikt precīzu prevalenci, tā varētu būt 5% no visiem bērnu astmas pacientiem jeb 0,5% no bērnu populācijas. [1; 2] Šiem pacientiem ir būtiski pazemināta dzīves kvalitāte, slimība var būt priekšlaicīgas nāves cēlonis, smagas norises astmas ārstēšana patērē milzīgus veselības aprūpes resursus. ASV smagas norises astmas pacientu (pusaudžu un pieaugušo) ārstēšanā tiek patērēti vairāk kā 60% no uz astmu attiecināmām veselības aprūpes izmaksām. [3; 4] Nav salīdzināmu datu par pirmskolas vecuma bērniem, bet varētu būt, ka līdzīgi kā smagas pirmskolas vecuma bērnu sēkšanas pacienti arī viņi patērē ļoti lielu daļu elpošanas slimību ārstēšanai atvēlēto veselības aprūpes resursu.
Ja par skolas vecuma bērnu vieglas un vidēji smagas norises astmas diagnostiku un ārstēšanu ir daudz dažādu pētījumu, tad pētījumu par terapijas iespējām bērniem ar smagu astmu ir salīdzinoši maz. Tāpēc rekomendācijas par terapijas iespējām bērniem ar smagas norises astmu pārsvarā pamato ekspertu viedoklis, jo zinātniski pierādītu vadlīniju nav (izņemot par anti-IgE terapiju).
Iespējamie nākotnes riski smagas norises astmas pacientiem
Smaga astma nav tikai problēma pašreizējo simptomu dēļ, bet arī nākotnes risku dēļ, un tie ir:
- normālas plaušu attīstības aizkavēšanās;
- iespējama astmas kontroles pasliktināšanās nākotnē;
- draudoši smagi uzliesmojumi;
- ilgtermiņā ir nopietnāks risks hroniskas obstruktīvas plaušu slimības attīstībai. [7; 8]
Smagas norises astmas pacientiem ir daudz lielāka iespējamība, ka medikamentoza terapija var radīt nopietnas blakusparādības. Tomēr tas attiecas tikai uz tiem pacientiem, kam ir smagas norises grūti ārstējama astma un tiek izvēlēta eksperimentāla "ārpus vadlīniju" terapija. [6]
Daudzi no šiem riskiem ir neizmērāmi, tos grūti iepriekš paredzēt, bet tie apstiprina nepieciešamību nākotnē veikt pētījumus, lai šīs problēmas izprastu labāk. Normālas elpceļu attīstības aizkavēšanās problēmas visskaidrāk aprakstītas Bērnu astmas terapijas programmas (Childhood Asthma Management Program - CAMP) pētījumā,kurā 25% bērnu neatkarīgi no terapijas paveida (nedokromils, budezonīds vai placebo) ar laiku pazeminājās FEV 1 rādītāji. Iemesli tam nav zināmi, bet lielai daļai šo bērnu var attīstīties neatgriezeniska elpceļu obstrukcija pieaugušo vecumā. [7] Labākais ilgtermiņa pētījums par smagas norises bērnu astmas iznākumu ir Melnburnas kohorta. Pētījuma dalībnieki šobrīd ir apmēram 50 gadu veci, 44% smagas norises astmas pacientu ir attīstījusies hroniska obstruktīva plaušu slimība (HOPS), un tie ir bērni, kam plaušu funkcija bija pazemināta 10 gadu vecumā, kad viņi tika iesaistīti kohortā. [8] Skaidrs ir arī tas, ka šiem bērniem nebija pieejama mūsdienu kvalitatīvā astmas terapija, tāpēc to nedrīkst salīdzināt ar smagas norises astmu bērniem mūsdienās, tomēr šie dati jāņem vērā kā nopietns brīdinājums.
Definīcija un klasifikācija
Galvenais šķērslis, lai izprastu smagas norises astmas radītās problēmas bērniem, ir atbilstīgu definīciju trūkums. Definīcijas bieži vien ir nekritiski pielāgotas no pieaugušo dokumentiem. 2000. gadā ATS (American Thoracic Society) darba grupa publicēja definīciju smagai astmai, radot koncepciju, ka astmas smagums var būt saistīts ar uzturošās terapijas devu, kāda nepieciešama, lai simptomu kontrole būtu adekvāta. [9] Būtisks trūkums šai oriģinālajai ATS definīcijai ir tas, ka nav atrunāts konkrēts laika periods, kad ar lielām IGK devām nevar nodrošināt labu astmas kontroli, kas ir priekšnosacījums smagas astmas diagnozes noteikšanai. Smagas, terapijas rezistentas astmas diagnozi var noteikt vienīgi tad, ja ārstam ir pilnīgi skaidrs, ka pacients regulāri un pareizi lieto ordinēto uzturošo terapiju, - un tikai pēc pietiekami ilga laika, kad pacients ir novērots saņemam šo terapiju.
Pasaules Veselības organizācijas (PVO) rekomendācijas
2009. gadā tika izveidota ekspertu grupa ar mērķi izveidot PVO definīciju astmas smagumam un kontrolei, kā arī precīzus kritērijus, lai aprakstītu astmas uzliesmojumus un to smagumu, kuri būtu lietojami gan bērniem, gan pieaugušajiem valstīs gan ar zemu, gan vidēju, gan augstu IKP rādītāju. [10]
Smagas norises astma tika definēta pēc klīniskās kontroles un uzliesmojumu riskiem: nekontrolēta astma, kuras dēļ ir augsts biežu, smagu uzliesmojumu (vai nāves) riska līmenis un/vai izteiktas medikamentu blakusparādības, un/vai hroniska slimības norise (pazemināta (slikta) plaušu funkcija vai aizkavēta plaušu attīstība bērniem). Tika definētas trīs pacientu kategorijas, kas savā starpā var pārklāties:
- neārstēta smagas norises astma- gadījumi, kad astma nav tikusi ārstēta, jo ir problēmas noteikt diagnozi, vai pacients nesaņem uzturošo terapiju, jo tā nav pieejama (ne tikai medikamenti, bet arī krājtelpas). Tā ir ļoti nozīmīga grupa valstīs ar zemu un vidēju IKP rādītāju. [11] Papildu izraisītāji var būt arī dažādi apkārtējās vides faktori- pasīvā smēķēšana, gaisa piesārņojums, kas var veicināt astmas uzliesmojumus. Problēmas var rasties, ja valstī nav astmas vadlīniju, ja netiek ievēroti galvenie pamatprincipi astmas ārstēšanā un ja nenotiek astmas pacientu ģimeņu izglītošana. Lielākajā daļā gadījumu šādas problēmas ir mazattīstītajās valstīs, tomēr daļā attīstīto valstu tās parādās situācijās, ja medikamentu izmaksas ir pārāk lielas un veselības aprūpes medikamentu kompensācijas sistēma ir nepilnīga;
- grūti ārstējama smagas norises astma (difficult-to-treat severe asthma)- šajā grupā ir pacienti, kuru astma nereaģē uz terapiju, bet bieži gadījumos, kad izvēlēta atbilstīga astmas terapija, astmas norise kļūst kontrolējama. Problēmas varētu radīt līdzestības trūkums, neadekvāta vai nepareiza inhalatoru lietošanas metode vai iespējamie kaitīgie apkārtējās vides faktori. Šajā kategorijā varētu ietilpt arī bērni ar dažādām neārstētām blakusslimībām, piemēram, aptaukošanos, kas ļoti ietekmē astmas kontroli;
- terapijas rezistenta smagas norises astma- šajā kategorijā ir bērni ar smagas norises astmu, kuriem, lai gan viņi saņem adekvātu terapiju (ar visu iespējamo papildterapiju) un ir ļoti līdzestīgi, astma tomēr netiek kontrolēta vai kontrole tiek sasniegta tikai ar ļoti lielu devu astmas medikamentiem, kas rada nozīmīgas blaknes. Attīstītajās valstīs šī diagnoze jālieto salīdzinoši reti, lai uzsvērtu gadījumus, kad jāveic molekulārie un celulārie izmeklējumi, lai precīzāk noteiktu iekaisuma raksturu un izmēģinātu jaunas ārpusvadlīniju terapeitiskas pieejas (novel therapies).
Starptautiskas pediatru respiratorās medicīnas pētnieku grupas rekomendācijas
Starptautiska pediatru respiratorās medicīnas pētnieku grupa GA2LEN initiative [12]problemātisku smagas norises astmu iesaka definēt saistībā ar vecumgrupām un pēc simptomu rakstura:
- skolas vecuma bērni, kam joprojām saglabājas simptomi, kaut arī viņi saņem lielu devu IGK (≥800µg/dn budezonīda ekvivalenta) un papildus ir nozīmēts izmēģinājuma terapijas kurss ar vismaz 2vai 3medikamentiem (ilgstošas darbības β2 agonisti (D β2A), leikotriēnu receptoru antagonisti (LTRA) un/vai teofilīns). Ja papildu medikaments nav efektīvs pietiekami ilgā laika periodā, tas jāatceļ;
- pirmsskolas vecuma bērni, ja bērnam, saņemot maksimāli pieļaujamo vadlīnijās rekomendēto medikamentu kombināciju, netiek panākta astmas simptomu kontrole, viņš jāuzskata par smagas norises astmas pacientu.
Klasifikācija pēc simptomu rakstura
Smagas norises astmas klasifikācija pēc simptomu rakstura:
- pastāvīgi (lielākajā daļā dienu ≥3mēnešus) hroniski elpceļu obstrukcijas simptomi, pasliktinājusies dzīves kvalitāte. Šajā grupā ietilpst arī 1.tipa nestabila (brittle) astma (ļoti izteiktas plaušu funkciju diennakts svārstības ilgstošā laika periodā);
- adekvātas astmas terapijas fonā (veikti arī pasākumi, lai izvairītos no alergēniem) akūti uzliesmojumi (ar vai bez periodiem starp tiem, kad astma ir slikti kontrolēta), kas var būt ļoti smagas norises. To raksturo:
- vismaz viena stacionēšana intensīvās terapijas (IT) nodaļā,
- vismaz 2 stacionēšanas reizes, kad nepieciešama i/v medikamentu ievade,
- vismaz 2 p/o GK kursi pēdējā gada laikā;
- pastāvīga elpceļu obstrukcija ar pozitīvu bronhodilatācijas testu, kura saglabājas pēc p/o GK terapijas kursa;
- 2.tipa nestabila astma, definīcija pēc pieaugušo pētījumu datiem, to raksturo ārkārtīgi strauji sācies smagas norises uzliesmojums, kura dēļ pacients tiek hospitalizēs IT nodaļā;
- nepieciešamība pēc p/o GK neregulārā režīmā vai katru dienu.
Kopumā ir ļoti būtiski saprast, ka astma drīzāk ir dažādu klīnisku pazīmju kopums, nevis precīza diagnoze - pretēji, piemēram, hroniskai nieru mazspējai, un tā ir daudzu faktoru mijiedarbības galarezultāts, tāpēc dažādās pasaules vietās astmas fenotipi var būtiski atšķirties, piemēram, Lielbritānijā bērniem ar astmu ļoti bieži ir alerģiska sensibilizācija [13], bet Brazīlijā astma biežāk ir neatopiska un pārsvarā saistīta ar agrīnām respiratorām vīrusu infekcijām. [14]
Bieži pie speciālista diagnozes precizēšanai tiek nosūtīti bērni, kuru astma "nepadodas standarta ārstēšanai", tomēr, pirms bērnam nosaka smagas norises astmas vai terapijas rezistentas astmas diagnozi, jāņem vērā vairāki apstākļi [15]:
- pilnībā jāizslēdz citu diagnožu iespējamība un nopietnas blakusslimības;
- jāoptimizē pamata terapija, jāpārbauda pacienta līdzestība, ideāli, ja ir iespējamas arī mājas vizītes pie pacienta, lai pārliecinātos, ka bērns patiešām adekvāti saņem ārsta parakstīto terapiju.
Tad mazāk kā puse bērnu, kam koriģē astmas bāzes terapiju un kas patiešām to saņem, tiek klasificēti kā smagas norises astmas pacienti.
![Izmeklējumi pacientam ar smagu astmu [13]](https://cdn.doctus.lv/media/2013/01/2/original/3b1a7f2c27c1.jpg)
![Izmeklējumi pacientam ar smagu astmu [13]](https://cdn.doctus.lv/media/2013/01/2/original/3b1a7f2c27c1.jpg)
Diagnostika
Pirmais solis ir detalizētas slimības vēstures precizēšana, pacienta objektīvā izmeklēšana un spirometrija. Protams, nav izmeklējumu, ar kuriem pilnīgi droši var apstiprināt vai izslēgt astmas diagnozi, bet ir četri jautājumi, kas noteikti jāuzdod.
- Vai trokšņi, ko apraksta pacients (ģimene), patiešām ir sēkšana izelpā vai tie ir kādi mazāk specifiski trokšņi? Īsta intermitējoša sēkšana būtu jāapstiprina ārstam. Protams, sēkšana var būt citu saslimšanu dēļ, bet tās neesamība varētu raisīt šaubas par astmas diagnozi.
- Vai ir kādas pazīmes, anamnēzes vai objektīvās apskates dati, kas varētu apstiprinātu kādu citu diagnozi?
- Ja pacientam ir, piemēram, bungvālīšu pirksti, tad jāapsver cistiskās fibrozes (CF) diagnoze, jāveic sviedru tests.
- Hronisks produktīvs klepus ar krēpām nav raksturīgs astmai, šādiem pacientiem jāveic izmeklējumi CF, bronhektāžu, primāras ciliāras diskinēzijas (PCD), imūndeficīta izslēgšanai.
- Ja bērnam simptomi ir jau no pirmās dzīves dienas, tas, visticamāk, liecina par kādu iedzimtu patoloģiju, nevis astmu.
- Ja simptomi sākušies ļoti pēkšņi, jāizslēdz svešķermeņa aspirācija.
- Vai pacientam klepus, sēkšana ir ēšanas laikā. Jāizvērtē, vai tos neizraisa rīšanas traucējumi neiroloģisku saslimšanu dēļ vai traheoezofageāla fistula (TEF).
- Nereversibla smaga obstrukcija var liecināt par kādu no intersticiālām plaušu slimībām (IPS).
- Vai bērns ir atopisks? Atopija jāpierāda gan ar ādas dūriena testiem, gan ar specifisko seruma IgE noteikšanu, jo ir pētījumi, ka abi šie rādītāji var nekorelēt. [16] Ja bērns tiek nosūtīts kā smagas norises astmas pacients un ir neatopisks, tad uzmanīgi jāpārvērtē diagnoze.
- Vai bērnam anamnēzē laika gaitā bijušas variablas elpceļu obstrukcijas, kā tās ārstētas, pierādītas?
Izmeklējumu algoritmu pacientam ar smagas norises astmu skat. attēlā. Fizioloģiskos testus smagas norises astmas gadījumā skat. 1. tabulā.
![Fizioloģiskie testi smagas norises astmas gadījumā [6]](https://cdn.doctus.lv/media/2013/01/2/original/fb780ab29f0b.jpg)
![Fizioloģiskie testi smagas norises astmas gadījumā [6]](https://cdn.doctus.lv/media/2013/01/2/original/fb780ab29f0b.jpg)
Smagas norises astmas bērnu vecuma pacientiem var būt laba plaušu funkcija.
Negatīvs bronhu provokācijas tests (BPT) bērniem ar izteiktiem simptomiem izslēdz astmu kā šo simptomu cēloni. Ja tomēr pacientam tiek apstiprināta astmas diagnoze, jāņem vērā, ka astmas norisi būtiski var pasliktināt dažādas neārstētas blakusslimības.
Blakusslimības
Astma un aptaukošanās
Tā ir visvieglāk diagnosticējamā blakusslimība. Astmas, nespecifisko elpceļu simptomu un aptaukošanās mijiedarbība ir kompleksa. Aptaukošanās viennozīmīgi var radīt elpas trūkumu, kas ne vienmēr saistīts ar astmu, tāpēc rūpīgi jāizvērtē reversiblu elpceļu obstrukcijas esamība, pirms bērniem ar lieko ķermeņa masu tiek nozīmēti astmas medikamenti. Aptaukošanās var radīt rezistenci pret steroīdiem, tāpēc bērniem ar lieko svaru un astmu ir ļoti būtiski normalizēt ķermeņa masas indeksu (ĶMI). [17]
Astma un augšējo elpceļu slimības
Labi zināms, ka alerģisks rinosinusīts ir ļoti bieža astmas blakus saslimšana [18], kas būtiski pasliktina dzīves kvalitāti. Līdz 80% astmas pacientu ir arī alerģisks rinīts, bet 15% alerģiskā rinīta pacientu ir astma. Neārstēts alerģisks rinīts palielina astmas uzliesmojumu iespējamību. [19]
Astma un disfunkcionāla elpošana
Balss saišu disfunkcijas simptomi, hiperventilācija un citas elpošanas disfunkcijas formas var imitēt astmas klīniku. Šīs problēmas var atklāt, precīzi ievācot slimības anamnēzi. Simptomi, kas izzūd, ja bērns ir miegā, ir ļoti neraksturīgi astmai. [20] Citas norādes, kas varētu vedināt uz domām par disfunkcionālu elpošanu, ir žņaudzoša sajūta kaklā, parestēzijas, krampji rokās, kā arī tad, ja stridors vai sēkšana ir skaļāka balsenes rajonā. Šādos gadījumos pacients jāsūta pie pieredzējuša fizioterapeita, runas terapeita vai klīniskā fiziologa.
Astma un gastroezofageālais atvilnis (GEA)
Respiratoro simptomu un GEA mijiedarbība ir kompleksa un daudzveidīga. 25-80% bērnu ar plaušu slimībām ir GEA. GEA izraisa aspirāciju un simptomus. GEA palielina bronhu hiperreaktivitāti, jo rada barības vada lejasdaļas neirālu aktivitāti. Respiratorie simptomi rada vai pastiprina GEA. Astmas medikamenti, piemēram, teofilīns, var provocēt GEA. [22]
Ja pacientam diagnosticē asimptomātisku GEA, tad maz ticams, ka GEA ārstēšana uzlabos astmas simptomus.
Ja ir aizdomas par simptomātisku GEA, noteikti ir vērts nozīmēt izmēģinājuma terapijas kursu, bet, ja uz to nav atbildes, tad pirms medikamentu devas palielināšanas jānozīmē 24 stundu barības vada pH-metrija. Lielākajā daļā gadījumu asimptomātiska GEA ārstēšana skolas vecuma bērniem ar smagas norises astmu būs mazefektīva. [23]
Astma un pārtikas alerģija
Bērniem ar smagas norises astmu bieži ir sensibilizācija pret pārtikas alergēniem. Tomēr līdz galam nav skaidrs, vai smagas norises astma un smaga pārtikas alerģija atspoguļo atopisku predispozīciju vai pārtikas alerģija rada smagu astmu.
Tā kā astmas pacientiem var būt īpaši smaga anafilaktiska rekcija uz pārtiku, tad gan pārtikas alerģijas, gan astmas ārstēšanā rekomendē agresīvu terapeitisko pieeju. [24]
Smagas norises astmas diagnoze tiek apstiprināta
Galvenie četri jautājumi, kuru atrisināšana var sniegt labu rezultātu smagas norises astmas pacientu ārstēšanā [6]:
- terapijas līdzestības uzlabošana, izglītošana;
- apkārtējās vides alergēnu ekspozīcijas samazināšana;
- pasīvās smēķēšanas izslēgšana;
- psihosociālo problēmu atrisināšana.
Izglītošana
Visiem bērniem un vecākiem ir jāparāda, kā pareizi lietot inhalatoru, un jāizsniedz izglītojoši materiāli par astmu. Tomēr ļoti būtiski ir atkārtot to katrā vizītē, jo pacienti daudz ko mēdz aizmirst un ne vienmēr visu saprot ar pirmo reizi. Ir pētījumu dati, ka gandrīz 40% pacientu inhalatorus lieto nepareizi, kaut arī viņi apmācīti atkārtoti. 15% lieto nepareizo ierīci inhalāciju medikamentiem (visbiežākā kļūda ir aerosola inhalatoru lietošana bez krājtelpas). [25]
Katrā vizītē ar pacienta vecākiem jārunā par izvairīšanos no simptomus provocējošajiem alergēniem un kairinātājiem, īpaši gadījumos, kad pacientam ir ļoti slikta astmas kontrole vai bieži astmas uzliesmojumi. Lai uzlabotu līdzestību, jāveidojas dialogam starp mediķu komandu un pacienta ģimeni.
Apkārtējā vide mājās un ap tām
Nav šaubu, ka sensibilizācija pret aeroalergēniem ir bieži izplatīta un, ja sensiblizētam bērnam aeroalergēni mājās ir augstā līmenī un ja tas kombinējas ar vīrusu infekciju, tad tas bieži izraisa smagas astmas lēkmes, ārkārtas vizītes pie ārsta un hospitalizāciju. [26] Polisensibilizētiem pacientiem biežāk ir astmas uzliesmojumi. [27] Ir ļoti grūti novērtēt pacienta mājas apstākļus bez mājas vizītes. Pētījumi pierāda, ka vecāki paši reti adekvāti apraksta mājas apstākļus un iespējamos astmas izraisītājus - pasīvo smēķēšanu, mājas putekļu ērcīšu, dzīvnieku epidermālo alergēnu klātbūtni, palielināta iekštelpu mitruma, pelējuma sēnīšu esamību. Arī tādi faktori kā ar malku kurināma vai gāzes plīts var būtiski negatīvi ietekmēt astmas norisi. [28; 29] Bērnam ar smagas norises astmu mājās pilnīgi jāizslēdz pasīvā smēķēšana, jo ir virkne pētījumu ar pieaugušajiem, pierādot, ka smēķēšana veicina steroīdu rezistences attīstību, un ir pietiekams pamats domāt, ka pasīvā smēķēšana rada līdzīgu efektu. [30] Ir jāiegulda vislielākās pūles, lai palīdzētu vecākiem atmest smēķēšanu, pat nosūtot pacientu pie narkologa. Šādiem pacientiem jānovērš alergēnu ekspozīcija mājās (mājas putekļu ērcīšu samazināšanas pasākumi, neturēt dzīvniekus, normalizēt ventilāciju, apkuri, lai izvairītos no pelējuma rašanās), jo sensibilizētiem pacientiem kontakts ar alergēniem var veicināt steroīdu rezistences attīstību. [31] Aeroalergēni lielā koncentrācijā mājās veicina astmas norises pasliktināšanos arī nesensibilizētiem pacientiem. [33] Sensibilizācija pret pelējuma sēnītēm un pelējums bērna dzīves telpā saistīti ar palielinātu saslimstību ar astmu, astmas norises pasliktināšanos un patiešām smagiem uzliesmojumiem. Šādos gadījumos terapija noteikti jāsāk ar pacienta pārcelšanu uz dzīvesvietu bez pelējuma, iespējams, kombinācijā nozīmējot arī perorāli lietojamos pretsēnīšu medikamentus, pirms sākt toksisku devu steroīdu terapiju. [34; 35]
Līdzestība terapijai
Ordinēto medikamentu nelietošana vai nepareiza lietošana ir biežākais iemesls ilgstošiem simptomiem pacientiem ar smagas norises astmu. Ārstam vizītes laikā ir ļoti grūti objektīvi izvērtēt, cik adekvāta ir pacienta līdzestība terapijai un vai pacients zāles saņem atbilstīgi norādēm un pareizā veidā. Raksturīgi, ka vecāki bieži vien novērtē līdzestību medikamentu lietošanā. Speciālists, kas strādā klīnikā, nevar nodrošināt ļoti labu līdzestību terapijai, tāpēc jānotiek ciešai sadarbībai ar ģimenes ārstu, lai precīzi zinātu pacientam izrakstīto medikamentu daudzumu. Sadarbībā ar aptieku būtu ļoti svarīgi noskaidrot, vai izrakstītie medikamenti tiek arī iegādāti. Izrakstīto medikamentu daudzums nenozīmē, ka medikamentu patiešām lieto, bet, ja medikaments nav izrakstīts, tas droši nozīmē, ka pacients to nav saņēmis. [36; 37]
Vairāku centru pieredze rāda, ka nozīmīga ir pieredzējušas medmāsas vizīte pie pacienta mājās, kur viņa iegūst ļoti plašu informāciju par līdzestību terapijai - vai medikaments vispār ir iegādāts, vai medikaments tiek lietots, vai tas tiek glabāts oriģinālajā iepakojumā; ja medikaments stāv grūti aizsniedzamā vietā, maz ticams, ka to regulāri lieto ikdienā. Māsa pārliecināsies, vai medikamentam nav beidzies derīguma termiņš un vai pacients nelieto tukšu aerosola inhalatoru. Ir dati, kas liecina, ka daudzi vecāki pat maziem bērniem medikamentus liek lietot patstāvīgi, bez uzraudzības. [38] Ir jāpārliecinās, vai tiek lietota bērna vecumam atbilstīga krājtelpa, vai krājtelpas lietošanas metode ir pareiza, vai krājtelpa tiek kopta regulāri un pareizi.
Pētījumā par medmāsas piesaisti mājas vizītēs pie pacienta ar smagu, slikti kontrolētu astmu atklājās, ka ordinēto terapijas veidu lieto mazāk kā puse pacientu. [39]
Vairāku pētījumu analīze liecina, ka lielākajai daļai pacientu ar smagu astmu, kas tiek klasificēta kā problemātiska, tā jāklasificē kā problemātiska zemās līdzestības dēļ, nevis kā smaga terapijas rezistenta astma. [40]
Ir ļoti būtiski pārliecināties par līdzestības kritērijiem, pirms pacientu klasificē kā smagas terapijas rezistentas astmas pacientu un viņam tiek nozīmēti invazīvi izmeklējumi, tādā veidā samazinot invazīvo izmeklējumu radīto blakusparādību risku un veselības aprūpes izmaksas astmas ārstēšanā.
Psihosociālās problēmas un stress
Bērniem un pusaudžiem, kuru nāves cēlonis ir astma, kā arī tiem pacientiem, kam ir gandrīz letāla astmas lēkme (near-fatal asthma episode), nozīmīgs tās iemesls ir psihosociālas problēmas - slimības noliegšana, medikamentu nelietošana. [41]
Daudzos gadījumos psihosociālās problēmas var atklāt tikai mājas vizītēs, kad pacienta vecāki ir vairāk gatavi runāt par konfidenciāliem jautājumiem.
Pierādīts, ka stress pasliktina astmas norisi, jo pastiprina eozinofilo iekaisumu un tādā veidā izraisa astmas uzliesmojumus. [42; 43] Psiholoģiskais distress ietekmē astmas norisi ar neiroimunoloģiskiem mehānismiem un veicina steroīdu rezistences attīstību. Šis faktors ir nozīmīgs, jo smagai grūti ārstējamai astmai raksturīga rezistence pret astmas medikamentiem. [44]
Astma ir smagas norises un nepadodas standarta terapijai
Nākamais solis ir detalizēta daudzdisciplināra pieeja, kurā piedalās arī pieredzējusi pneimonologa/alergologa māsa. Ja tas nav iespējams, jāiesaista ģimenes ārsts.
Ir vairāki pētījumi, kas pierāda: ja pacientam izvēlēta mērķtiecīga terapija, kas vērsta uz astmas kontroles uzlabošanu, vairāk nekā pusē gadījumu tas atrisina smagas astmas problēmas bērnu vecumā, diemžēl nav skaidru padomu, kā ikdienas praksē atrisināt līdzestības problēmas. Viens no variantiem apkopots Bromptonas Karaliskā hospitāļagrūtiārstējamās astmas protokolā (skat. 2. tabulu).[13] Atkārtota vizīte notiek pēc 4 nedēļām. Šo izmeklējumu mērķis ir atbildēt uz 4 jautājumiem.
- Kāds ir elpceļu iekaisuma raksturs?
- Vai ir atbilstība starp simptomiem un iekaisumu?
- Vai bērnam tiešām ir uz steroīdiem nereaģējoša astma?
- Vai bērnam ir pastāvīga elpceļu obstrukcija?
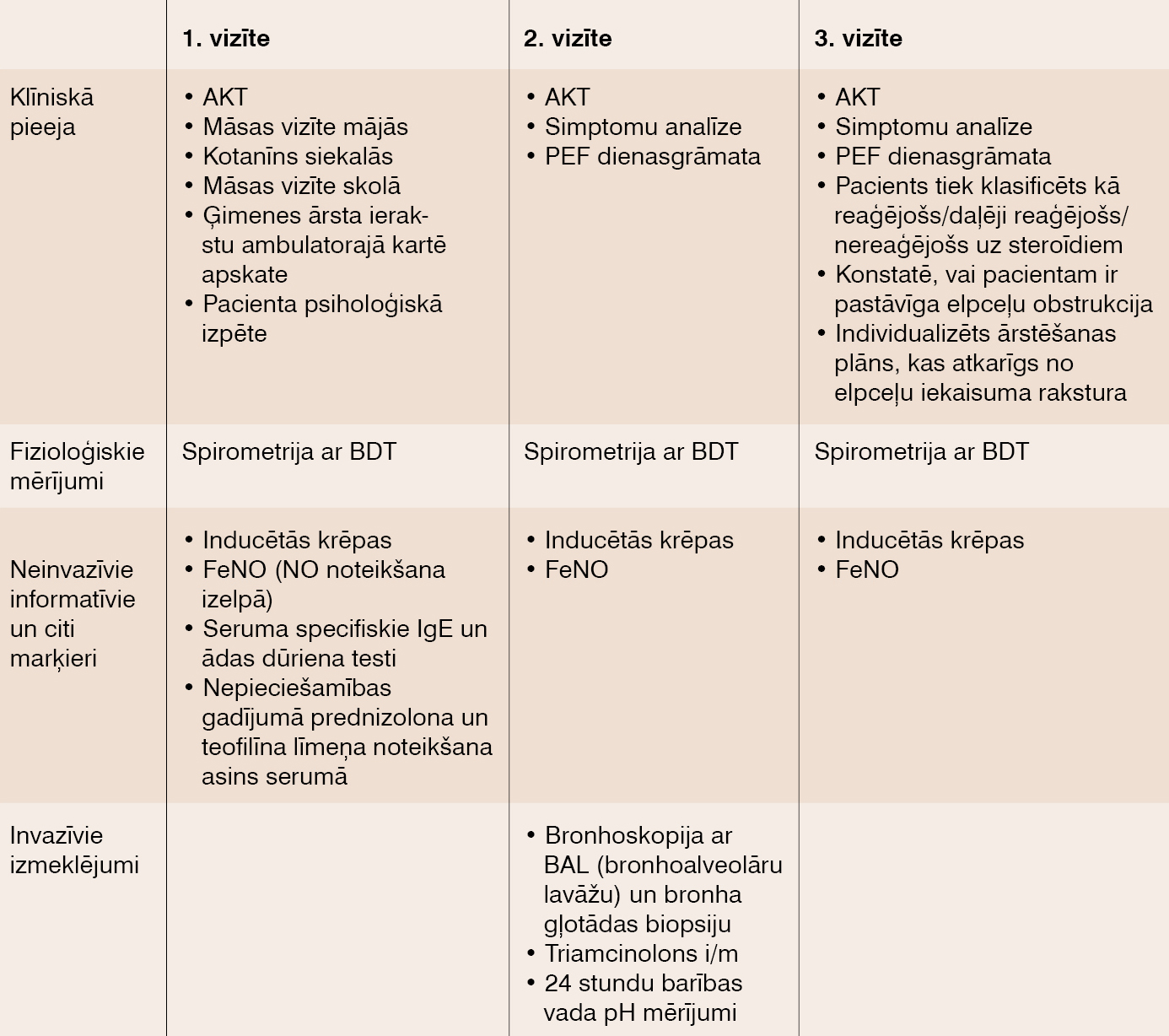
 2. tabulaBromptonas Karaliskā hospitāļa grūti ārstējamās astmas protokols
2. tabulaBromptonas Karaliskā hospitāļa grūti ārstējamās astmas protokols
Elpceļu iekaisuma raksturs
Teorētiski iekaisumu var klasificēt kā eozinofilu, neitrofilu vai jaukta tipa. Iespējams (bet tas nav līdz galam pierādīts), ka atsevišķos gadījumos terapiju var izvēlēties pēc elpceļu iekaisuma rakstura, piemēram, ir atsevišķi pierādījumi, ka neirotrofilas astmas gadījumā efektīva var būt makrolīdu lietošana. [45]
Atbilstība starp simptomiem un iekaisumu
Koncepciju par "atbilstīgu" un "neatbilstīgu" fenotipu pamato pētījumi pieaugušo grupā. Par "neatbilstīgam" fenotipam piederošu jāuzskata pacients, kam ir ļoti daudz simptomu, bet minimālas elpceļu iekaisuma pazīmes, vai pretēji - pacients bez sūdzībām, bet ar izteiktu eozinofilo iekaisumu elpceļos. Pēdējā grupa varētu būt fenotips "ar noslieci uz uzliesmojumiem", un šiem pacientiem varētu būt noderīga terapijas intensificēšana. [46]
Būtiskākais iemesls šo divu fenotipu nodalīšanai ir tas, ka "neatbilstīgā" fenotipa pacientiem bez sūdzībām būtu vērts regulāri veikt neinvazīvo iekaisuma rādītāju noteikšanu, lai pārraudzītu terapijas efektivitāti. Savukārt pacientiem ar izteiktām sūdzībām, bet bez paaugstinātiem iekaisuma rādītājiem elpceļos nav loģiski parakstīt potenciāli toksisku pretiekaisuma terapiju lielās devās.
Vai bērnam tiešām ir uz steroīdiem nereaģējoša astma


Kritērijus GK terapijas kursa efektivitātes izvērtēšanai skat. 3. tabulā.
Terapijas iespējas pacientiem ar smagas norises astmu apkopotas 4. tabulā.
![Terapijas iespējas pacientiem ar smagas norises astmu [6; 13]](https://cdn.doctus.lv/media/2013/01/2/original/00498d7b009b.jpg)
![Terapijas iespējas pacientiem ar smagas norises astmu [6; 13]](https://cdn.doctus.lv/media/2013/01/2/original/00498d7b009b.jpg)
Kopsavilkums
Smagas norises grūti ārstējamas astmas pacienti ir ļoti neliela daļa no visiem astmas pacientiem bērnu vecumā. Tā rada nopietnus riskus nākotnē. Lielākajā daļā gadījumu, optimizējot astmas terapiju un izslēdzot alergēnus/kairinātājus apkārtējā vidē, izdodas būtiska astmas kontroles uzlabošanās. Ja tomēr terapijas korekcija vēlamo rezultāti nedod, jāorganizē apmācītas medmāsas vizīte pie pacienta mājās, lai pārliecinātos par bērna dzīves apstākļiem un medikamentu lietošanas paradumiem. Ja šo pasākumu rezultātā astmas kontrole neuzlabojas, bērns stacionējams terciārā līmeņa stacionāra pneimonoloģijas nodaļā izmeklēšanai un terapijas korekcijai, jo neiedarbīga ilgstoša terapija ar lielām medikamentu devām nav pieļaujama.
Literatūra
- Kupczyk M, Wenzel S. US and European Severe Asthma Cohorts: what can they teach us about severe asthma? J Intern Med, 2012; 272: 121-32.
- Lang A, Carlsen KH, et al. Severe asthma in childhood: assessed in 10 year olds in a birth cohort study. Allergy, 2008; 63: 1054-1060.
- Godard P, Chanez P, et al. Costs of asthma are correlated with severity: a 1-yr prospective study. Eur Respir J, 2002; 19: 61-67.
- Smith DH, Malone DC, et al. A national estimate of the economic costs of asthma. Am J Respir Crit Care Med, 1997; 156: 787-793.
- Brand PL, Baraldi E, et al. Definition, assessment and treatment of wheezing disorders in preschool children: an evidence-based approach. Eur Respir J, 2008; 32: 1096-1110.
- Hedlin G, de Benedictis FM, Bush A. Problematic severe Asthma. Eur Respir Monogr, 2012; 56: 22-39.
- Covar RA, Spahn JD, et al. Progression of asthma measured by lung function in the childhood asthma management program. Am J Respir Crit Care Med, 2004; 170: 234-241.
- Phelan PD, Robertson CF, Olinsky A. The Melbourne Asthma Study: 1964-1999. J Allergy Clin Immunol, 2002; 109: 189-194.
- Proceedings of the ATS workshop on refractory asthma: current understanding, recommendations, and unanswered questions. Am J Respir Crit Care Med, 2000; 162: 2341-2351.
- Bousquet J, Mantzouranis E, et al. Uniform definition of asthma severity, control, and exacerbations: document presented for the World Health Organization Consultation on Severe Asthma. J Allergy Clin Immunol, 2010; 126: 926-938.
- Robertson J, Forte G, et al. What essential medicines for children are on the shelf? Bull World Health Organ, 2009; 87: 231-237.
- Hedlin G, Bush A, et al. Problematic severe asthma in children, not one problem but many: a GA2LEN initiative. Eur Respir J, 2010; 36: 196-201.
- Bush A, Frey U, Teague WG. Special problems of severe asthma in childhood. Eur Respir Mon, 2011; 51: 59-81.
- Pereira MU, Sly PD, et al. Nonatopic asthma is associated with helminth infections and bronchiolitis in poor children. Eur Respir J, 2007; 29: 1154-1160.
- Bush A, Hedlin G, et al. Severe asthma in childhood: a common international approach. Lancet, 2008; 372: 1019-1021.
- Frith J, Fleming L, Bossley C, et al. The complexities of defining atopy in severe childhood asthma. Clin Exp Allergy, 2011; 7: 948-953.
- Sutherland ER, Goleva E, et al. Body mass and glucocorticoid response in asthma. Am J Respir Crit Care Med, 2008; 178: 682-687.
- Bourdin A, Gras I, Chanez V. Upper airway? Allergic rhinitis and asthma: united disease through epithelial cells. Thorax, 2009; 64: 999-1004.
- de Benedictis FM, Bush A. Hypothesis paper: rhinosinusitis and asthma - epiphenomenon or causal association? Chest, 1999; 115: 550-556.
- Niggemann B. Functional symptoms confused with allergic disorders in children and adolescents. Pediatr Allergy Immunol, 2002; 13: 312-318.
- Bechard DE, Shumert ML. Gastro-oesophageal reflux-induced asthma: new insights. Gastroenterology, 1998; 114: 849-850.
- de Benedictis FM, Carnielli VP, de Benedictis D. Aspiration lung disease. Pediatr Clin North Amer, 2009; 56: 173-190.
- Thakkar K, Boatright RO, et al. Gastroesophageal reflux and asthma in children: a systematic review. Pediatrics, 2010; 125: e925-e930.
- Roberts G, Patel N, et al. Food allergy as a risk factor for life-threatening asthma in childhood: a case controlled study. J Allergy Clin Immunol, 2003; 112: 168-174.
- Kamps AW, van Ewijk B, et al. Poor inhalation technique, even after inhalation instructions, in children with asthma. Pediatr Pulmonol, 2000; 29: 39-42.
- Murray CS, Poletti G, et al. Study of modifiable risk factors for asthma exacerbations: virus infection and allergen exposure increase the risk of asthma hospital admissions in children. Thorax, 2006; 61: 376-382.
- Haselkorn T, Zeiger RS, et al. Recent asthma exacerbations predict future exacerbations in children with severe or difficult-to-treat asthma. J Allergy Clin Immunol, 2009; 124: 921-927.
- Belanger K, Triche EW. Indoor combustion and asthma. Immunol Allergy Clin North Am, 2008; 28: 507-519.
- Howden-Chapman P, Pierse N, et al. Effects of improved home heating on asthma in community dwelling children: randomised controlled trial. BMJ, 2008; 337: a1411.
- Livingston E, Chaudhuri R, et al. Systemic sensitivity to corticosteroids in smokers with asthma. Eur Respir J, 2007; 29: 64-71.
- Matsui EC, Hansel NN, et al. Asthma in the inner city and the indoor environment. Immunol Allergy Clin North Am, 2008; 28: 665-686.
- Nimmagadda SR, Szefler SJ, et al. Allergen exposure decreases glucocorticoid receptor binding affinity and steroid responsiveness in atopic asthmatics. Am Rev Respir Crit Care Med, 1997; 155: 87-93.
- Langley SJ, Goldthorpe S, et al. Relationship between exposure to domestic allergens and bronchial hyperresponsiveness in non-sensitised, atopic asthmatic subjects. Thorax, 2005; 60: 17-21.
- Neukirch C, Henry C, et al. Is sensitization to Alernaria alternate a risk factor for severe asthma? A population based study. J Allergy Clin Immunol, 1999; 103: 709-711.
- Black PN, Udy AA, Brodie SM. Sensitivity to fungal allergens is a risk factor for life-threatening asthma. Allergy, 2000; 55: 501-504.
- Chanez P, Wenzel SE, et al. Severe asthma in adults: what are the important questions? J Allergy Clin Immunol, 2007; 119: 1337-1348.
- Robinson DS, Campbell DA, et al. Systematic assessment of difficult-to-treat asthma. Eur Respir J, 2003; 22: 478-483.
- Orrell-Valente JK, Jarlsberg LG, et al. At what age do children start taking daily asthma medicines on their own? Pediatrics, 2008; 122: e1186-e1192.
- Bracken M, Fleming L, et al. The importance of nurse-led home visits in the assessment of children with problematic asthma. Arch Dis Child, 2009; 94: 780-784.
- Kamps AW, van Ewijk B, et al. Poor inhalation technique, even after inhalation instructions, in children with asthma. Pediatr Pulmonol, 2000; 29: 39-42.
- Martin AJ, Cambell DA, et al. Characteristics of near fatal asthma in children. Pediatr Pulmonol, 1995; 20: 1-8.
- Sandberg S, Paton JY, et al. The role of acute and chronic stress in asthma attacks in children. Lancet, 2000; 356: 982-987.
- Sandberg S, McCann DC, et al. Positive experiences and the relationship between stress and asthma in children. Acta Paediatr, 2002; 91: 152-158.
- Wright RJ. Further evidence that the wealthier are healthier: negative life events and asthma-specific quality of life. Thorax, 2007; 62: 106-108.
- Simpson JL, Powell H, et al. Clarithromycin targets neutrophilic airway inflammation in refractory asthma. Am J Respir Crit Care Med, 2008; 177: 148-155.
- Payne DN, Hubbard M, McKenzie SA. Corticosteroid unresponsiveness in asthma: primary or acquired? Pediatr Pulmonol, 1998; 25: 59-61.
- Lex C, Payne DN, et al. Is a two-week trial of oral prednisolone predictive of target lung function in pediatric asthma? Pediatr Pulmonol, 2005; 39: 521-527.
- Schatz M, Sorkness CA, et al. Asthma Control Test: reliability, validity, and responsiveness in patients not previously followed by asthma specialists. J Allergy Clin Immunol, 2006; 117: 549-556.
- van Dalen C, Harding E, et al. Suitability of forced expiratory volume in 1 second/forced vital capacity versus percentage of predicted forced expiratory volume in 1 second for the classification of asthma severity in adolescents. Arch Pediatr Adolesc Med, 2008; 162: 1169-1174.
- Nair P, Pizzichini MM, et al. Mepolizumab for prednisone-dependent asthma with sputum eosinophilia. N Engl J Med, 2009; 360: 985-993.
- Humbert M, Beasley R, et al. Benefits of omalizumab as add-on therapy in patients with severe persistent asthma who are inadequately controlled despite best available therapy (GINA 2002 step 4 treatment): INNOVATE. Allergy, 2005; 60: 309-316.
- Bush A, Pedersen S, et al. Pharmacological treatment of severe, therapy resistant asthma in children: what can we learn from where? Eur Respir J, 2011; 38: 947-958.
- Payne DN, Balfour Lynn IM, et al. Subcutaneous terbutaline in children with chronic severe asthma. Pediatr Pulmonol, 2002; 33: 356-361.