Reimatoīdais artrīts (RA) ir izplatītākā un vienlaikus arī viena no nopietnākajām iekaisuma artrīta formām. Neārstēts RA izraisa neatgriezeniskus bojājumus locītavās, funkcionālus traucējumus un saīsina dzīvildzi. Tomēr, pateicoties agrīnai diagnostikai un efektīvām ārstēšanas metodēm, slimību izdodas apturēt un efektīvi ārstēt.
Jo agrāk sāk intensīvu terapiju, jo labāki ārstēšanas rezultāti. Remisija bez medikamentiem, funkcionālās nespējas un klīniski nozīmīgu radiogrāfisku locītavu bojājumu novēršana, dzīves kvalitātes uzlabošana kļuvusi par iespējamu realitāti. Tomēr ir vairāki nosacījumi, kuru īstenošanai būtiska ārstu profesionalitāte.
Lai sāktu agrīnu terapiju, ārstam jāspēj iespējami savlaicīgi atpazīt agrīna iekaisuma artrīta pazīmes. Turklāt agrīnās reimatoīdā artrīta (RA) pazīmes, kas brīdina par iekaisuma artrīta potenciālu progresēt un radīt destruktīvus procesus, jādiferencē no tādām artrīta formām, kas var pāriet spontāni, kā arī slimībām ar artrīta klīniskajai ainai līdzīgām izpausmēm, piemēram, sistēmisko sarkano vilkēdi (SLE) un Šēgrena sindromu.
Izstrādājot izmeklēšanas un ārstēšanas plānu, terapijas kurss jāpiemēro katram pacientam atsevišķi. Ārstēšanas mērķis ir agrīnā iekaisuma apspiešana, lai iespējami ātrāk sasniegtu remisiju un novērstu locītavu bojājumus, invaliditāti un slimības ilgtermiņa komplikācijas. Ārstēšanai jābūt laicīgi sāktai, individuālai un efektīvai. Savlaicīgums padara iespējamu slimības nemedikamentozu remisiju, artrīta simptomu izzušanu un normāla funkcionālā stāvokļa atgūšanu.
Tā kā šāds rezultāts izdodas jau pašreiz, jāsecina, ka RA hroniskā procesa virzība ir ietekmējama.
Agrīnas terapijas nepieciešamība
Lielākajai daļai neārstētu pacientu slimība attīstās un izraisa locītavu bojājumus, funkcionālas problēmas un saīsina dzīvildzi. Spontāna remisija parasti ir retums. Tomēr daži pētījumi liecina, ka stabilu remisiju, nelietojot slimību modificējošus antireimatiskos medikamentus (SMARM), var piedzīvot 10—15 % pacientu ar agrīnu RA.
Locītavu bojājumi un funkciju zudums RA pacientiem sākas slimības agrīnā stadijā.
Radiogrāfisko datu pētījumi liecina, ka pirmajos trīs gados pēc slimības sākuma kaulu erozija attīstās 70 % pacientu ar nesen konstatētu RA. Tomēr 25 % pacientu erozīvas izmaiņas rentgena izmeklējumos redzamas jau trīs mēnešus pēc slimības sākuma.
Jutīgākas attēlveidošanas tehnoloģijas, piemēram, magnētiskā rezonanse (MRI) un muskuloskeletālā ultrasonogrāfija (MSUS), bojājumus uzrāda ievērojami agrāk — vien dažas nedēļas pēc simptomu rašanās. Salīdzinot ar rentgenoloģiskiem izmeklējumiem, MSUS rada iespēju diagnosticēt 1,4 reizes vairāk pacientu ar erozīvām locītavu izmaiņām, bet kaulu eroziju agrīnā RA stadijā izdodas atpazīt pat 60 % pacientu.
Agrīnas radiogrāfiskas erozīvas izmaiņas liecina par locītavu bojājumu progresēšanu. MSUS redzamā kaulu erozija korelē ar vēlāku erozijas attīstību rentgenogrammās. Sākotnējās un agrīnās izmaiņas MRI paredz izmaiņu progresēšanu turpmākajās rentgenogrammās un MRI. Neatkarīgi no lokāla sinovīta magnētiskās rezonanses attēlveidošanas izmeklējumā tieši persistējoša kaulu smadzeņu tūska (nevis sinovīts) norāda uz erozīvu izmaiņu attīstību.
Ja ārstēšanu nesāk agrīnā stadijā, izredzes uz labu rezultātu ir niecīgas. Divpadsmit pētījumu meta–analīzē radiogrāfiskie izmeklējumi RA pacientiem, kuru simptomu ilgums nepārsniedza divus gadus un ārstēšanas kurss ar SMARM bija nokavēts vidēji par deviņiem mēnešiem, uzrādīja būtiskus kaulaudu bojājumus. Ja līdz ārstēšanas sākšanai agrīna artrīta simptomu ilgums pārsniedz 12 nedēļas, tad par 1,3 reizēm palielinās locītavu destrukcijas ātrums nākamajos sešos gados, samazinās iespēja sasniegt remisiju bez zālēm, salīdzinot ar agrīnu ārstēšanas sākšanu līdz 12 nedēļām kopš simptomu parādīšanās.
Simptomu ilgums saistīts ar bojājuma progresēšanu radiogrāfiskos izmeklējumos un mazāku varbūtību ilgstošai remisijai bez SMARM lietošanas. Lai gan pēdējos gados pierādīta SMARM agrīnas lietošanas nozīme, būtiski ir laikus atpazīt pacientus ar iespējamu iekaisuma artrītu. Realitātē reimatologu konsultācijas pacientiem ar agrīnu RA vai spondiloartrītu pamatā ir novēlotas par 18 nedēļām. Tikai 31 % pacientu ar artrīta simptomiem uz konsultāciju pie speciālista nokļūst ne vēlāk kā 12 nedēļas pēc slimības pazīmju parādīšanās.
Iespēju periods
Darbā ar RA pacientiem svarīgākais terapeitiskais mērķis ir aizkavēt un, ja iespējams, novērst nediferencētu artrītu vai ļoti agrīna RA attīstību. Agrīnā slimības stadijā ir ierobežots laiks, kad slimības procesu iespējams ietekmēt vai pat apturēt, pilnībā novēršot destruktīvos procesus.
Salīdzinot ar vēlākiem slimības posmiem, ārstēšanas uzsākšana ar SMARM šajā periodā var būt daudz efektīvāka, tā pārtraucot slimības progresēšanu un reāli ietekmējot ārstēšanas rezultātu. Paredzams, ka jaunu EULAR/ACR kritēriju ieviešana diagnozes noteikšanai var palīdzēt atpazīt agrīnus RA pacientus un iespējami ātrāk sākt terapiju, lai panāktu remisiju un novērstu neatgriezeniskus bojājumus (1. tabula). Lai pacientu klasificētu kā RA pacientu, jābūt ≥ 6/10 klasifikācijas kritērijiem. Ja ir < 6 punkti, kritēriji laika gaitā jāpārskata, lai izvērtētu iespējamu RA attīstību. “Lielā locītava” attiecas uz plecu, elkoņu, gūžu, ceļu, potīšu locītavām, “mazā locītava” attiecas uz metakarpofalangeālām (MKF), proksimālām interfalangeālām (PIF), 2.—5. metatarsofalangeālo (MTF) locītavu, kāju īkšķu interfalangeālajām locītavām un plaukstu pamatņu locītavām.
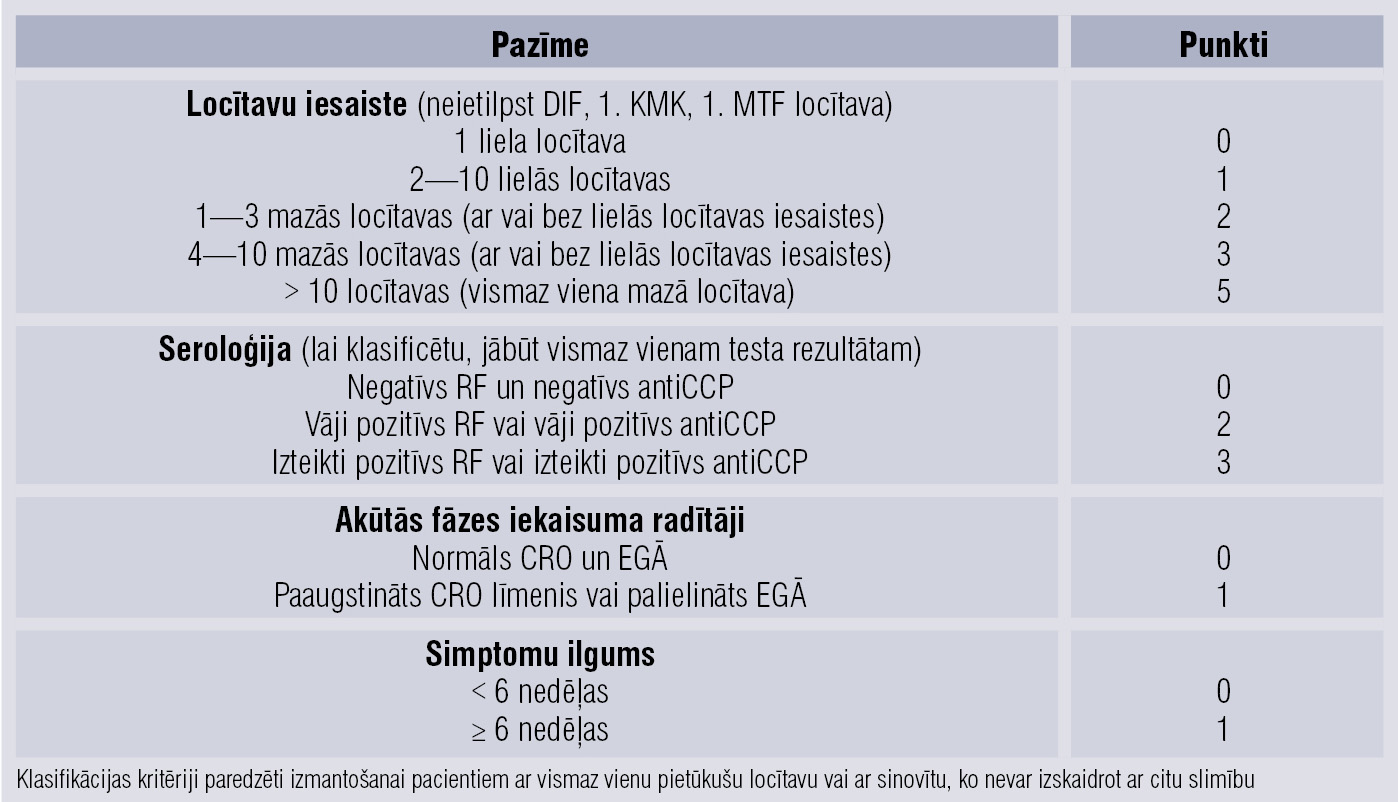

1.tabula
RA klasifikācijas kritēriji, ACR/EULAR, 2010. gads
Pēdējās desmitgadēs pakāpeniski samazinājusies robeža starp agrīnu un izveidojušos RA. RA agrīnais periods iedalīts “ļoti agrīnā RA” ar slimības ilgumu līdz trim mēnešiem un “vēlīni agrīnā RA” ar simptomu ilgumu no trim līdz 12 mēnešiem.
Agrīni atklātas slimības izaicinājumi
Iekaisuma artrīts var sākties vēl labu laiku pirms simptomu parādīšanās. Pieņem, ka RA attīstībā ir vairāki posmi, kas var arī izpalikt. Slimības attīstībai var būt raksturīga gan preklīniska asimptomātika, gan klīniski pārliecinošs nediferencēts artrīts, kā arī RA.
Iedzimtie un vides faktori, dzīvesveids un stohastiskie stimuli spēj ietekmēt nenobriedušo autoantivielu sintēzi pret kādu antigēnu. Ģenētiski predisponētam cilvēkam autoantivielu atbildreakcija pastiprinās tieši pirms artrīta attīstības. To atspoguļo pieaugošie autoantivielu titri. Tomēr nav zināms, vai pacientiem šajā posmā jau ir artralģija.
Vairākas seroloģiskas izmaiņas pacientiem novērotas dažus gadus pirms klīniskā artrīta sākuma. Piemēram, reimatoīdā faktora (RF) klātbūtne un antivielas pret citrulinēto peptīdu (antiCCP), ka arī paaugstināts augsti jutīgo C reaktīvo olbaltumvielu (CRO) līmenis. Strukturālas izmaiņas locītavās bez klīniskā sinovīta pacientiem ar agrīnu RA var konstatēt ar MSUS un artroskopijas palīdzību.
Daļai pacientu ar iekaisuma artrītu tiek noteikta diagnoze “nediferencēts artrīts” — artrīta forma, kas neatbilst klasifikācijas kritērijiem precīzākas diagnozes noteikšanai. Prognoze šiem pacientiem var variēt, diagnozi pirmajos pārraudzības gados var izdoties precizēt. Dažiem pacientiem slimība progresē līdz RA, citiem uzrādās atšķirīgas reimatoloģiskas slimības (2. tabula). Daļai pacientu turpinās nediferencēts artrīts, bet var iestāties arī remisija.
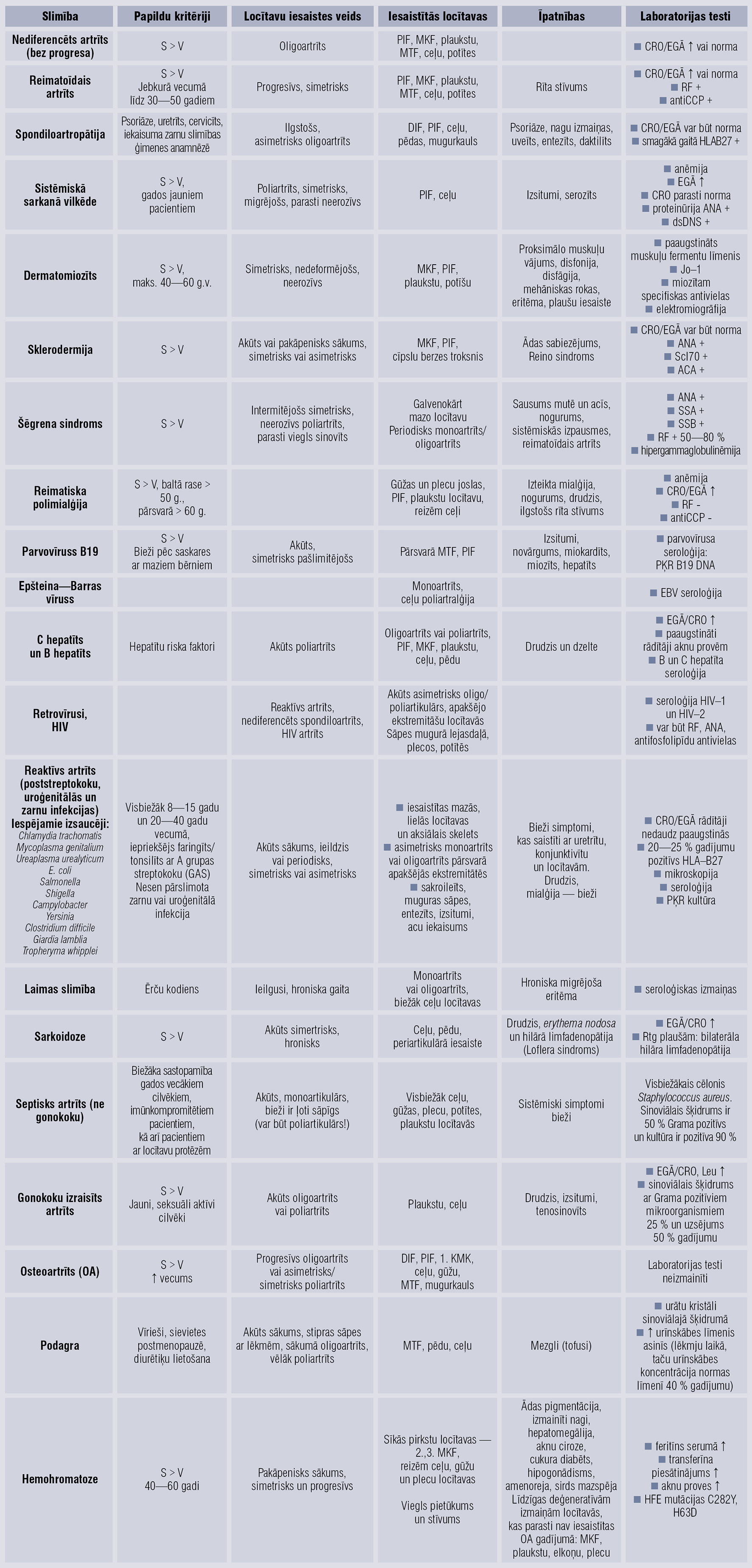

2.tabula
Agrīna artrīta diferenciālā diagnoze
Leidenas agrīnā artrīta klīnikas statistiskie dati liecina, ka 30 % pacientu no visiem pacientiem ar nediferencētu artrītu iestājas remisija, 30 % attīstās RA (pēc 1987. gada ACR kritērijiem), līdz 20 % paliek nediferencēti. Galvenais uzdevums ārstiem, konsultējot nediferencēta vai agrīna artrīta slimniekus, ir pacientus ar pašlimitējošu slimību diferencēt no tiem, kam perspektīvā var attīstīties iekaisuma un erozīvs artrīts. Šī diferenciācija dod iespēju, pirmkārt, sākt piemērotu ārstēšanu pacientiem ar potenciāli progresīvu, erozīvu slimību, otrkārt, izvairīties no nevajadzīgas ārstēšanas pacientiem ar pašlimitējošu slimību.
Kompleksa pieeja artrīta agrīnā diagnosticēšanā
Klīniskā izmeklēšana joprojām ir stūrakmens agrīna artrīta novērtēšanai un palīdz identificēt pacientus ar erozīvas slimības attīstības risku. Izmeklējot pacientu, jānosaka artrīta esība vai neesība, jādiferencē iekaisuma vai neiekaisuma slimības un jānosaka artropātijas etioloģija.
Simptomātiskas izmaiņas locītavā var būt dažādu slimību izpausme, piemēram, infekcijas, iekaisuma vai ļaundabīgā audzēja.
Anamnēze jādokumentē, tajā iekļaujot precīzu simptomātisku locītavas izmaiņu aprakstu, simptomu ilgumu, rīta stīvuma ilgumu, atbildreakciju uz nesteroīdajiem pretiekaisuma līdzekļiem, pavadošo slimību sarakstu un saistītos simptomus. Izvērtējot pacientu, jāiepazīstas ar individuālo slimību vēsturi un dzīvesveidu. Tomēr ne vien pacienta, bet arī ģimenes anamnēze ir vienlīdz svarīga, ārstējot RA, psoriāzes un citu autoimūno slimību pacientus. Ārstam vispusīgi jāizmeklē visas pacienta sistēmas un orgāni. Laboratorijas izmeklējumi un vizualizācija sniedz papildu datus agrīna artrīta diagnozes un prognozes noteikšanai. Liela nozīme ir rezultātu pareizai interpretācijai, piemēram, testa rezultātu atbilstība normai vēl neapstiprina, ka slimības nav. Būtiski izvērtēt arī radioloģisko izmeklējumu rezultātus. Pirmreizējie pacienti ar iekaisuma artrīta simptomiem agrīnā slimības stadijā noteikti jānosūta pie speciālista, ideālā gadījumā — ne vēlāk kā sešas nedēļas pēc simptomu rašanās. Būtiski zināt, ka daļai pacientu, kam ar laiku attīstās smags persistējošs iekaisuma artrīts, testu rezultāti slimības sākumā ir normāli vai negatīvi. Tāpēc visi pacienti ar iekaisuma artrīta simptomiem neatkarīgi no asins analīžu rezultātiem vai radioloģiskām atradēm jānosūta pie reimatologa.
Nediferencēts artrīts un agrīni diagnosticēts RA
Pacientiem ar agrīnu artrītu bieži notiek spontāna sinovīta remisija (īpaši gadījumā, ja simptomi nav bijuši ilgāk par trim mēnešiem). Jāsecina: ja visus pacientus ar agrīnu sinovītu ārstē pēc vienota plāna, daļu cilvēku pakļauj nevajadzīgai un potenciāli toksisku medikamentu lietošanai. Tāpēc ir tik būtiski pašlimitējošas slimības atšķirt no ieilgušiem sinovītiem ar pāreju līdz attīstītam RA.
Sieviešu dzimums, smēķēšana, simptomu ilgums, sāpīgo un pietūkušo locītavu skaits, simptomu parādīšanās plaukstu locītavās, izmaiņas iekaisuma radītāju līmenī, RF un antiCCP, atbilstība 1987. gada ACR klasifikācijas kritērijiem par RA (jutība 88 %, specifiskums 73 %) ir faktori, kas norāda uz slimības ieilgšanu.
Alternatīva pieeja ir diferencēt pacientus ar artrītu, kuriem ir potenciāls sasniegt spontānu agrīnu remisiju. Seronegativitāte pēc RF un neliels iekaisušo locītavu skaits agrīnā RA stadijā var liecināt par remisijas iespēju.
Slimības ilgumu un smaguma pakāpi ietekmējošie faktori
Faktori, kas prognozē slimības ieilgšanu agrīna artrīta gadījumā:
- sieviešu dzimums,
- simptomu ilgums (ilgāk par 12 nedēļām),
- liels sāpīgo un pietūkušo locītavu skaits,
- simptomu parādīšanās plaukstas locītavās,
- smēķēšana,
- paaugstināti akūtās fāzes rādītāji,
- pozitīvs RF,
- pozitīvas antiCCP,
- erozijas rentgenogrammās.
Faktori, kas prognozē slimības smagumu agrīna artrīta gadījumā:
- sieviešu dzimums,
- liels sāpīgo un pietūkušo locītavu skaits,
- augsts HAQ indekss (pēc veselības novērtējuma anketas),
- paaugstināti akūtās fāzes rādītāji,
- pozitīvs RF,
- pozitīvas antiCCP,
- dalīta epitope,
- erozijas rentgenogrammās.
Paaugstināti akūtās fāzes rādītāji
Akūtās fāzes rādītāju līmeņa paaugstināšanās, piemēram, EGĀ un CRO, liecina par iekaisuma pakāpi. EGĀ un CRO kombinācija sniedz noderīgu informāciju, kas bieži vien nav skaidra, ja izmanto tikai vienu no testiem.
Paaugstināts autoantivielu līmenis
Pacientiem ar iekaisuma artrītu pozitīvs RF ir viens no pastāvīgas slimības ieilgšanas un radioloģiskā bojājuma progresēšanas rādītājiem. Turklāt augsti RF titri atzīti par invaliditātes prognozes rādītāju.
AntiCCP līmenis var būt paaugstināts slimības agrīnā stadijā, antivielas var būt pozitīvas pat desmit gadus pirms simptomu parādīšanās. AntiCCP uzrāda risku saslimt ar RA pacientiem ar nediferencētu artrītu vai artralģiju. Pierādīts, ka antiCCP klātbūtne ir neatkarīgs rādītājs iekaisīga poliartrīta un RA izraisītu radiogrāfisku bojājumu un to progresēšanas diagnostikai. Lai gan antiCCP un RF diagnostiskā nozīme nav noliedzama, dažiem pacientiem ar iekaisuma artrītu slimību tomēr var klasificēt kā seronegatīvu RA.
Šobrīd atklātas vairākas citas autoantivielas, kas saistītas ar RA, piemēram, antivielas pret karbamilētiem antigēniem (antiCarP). Šīs autoantivielas atpazīst karbamilētus, bet ne citrulinētus proteīnu antigēnus. IgG antiCarP un IgA antivielas pret CarP atklātas 16 % un 30 % iekaisuma artrīta pacientu ar negatīvu antiCCP. AntiCarP antivielas konstatētas pacientiem ar antiCCP negatīvu, kā arī ar antiCCP pozitīvu RA, gan arī slimības preklīniskajā fāzē.
Smēķēšana
Smēķēšana ir būtiskākais vides riska faktors RA attīstībai. Ir cieša saikne starp smēķēšanu un ārpus locītavu izpausmju palielināšanos, ieskaitot reimatoīdos mezgliņus agrīnā seropozitīvā RA. Pētījumi sniedz priekšstatu par smēķēšanas potenciālo lomu RA patoģenēzē. Pierādīts, ka smēķēšana palielina anti–CCP attīstības risku. HLA–DRB1 SE allēļu klātbūtnē šis risks pieaug līdz 20 reizēm homozigotās, salīdzinot ar SE negatīviem nesmēķētājiem starp anti–CCP pozitīviem cilvēkiem. Tas liecina, ka smēķēšana ģenētiski predisponētam indivīdam izraisa apoptozi un proteīna citrulenizāciju, kam seko anti–citrulīnam specifiskā imūnā atbildreakcija. Bijušajiem smēķētājiem lielāka iespēja saslimt ar RA ir 20 gadus pēc smēķēšanas atmešanas, bet šis risks laika gaitā pakāpeniski samazinās.
Attēldiagnostika
Rentgenogrāfiskas erozijas ir ļoti specifiskas pašlimitējoša un ieilguša artrīta atpazīšanai. Agrīnas radiogrāfiskas pārmaiņas liecina par slimības progresēšanu. Rentgenogrāfisks bojājums sākotnējā stadijā ir pamatots prognozes faktors izteiktākam strukturālam bojājumam perspektīvā. Locītavas erozija un locītavas spraugas sašaurināšanās, kas redzamas rentgena izmeklējumos, liecina par jau progresējušu slimību, nevis tās sākumu. Jaunākās attēlveidošanas metodes RA agrīnā stadijā nodrošina uzticamāku diagnostisko informāciju.
MRI var novērtēt visu iekaisuma locītavas struktūru. Sinovīta un eroziju noteikšanai agrīnā RA stadijā MRI ir precīzāka par klīnisko izmeklēšanu un jutīgāka par rentgenogrāfiju. Pierādīts, ka MRI rezultāti (sinovīts, kaulu tūska un kaulu erozijas) var palīdzēt ārstam prognozēt turpmāku rentgenogrāfisko progresēšanu. Tomēr jāpatur prātā, ka arī veselīgu indivīdu locītavās dažreiz atrodamas pārmaiņas, kas atgādina vieglu sinovītu vai kaulu eroziju. Nesens literatūras pārskats par 31 MRI pētījumu uzrāda MRI īpatnības cilvēkiem bez slimības simptomiem. MRI erozija konstatēta 33—52 % veselu cilvēku, sinovīts — 27 %, kaulu tūska — 16 %.
Pēdējos gados pacientus ar agrīnu artrītu arvien biežāk izmeklē ar MSUS. Tā ir noderīga metode, lai identificētu sinovītu mazajās plaukstu un pēdu locītavās. Salīdzinot ar parastu radiogrāfiju, MSUS ir jutīga metode sinovīta un kaulu eroziju vizualizācijai pirkstu locītavās. MSUS procedūra ir neinvazīva, vienlaikus ļauj novērtēt daudzu locītavu stāvokli. Galvenie izmeklējuma trūkumi — attēla reproducēšanas kvalitāte un apstāklis, ka datu uzticamība atkarīga no speciālista zināšanām un prasmēm attēla interpretēšanā.
Jāatzīmē, ka MSUS atrades ir diezgan izplatītas veseliem cilvēkiem: 88 % konstatē izmaiņas bez locītavu simptomiem. Ir svarīgi MSUS atrades interpretēt piesardzīgi un vienmēr klīniskās situācijas kontekstā. Pacientiem ar RA MSUS atrades gan lielajās, gan mazajās locītavās atspoguļo sinoviālās histoloģijas rezultātus, DAS28 un CRO.


3.tabula
ACR/EULAR RA remisijas kritēriji
Ārstēšanas principi
Agrīni diagnosticēts artrīts jāārstē savlaicīgi un efektīvi, farmakoloģiski un nefarmakoloģiski. Jāārstē, lai sasniegtu mērķi (treat to target — T2T), lai stingri kontrolētu slimības aktivitāti. Praksē tas nozīmē slimības aktivitātes kontroli un ārstēšanas pielāgošanu, ja vien nav sasniegts iepriekš noteiktais slimības aktivitātes mērķis — ideālā remisija (3. tabula, attēls).
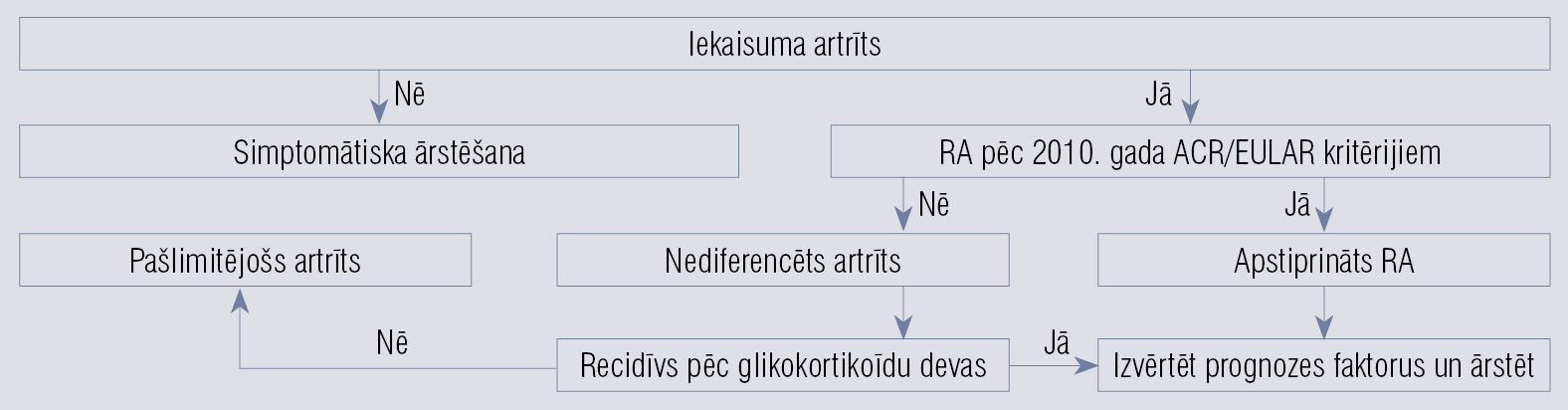

Attēls
Agrīna iekaisuma artrīta ārstēšanas algoritms
Ārstēšanas stratēģijas — praktiskie aspekti
- Nefarmakoloģiska ārstēšana un atbilstīga dzīvesveida ievērošana. Smēķēšanas atmešana un svara samazināšana pacientiem ar lieko svaru var labvēlīgi ietekmēt ne vien artrīta ārstēšanas gaitu, bet arī samazināt sirds—asinsvadu sistēmas slimību attīstības risku.
- Efektīvas ārstēšanas savlaicīga sākšana ir agrīna artrīta ārstēšanas stūrakmens. Novēlota ārstēšana var būt efektīva vienīgi pacientiem, kuru slimības gaita ir ļoti viegla un simptomu ilgums nepārsniedz trīs mēnešus. Šādiem pacientiem var izrakstīt vienu intramuskulāri ievadāmu steroīdu devu. Ieildzis artrīts, kura gaita pārsniedz 12 nedēļas, reti mēdz pāriet spontāni. Vairākumam šo pacientu attīstīsies RA. Pacientiem, kam ir ieilguša vai erozīva artrīta risks, jāsāk lietot SMARM.
- Samērīgi riska/ieguvuma attiecībai uzskata, ka sākotnējā artrīta stadijā jāsāk ar konvencionālajiem sintētiskajiem SMARM, ar NSPL un glikokortikoīdiem kā papildlīdzekļiem. Pirmais vēlamais SMARM lielākoties ir metotreksāts. Citi SMARM, piemēram, sulfasalazīns vai leflunomīds, ir piemērotas alternatīvas.
- Pacientiem ar ievērojamu slimības aktivitāti un sliktas prognozes riska faktoriem, piemēram, augstu RF vai anti–CCP, jau agrīni jāizmanto intensīvāka stratēģija — trīskārša (kombinēta) terapija vai jākombinē metotreksāts un bioloģiskās zāles.
- Remisijas indukcija, īslaicīgi lietojot bioloģisko SMARM, remisijas uzturēšana ar konvencionāliem SMARM un turpmāka medikācijas samazināšana un preparāta pārtraukšana pēc stabilas remisijas sasniegšanas ir potenciāla terapeitiskā stratēģija nākotnei.