Streptococcus pneumoniae joprojām ieņem galveno lomu dažādu infekcijas slimību etioloģijā. Pneimokoka izraisītās komplikācijas ir viens no galvenajiem nāves iemesliem pacientiem dažādās vecumgrupās visā pasaulē. Šis mikroorganisms ir oportūnists un izmanto savu iespēju, kad saimniekorganisms ir novājināts, un rada vai nu lokālu iekaisumu, agravējas uz dziļajiem elpceļiem, vai diseminējas sistēmiski.
Kāda ir situācija Latvijā un kādas ir aktuālās vadlīnijas uzraudzībai, diagnostikai, ārstēšanai un profilaksei? Par to 2022. gada 6. oktobrī profesionālās pilnveides konferencē “Pneimokoku infekcijas epidemioloģiskie, klīniskie, laboratorie, terapeitiskie un profilakses aspekti 21. gadsimta skatījumā” informēja nozares vadošie eksperti.*
Streptococcus pneumoniae — klīniski nozīmīgs diplokoks
Epidemioloģija un slimības slogs
Pneimokoks ir fakultatīvi anaerobs Grama pozitīvs mikroorganisms, ar kuru cilvēce sadzīvo visu pastāvēšanas laiku, tomēr speciālisti uzsver tā bīstamību gan no klīniskā viedokļa, gan pieaugošās antibakteriālās rezistences dēļ.
Pesimistiskākie scenāriji rāda, ka 2050. gadā pret antibiotikām rezistents Str. pneumoniae varētu laupīt desmit miljonus cilvēku dzīvību!
Tikpat būtiski uzsvērt invazīvās pneimokoku slimības (IPS; meningīts, sepse) nozīmi sabiedrības veselībā: IPS šobrīd ir trešajā vietā pasaulē aiz gripas un tuberkulozes pēc DALY rādītāja (viens potenciāli zaudēts veselīgas dzīves gads).
Latvijā IPS izplatības rādītājus apkopo SPKC (1. attēls), pēdējos desmit gados ziņots par vidēji 69 pneimokoku infekcijas gadījumiem gadā. Neliela atšķirība dzimumiem: 40 % sieviešu, 60 % vīriešu; ļoti plašs inficēto vecuma diapazons: no zīdaiņa līdz 95 gadiem. Visvairāk slimo bērni zem gada vecuma un seniori 65+.
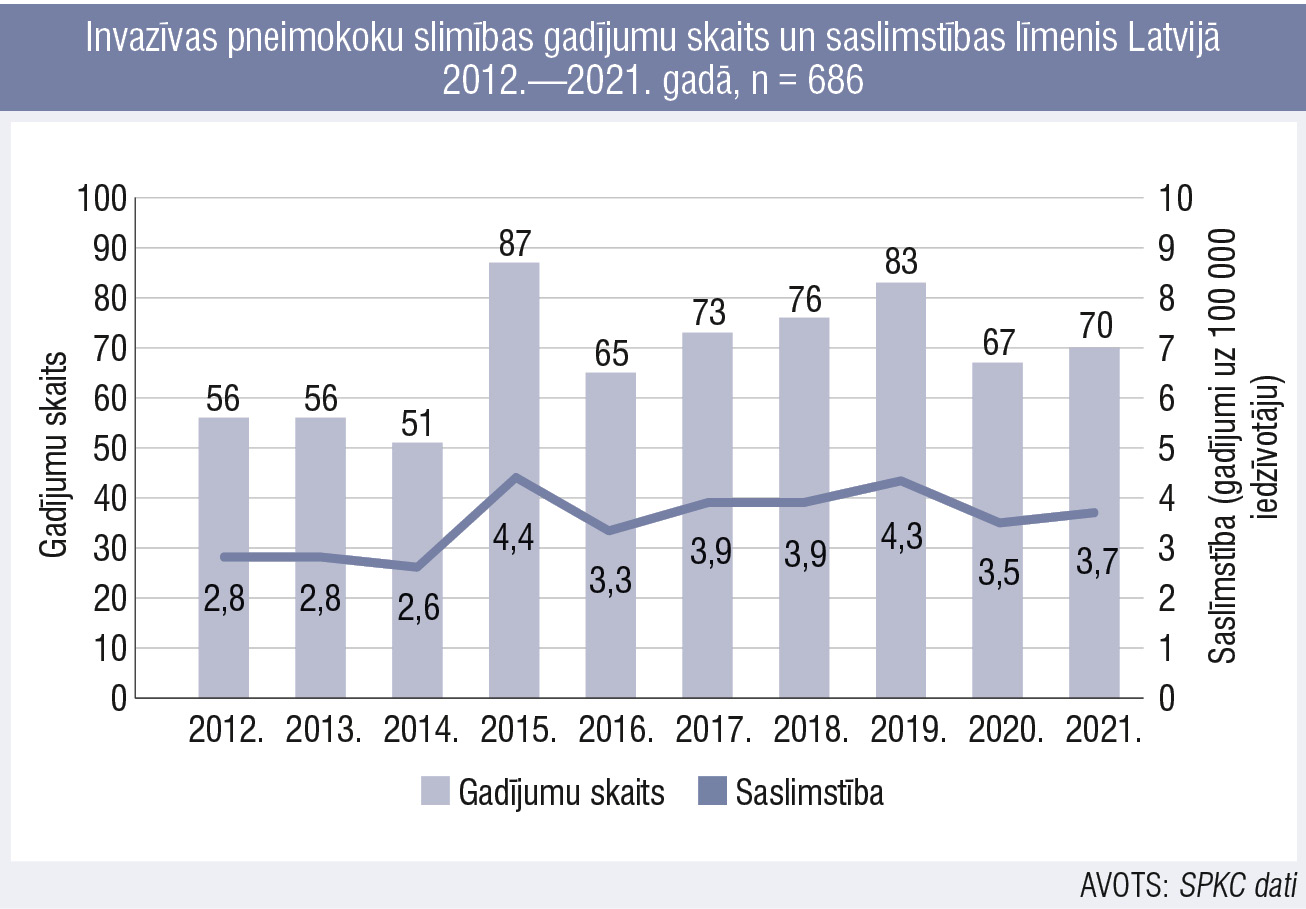

1. attēls
Invazīvas pneimokoku slimības gadījumu skaits un saslimstības līmenis Latvijā 2012.—2021. gadā, n = 686
Ja analizē IPS klīniskās izpausmes, tad Latvijas apstākļos galvenais klīniskais sindroms ir sepse (78,6 % gadījumu), tālāk seko meningīts (17,5 %), tāpat ir fiksēti smagas Str. pneumoniae izraisītas pneimonijas gadījumi un meningīts ar septicēmiju. Desmit gados konstatēti 120 nāves gadījumi (īpatsvars 17,5 %). Izgaismojas letalitātes riska vecumgrupas: 65+ (19,9 %) un 15—64 gadi (17,3 %), turklāt fiksēts arī viens nāves gadījums bērnam vecumgrupā 1—4 gadi (5,3 %), kas ir vienīgais šāds gadījums pēdējo desmit gadu uzraudzības periodā. Šā brīža imunizācijas rādītāji varētu būt labāki: 2021. gadā vakcināciju pret pneimokoku iesākuši 93,1 % bērnu, pabeiguši 91,8 %.
Diagnostika un serotipēšana
Ir pieņemts, ka atbilstīgs diagnostiskais materiāls ir sterili paņemtas venozās asinis vai cerebrospinālais šķidrums. Kā diagnostisku papildu metodi izmanto urīna antigēna testu.
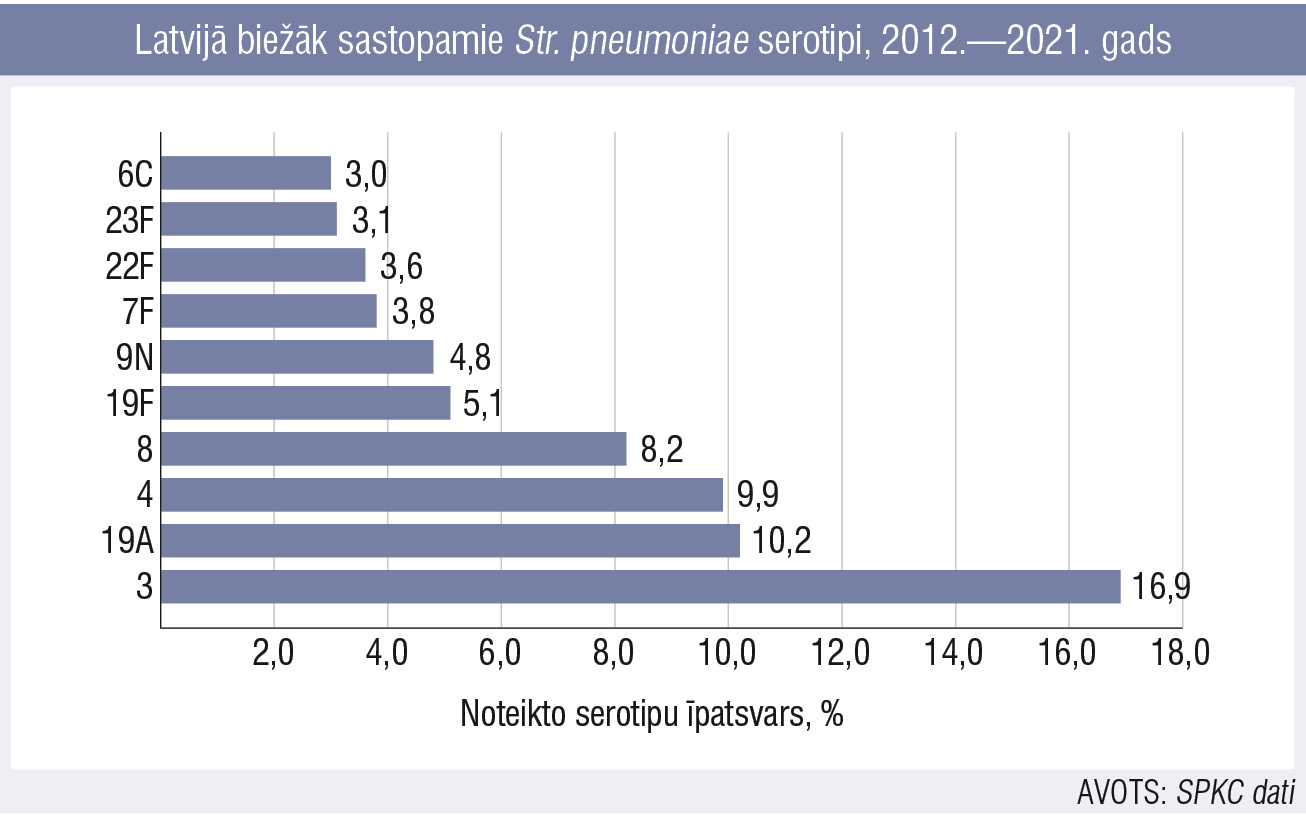

2. attēls
Latvijā biežāk sastopamie Str. pneumoniae serotipi, 2012.—2021. gads
Izaicinājumi pneimokoku infekciju laboratoriskajā diagnostikā ir paraugņemšanas process un organizatoriskais darbs, jo 2—4 stundas pēc parauga paņemšanas materiālam jānonāk analizatorā. Pneimokoks ir kaprīzs mikroorganisms, neaugs visos piedāvātajos apstākļos, tāpēc šīm 2—4 stundām ir būtiska nozīme, paraugs ātri lizējas. Un, ja ir jau sākta antibakteriālā terapija, pastāv liela iespēja, ka pneimokoku vairs neizgūsim. Desmit gados izdevies serotipēt 88,6 % no visiem paraugiem. Līderis — 3. serotips (2. attēls), kurš nav iekļauts PCV10 pneimokoku vakcīnā, tāpat kā 19A serotips. Novērojam, ka PCV10 vakcīnas ietekmē pamazām mazinās to izdalīto serotipu īpatsvars, kuri ir šīs vakcīnas sastāvā.
Infekcijas klīniskās formas antibakteriālās rezistences ēnā
Ar pneimokoku infekciju var saslimt jebkurā vecumā, bet vislielākajam riskam pakļauti bērni līdz divu gadu vecumam un pieaugušie pēc 65 gadu vecuma. Biežāk izraisītās slimības ir sinusīts, vidusauss iekaisums, pneimonija, smagākos gadījumos — meningīts vai sepse.
Sinusīts pieaugušo populācijā
Ar deguna un deguna blakusdobumu gļotādas iekaisumu jeb rinosinusītu (RS) katru gadu slimo ap 16 % populācijas. RS ir viens no pieciem biežākajiem antibiotiku izrakstīšanas iemesliem un viens no iemesliem, kāpēc veidojas antibakteriālā rezistence.
Akūts bakteriāls rinosinusīts
Viens no ierosinātājiem — Str. pneumoniae (20—43 % gadījumu). Par diagnozi domājam, ja ir šādi simptomi:
- drudzis virs 38 ℃,
- izteiktas lokālas sāpes sinusu projekciju zonās,
- simptomi vienā pusē,
- paaugstināts CRO līmenis vai palielināts EGĀ,
- anamnēzē pēc īslaicīga uzlabojuma atkārtota saslimšana — it kā atveseļošanās, bet tad straujš pasliktinājums.
Nav jāpievērš uzmanība gļotu krāsas izmaiņām, jo konstatēts, ka arī virāla RS gadījumā izdalījumi trešajā dienā var kļūt dzeltenīgi vai zaļgani.
Ārstēšana
Vīrusa RS gaita ir pašlimitējoša. Bakteriāla RS gadījumā pirmā izvēle ir amoksicilīns vai amoksicilīns/klavulānskābe (500/125 mg × 3 dienā vai 875/125 mg × 2 dienā), terapijas ilgums 5—10 dienas. Makrolīdi un trimetoprims—sulfametoksazols nebūtu jāizvēlas augstā Str. pneumoniae un H. influenzae rezistences riska dēļ.
Komplikāciju risks un “sarkanā karoga” simptomi
Otorinolaringologa apskate steidzamā kārtā nepieciešama tad, ja pacientam attīstās periorbitāla tūska/apsārtums, ir redzes dubultošanās, oftalmoplēģija, redzes asuma izmaiņas, spēcīgas galvassāpes, tūska pieres/uzacu rajonā, meningīta pazīmes, neiroloģiskā simptomātika.
Rinosinusīti bērniem
Jāpievērš uzmanība anatomiskajām atšķirībām, jo bērni piedzimst ar augšžokļa dobumu un nedaudz etmoidālajiem dobumiem, tikai 6—7 gadu vecumā sāk attīstīties pieres un citi dobumi. Tāpat arī bērniem adenoīdi bieži vien ir pneimokoku rezervuārs, kas attiecīgi var pasliktināt klīnisko gaitu. Tātad vakcinācija nepieciešama arī tādēļ, lai mazinātu kādu potenciālu komplikāciju attīstību.
Bērniem ir vairāki riska faktori, kuru dēļ varētu attīstīties bakteriāls rinosinusīts. Būtiskākie — alerģija, atviļņa slimība un adenoīdi.
Bērnu populācijā tikai 0,5—2 % no vīrusu izraisītiem akūtiem RS komplicējas ar bakteriālu infekciju. Pirmajās 3—4 saslimšanas dienās diferenciāldiagnoze praktiski nav iespējama, 5.—10. dienā svarīga slimības dinamika, jo stāvokļa pasliktināšanās var liecināt par bakteriāla sinusīta sākumu.
Pazīmes, kas liecina par potenciālu bakteriālu RS, ir iesnas ilgāk par desmit dienām ar klepu dienas laikā (un pasliktinājumu naktī), iesnas nemazinās un stāvoklis neuzlabojas. Ir smagi simptomi (paaugstināta ķermeņa t° > 39 ℃ vismaz trīs dienas) vai simptomi pasliktinās.
Ārstēšana bakteriālas infekcijas gadījumā
Antibiotiku devu rēķina pēc svara, līdz bērns sasniedz 35—40 kg. Amoksicilīns, amoksicilīns/klavulānskābe vai klaritromicīns ir biežāk lietotās antibiotikas bērniem LOR patoloģijas dēļ.
Vidusauss iekaisums pieaugušajiem
Ap 26 % gadījumu novēro primāru bakteriālu infekciju vidusauss gļotādā pieaugušajiem. Viens no biežākajiem izraisītājiem — Str. pneumoniae, tad H. influenzae, M. catarrhalis, arī A grupas streptokoki — retāk, atsevišķās pacientu grupās.
Klīniskā aina un terapija
Vidusauss iekaisums pieaugušajiem ir salīdzinoši reti, parasti pēc akūtas vīrusinfekcijas. Sākas ar aizliktas auss sajūtu, spiedienu ausī, ātri pievienojas sāpes. Paaugstinātu temperatūru novēro reti, tikpat reti pārmaiņas iekaisuma rādītājos analīzēs. Diagnostikas pamatā anamnēze un otoskopija.
Pieaugušajiem retāk nekā bērniem izmanto taktiku “novērot + nogaidīt”. Ja domājam par bakteriālu ģenēzi, antibakteriālai terapijai jābūt vērstai uz biežākajiem bakteriālajiem izraisītājiem. Pirmā izvēle — penicilīnu grupas antibiotiķi (pārsvarā amoksicilīns) atbilstošā devā desmit dienas un pretsāpju terapija sistēmiski.
Komplikācijas — intratemporālas vai intrakraniālas
Intratemporālās komplikācijas:
- akūta sensorineirāla vājdzirdība,
- akūts labirintīts,
- n. facialis parēze,
- mastoidīts,
- sinus sigmoideus tromboze (reta komplikācija).
Intrakraniālās komplikācijas: meningīts, encefalīts, intrakraniālie abscesi, kad pacients jāstacionē un stāvoklis jāstabilizē.
Vidusauss iekaisums bērniem
Viena no biežākajām infekcijas slimībām bērna vecumā. Līdz četru gadu vecumam vismaz 60 % bērnu bijis vismaz viens vidusauss iekaisuma gadījums. Tas ir arī viens no biežākajiem antibiotiku izrakstīšanas iemesliem bērniem līdz trīs gadu vecumam, taču pat ½ gadījumu nepamatoti, jo ierosinātāji ir gan baktērijas, gan vīrusi.
Jaukta vīrusu—bakteriāla flora ir 66 % gadījumu, tikai bakteriāla flora — 27 %, biežākie bakteriālie ierosinātāji Str. pneumoniae, H. influenzae, M. catarrhalis, Str. pyogenes.
Ir zināmi riska faktori infekcijas attīstībai: mazs bērna vecums, kontakts ar citiem maziem bērniem (bērnudārzā, mājās), sejas—žokļa īpatnības, kā arī ietekmējamie riska faktori: pasīvā smēķēšana, māneklīša lietošana, GERS, imūndeficīti, barošanas īpatnības (resp., mātes pienam ir aizsargājoša nozīme), akūti vidusauss iekaisumi ģimenes anamnēzē.
Kad sākt terapiju ar antibiotikām?
Ir divas terapijas taktikas: novērošana vai tūlītēja antibakteriāla ārstēšana, ja ir perforācija, otoreja vai smaga klīnika. Galvenie kritēriji taktikas izvēlei ir pacienta vecums, abpusēja vai vienpusēja iesaiste, perforācija/otoreja, pacienta aprūpētāju uzraudzības un sapratnes līmenis.
Korekta akūta vidusauss iekaisuma diferencēšana no sekretora vidusauss iekaisuma ir ļoti svarīga, lai nepieļautu nepamatotu antibakteriālo līdzekļu nozīmēšanu. Lai noteiktu diagnozi, jābūt anamnēzei ar akūtu sākumu un sūdzībām par sāpēm ausī, iekaisuma un izsvīduma pazīmēm vidusausī vai otorejai bez ārējās auss ejas iekaisuma pazīmēm.
Pirmās izvēles preparāts vidusauss iekaisuma ārstēšanā ir amoksicilīns, terapijas efektivitāti izvērtē pēc 48—72 h. Jāizvairās no trimetoprima—sulfametoksazola lietošanas rezistences dēļ, kā arī makrolīdiem, jo novērota ierobežota šo preparātu efektivitāte pret pneimokoku un H. influenzae.
Komplikācijas un LOR iesaiste
Komplikācijas bērniem vidusauss iekaisuma gadījumā novēro reti, bet to dēļ bērns ir jāstacionē: akūts mastoidīts, labirintīts, n. facialis parēze, intrakraniālas komplikācijas, sepse.
LOR konsultācija klātienē nepieciešama tad, ja ārstēšanas iznākums neveiksmīgs, ja bērnam ir kohleārs implants un ja ir jāizvērtē indikācijas timpanostomijai.
Invazīvās pneimokoku slimības — augsta mirstība
IPS grupai pieskaita pneimokoku meningītu, bakteriēmiju (sepsi), kā arī smagākos pneimokoku pneimonijas gadījumus. Augstākā mirstība — pacientiem ar meningītu.
Pētot, cik daudzi nonāk intensīvajā terapijā un ir nepieciešama orgānu atbalsta terapija, Francijas kolēģi veikuši observācijas pētījumu, kur no 182 858 gada laikā hospitalizētiem pneimonijas pacientiem pneimokoks bija izsaucējs 10 587 pacientiem jeb 5,8 %; intensīvā terapija bija nepieciešama 1665 no šiem pacientiem (15,7 %), bet 379 (22,8 %) nomira. Tātad mirstība ir augsta —katrs piektais intensīvajā terapijā nonākošais neizdzīvo.
IPS gadījumā ir zināmi riska faktori, kas veicina invāziju: vecums < 2 g. un > 65 g., virāla infekcija fonā, alkohola ļaunprātīga lietošana, smēķēšana, HOPS, imūnsupresija.
Biežāk ITN nonāk vīrieši, hroniski alkohola lietotāji, smēķētāji. Taču ļoti svarīgi uzsvērt, ka neliela daļa (~ 5 %) būs bez blakusslimībām un prognozi noteiks pacienta vecums, blakusslimības, slimības gaita, antibakteriālās terapijas efektivitāte.
Kādas IT metodes visbiežāk nepieciešamas?
- Mehāniska plaušu ventilācija.
- Terapija ar vazopresoriem.
- Nieru aizstājterapija.
Pneimonijas bērnu populācijā
Pneimonija katru gadu ir nāves cēlonis > 2 miljoniem bērnu vecumā no 28 dienām līdz pieciem gadiem (~ 20 % letālo iznākumu bērniem šajā vecumgrupā). Str. pneumoniae ir visbiežākais sadzīvē iegūtas bakteriālas pneimonijas izraisītājs bērniem.
60 % bērnu ir asimptomātiski nēsātāji, lai gan vakcinēti. Būtiski atzīmēt, ka, piemēram, Str. pneumoniae sastopamība ASV mazinājās pēc PCV7 vakcīnas nomaiņas uz PCV13.
Riska faktori attīstībai
Imūnkompromitējoši stāvokļi, hroniskas slimības, SIP vispārējie riska faktori (zems sociālekonomiskais stāvoklis, zems mātes izglītības līmenis, slikta aprūpes pieejamība, piesārņojums, cigarešu dūmi, apreibinošu vielu lietošana pusaudžiem).
Klīniskā aina
Bērnam ar pneimoniju:
- drudzis,
- respiratoriskās pazīmes — sauss klepus, tahipnoja,
- izmainīts aktivitātes līmenis (letarģija, uzbudinājums),
- ādas krāsa — cianoze, perorāla cianoze,
- krūškurvis — tahipnoja, dispnoja, retrakcijas, palīgmuskulatūras iesaiste,
- auskultatīva atrade (var būt arī bez patoloģijas!) — krepitācija, sēkšana, bronhiālas skaņas,
- vitālie rādītāji — svarīgi! Bērnus ar SpO₂ 92 % stacionē, nodrošina O₂ atbalstu ar kanilēm/masku.
Ārstēšanas taktika
Terapijā svarīga i/v rehidratācija un empīriska antibakteriāla terapija. Jāņem vērā, ka pneimokoku pneimonijas pacienti vēl ir infekciozi 24 h pēc antibakteriālās terapijas sākšanas. Ambulatori pirmā izvēle ir amoksicilīns, alternatīvas — amoksicilīns/klavulānskābe, cefaklors, azitromicīns, klaritromicīns.
Pneimokoku pneimonijas komplikācijas
Attīstās 40—70 % pacientu, kas ārstējas stacionārā. Biežāk novērotās:
- pleiras izsvīdums (36—83 %),
- empiēma (49—52 %),
- nekrotizējoša pneimonija (31 %),
- plaušu abscess (5 %),
- pneimatocēle (19 %),
- pneimotorakss (10 %).
Tāpat ir risks infekcijas diseminācijai (sepse, endokardīts, meningīts), hiponatrēmijai. Literatūrā aprakstītas arī kardioloģiskās komplikācijas.
Pneimonija pieaugušo populācijā
Ir zināma lielākā daļa faktoru, kuri vājina dziļo elpceļu aizsargmehānismu: smēķēšana, auksta vai karsta gaisa, kaitīgu gāzu ieelpošana, elpceļu vīrusinfekcijas, iedzimti skropstiņepitēlija funkciju traucējumi, vecums, hroniskas slimības, mazkustīgums.
Imūnkompetentiem pacientiem pneimonijas izraisītāji ir tipiskās baktērijas (Str. pneumoniae, H. influenazae, M. catarrhalis u.c.), atipiskās baktērijas (Mycoplasma pneumoniae, Chl. pneumoniae, Legionella spp.), vīrusi (SARS–CoV–2, A un B tipa gripas vīrusi, rinovīrusi u.c.).
Kopējā pneimokoku pneimonijas sastopamība vakcinācijas dēļ ir mazinājusies, tomēr pneimokoks izraisa 10—15 % sadzīvē iegūtu pneimoniju ASV un 30 % Eiropā.
Klīniskā aina un ārstēšana
Pacients sūdzēsies par elpošanas sistēmas simptomiem: klepu ar vai bez krēpām, tahipnoju, palielinātu elpošanas darbu, pleirītiskām sāpēm, sistēmiskiem simptomiem; var būt izklausāmi trokšņi plaušās.
Antibakteriālā terapija jāizvēlas gudri, jo vēlamies izvairīties no potenciālas antibakteriālās rezistences. Ambulatori ārstētiem pacientiem tas ir amoksicilīns 1 g × 3 dienā vai doksiciklīns 100 mg × 2 dienā, vai amoksicilīns/klavulānskābe 875/125 mg × 2 dienā + klaritromicīns 500 mg × 2 dienā, ja nopietnas blakusslimības.
Ja simptomi pēc 5—7 dienām izzūd, atkārtot Rtg nav nepieciešams. NB! 1,3—4 % pēc pneimonijas ārstēšanas DT konstatē malignitāti, tāpēc būtiski aizdomāties, varbūt tomēr pacientam ar plaušu vēža riska faktoriem pēc pneimonijas izārstēšanas izmeklējumu veikt.
Svarīgākā pneimokoku profilakses daļa — vakcinācija
Kāpēc bija un ir nepieciešama vakcīna?
- Augsta saslimstība un mirstība (IPS). Tajā pašā laikā tas ir arī normālās deguna un aizdegunes mikrofloras sastāvdaļa, bērni ir nēsātāji.
- Nav surogātmarķiera — nav antivielu, ko noteikt, arī diagnostika ir sarežģīta, tāpēc daļa gadījumu paliek nediagnosticēti.
- Grūti atpazīt, nav specifisku pneimokokam raksturīgu simptomu.
- Grūti ārstēt, antibakteriālas rezistences riski.
- Svarīga agrīni sākta mērķtiecīga terapija.
Pneimokoki ir labi nodrošinājušies, lai aizsargātos no apkārtējās pasaules ietekmes. Šīs diplokoku ķēdītes salīp kopā ar polisaharīdu kapsulu, ko tie izmanto aizsardzībai pret fagocitozi. Zinot, ka šāds mikrobs mīt mūsu vidū, potenciālās briesmas jānovērš iespējami efektīvi un ilglaicīgi.
Vakcīnu vēsture un situācija šobrīd
Joprojām pasaulē ir divu veidu pneimokoku vakcīnas: PPSV (Pneumo 23) — vakcīna, kas satur tikai pneimokoku polisaharīdus, un konjugētās vakcīnas PCV10, PCV13, nu jau arī PCV15 un PCV20.
Lielākie polisaharīdu vakcīnas mīnusi — bērniem līdz divu gadu vecumam tā ir vāji imunogēna, imūnās atbildes veidošanā netiek iesaistītas T šūnas, veidojas slikta imūnā atbilde, sliktas afinitātes antivielas, kā arī polisaharīdu vakcīnas fenomens — dodot būsteri, antivielu paliek vēl mazāk, nekā bija pirms tam.
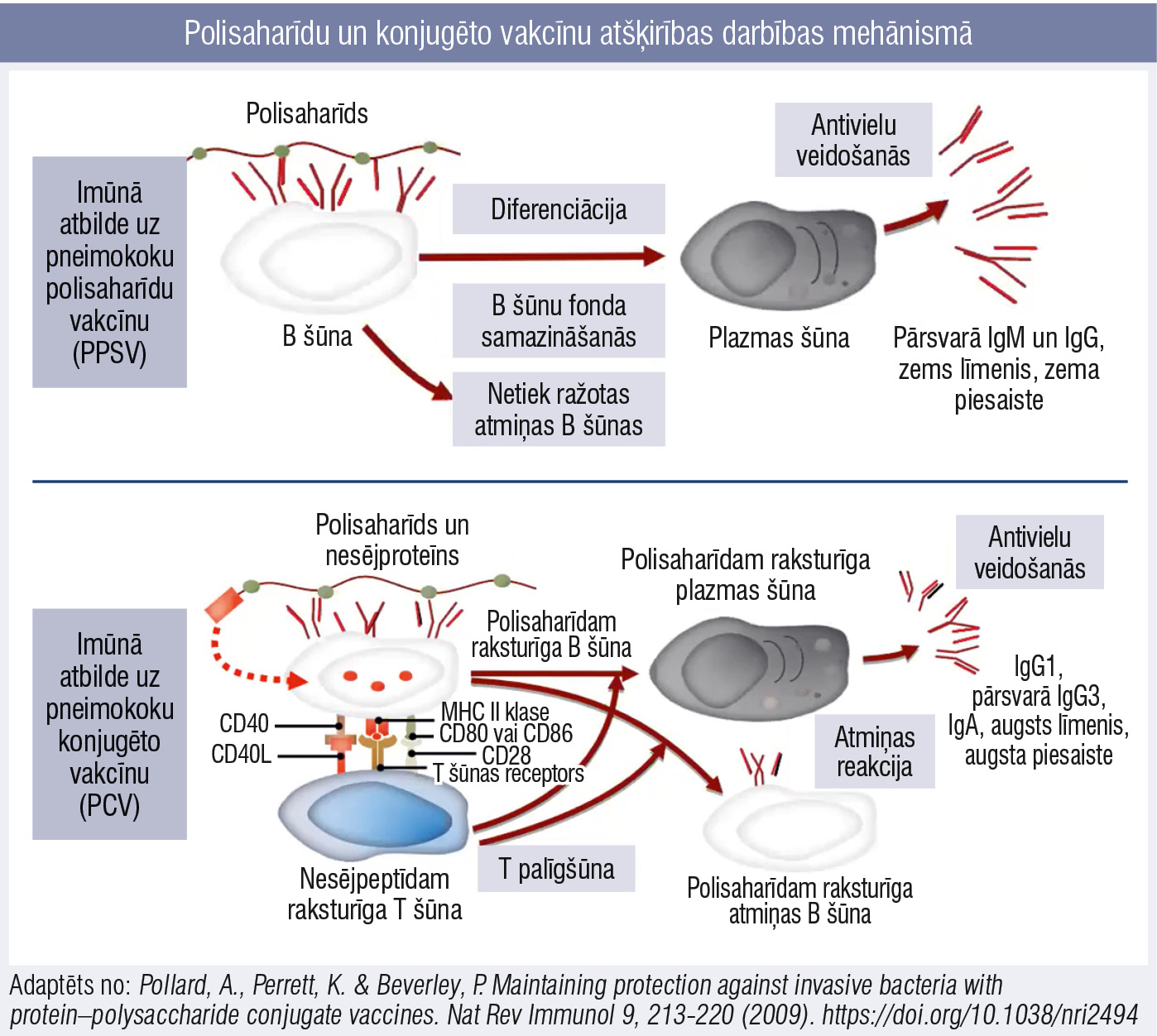

3. attēls
Polisaharīdu un konjugēto vakcīnu atšķirības darbības mehānismā
Tāpēc tika meklēti veidi, kā to mainīt, ņemot piemēru no H. influenzae B tipa vakcīnas veiksmes stāsta, attīstot konjugētās vakcīnas imunizācijā pret pneimokoku. Šobrīd pieaugušajiem konjugēto vakcīnu var ievadīt reizi dzīvē. Vakcīnu atšķirības 3. attēlā, serotipu pārklājums konjugētajās vakcīnās 4. attēlā.
PVO, EMA un FDA ziņo, ka PPSV vakcīnas nav rekomendējamas pneimokoku infekciju profilaksē, jo efektivitāte ir īslaicīga un nav ilglaicīgas ietekmes pat vienam indivīdam, nav ietekmes uz nazofaringeālo nēsāšanu, katra jauna vakcīnas deva vēl vairāk samazina imūnās sistēmas atbildi.


4. attēls
Pneimokoku vakcīnas aizsargā pret noteiktiem serotipiem
Konjugētās vakcīnas
Jāuzsver, ka, vakcinējot bērnus, uzskatāmi samazinām izplatību arī pieaugušo vidū. Ar šo vakcīnu palīdzību spēts pierādīt, ka PCV stimulē arī gļotādu imunitāti, novērš (ietekmē) nazofaringeālo kolonizāciju. Plaša PCV lietošana veicina kolektīvo aizsardzību, ievērojami arī nevakcinētiem bērniem un pieaugušajiem, un tā ir vakcīnas netiešā pozitīvā ietekme.
Vakcīnā tiek ielikti tie serotipi, kas ir bīstamāki, kam ir lielāks potenciāls saslimšanai salīdzinājumā ar citiem kopumā 100 zināmajiem serotipiem.
Vakcīnas tiešais efekts ir tās augstā efektivitāte pret serotipiem, kuri izraisa IPS un potenciālu letalitāti.
Vakcinācijas rekomendācijas
Latvijā PCV vakcīna iekļauta kalendārā kopš 2010. gada, vakcinēšanas intervāls bērniem: 2+1 (priekšlaikus dzimušajiem 3+1).
Īpaša uzmanība jāpievērš bērniem ar kohleārajiem implantiem — meningīta risks ir vismaz 40 × lielāks nekā populācijā. Ar HIV inficētiem bērniem IPS risks ir 100 × lielāks un var būt pirmā AIDS stadijas izpausme, noteikti jābūt vakcinētiem arī bērniem ar funkcionālo aspleniju vai citiem imūnkompromitētiem stāvokļiem.
Jau parādījušās jaunas rekomendācijas par jaunajām PCV15 un PCV20 vakcīnām, šobrīd gan tikai ASV: ja pieaugušais vecumgrupā 65+ iepriekš nav saņēmis konjugēto vakcīnu vai anamnēze nav zināma, jāsaņem PCV20 vienreizējā devā vai PCV15 + papildu vakcinācija ar PPSV23 pēc viena gada. Jaunākiem pacientiem (19+) PCV15 vai PCV20 rekomendē tad, ja ir noteikti riska faktori.
Riska grupu vakcinācijas iespējas
Ieguvums no vakcinācijas riska grupu pacientiem ir lielāks nekā pārējiem. Tās ir personas, kam fizioloģisku, sociālu, etnisku, profesionālu vai ekonomisku apstākļu dēļ ir paaugstināti ar slimību vai ar vakcīnām un vakcināciju saistītie riski.
Analizējot savu pacientu profilu, jāizvērtē, cik daudzi no pacientiem īstenībā iekļaujas riska kategorijās un kuriem nepieciešama pneimokoku imunizācija! Tie ir pacienti ar imūndeficītu (HIV, onkoloģiskām slimībām, cukura diabētu, orgānu vai cilmes šūnu transplantāciju, aspleniju, humorālās imunitātes defektiem, komplementa deficītiem, kohleāro implantu, cerebrospinālā šķidruma noplūdi), elpceļu slimībām (astmu, hronisku bronhītu, HOPS), noteiktu vecumu (< 2 gadiem vai > 65 gadiem), nelabvēlīgiem sociālekonomiskiem apstākļiem, smēķētāji, hronisku slimību pacienti (hroniskas sirds slimības, hroniska nieru slimība, aptaukošanās), alkoholiķi, ilgstoši dzīvojoši aprūpes iestādēs.
SPKC mājaslapā šobrīd aktualizētas praktiskas rekomendācijas vakcinācijai veseliem pieaugušajiem un riska grupu indivīdiem Latvijā (2022), pēc kurām strādāt aicināti visi veselības aprūpes speciālisti.
Pacienti ar imūnkompromitētu stāvokli — praktiski ieteikumi
Vakcinācija ar dzīvām novājinātām vakcīnām netiek rekomendēta ķīmijterapijas vai citas imūnsupresīvas terapijas laikā, kā arī onkoloģiskas pamatslimības radītās imūnsupresijas periodā, jo ir risks vakcīnas mikroorganismu proliferācijai un infekcijas attīstībai.
Imunizācija ar inaktivētām vakcīnām ķīmijterapijas vai citas imūnsupresīvas terapijas laikā netiek rekomendēta, jo vakcinācija var nebūt efektīva samazinātas imūnās sistēmas atbildes dēļ.
Tāpēc visas standarta vakcīnas atbilstoši rekomendācijām vēlams saņemt pirms ķīmijterapijas vai citas imūnsupresīvas terapijas sākšanas, pirms staru terapijas un pirms plānveida splenektomijas. Inaktivētās vakcīnas ievadāmas vismaz divas nedēļas pirms terapijas sākšanas, dzīvās novājinātās vakcīnas — ne mazāk kā četras nedēļas pirms plānotās terapijas.
Noslēgumā
Jebkura vakcinācija pacientiem ar riska faktoriem izvērtējama, pamatojot to ar imūnsupresijas pakāpi un iespējamo slimības attīstības perspektīvu. Svarīgākais — nenokavēt to brīdi, kad jau ir par vēlu. Tāpēc ik ārstam jāpārdomā savu pacientu atbilstība kādai no riska grupām — šo pacientu mūsu kartotēkā ir daudz vairāk, nekā sākumā domājam...
Raksts tapis ar PFIZER Luxembourg SARL filiāles Latvijā atbalstu, neietekmējot saturu